Clear Sky Science · de
Hochdurchsatz-Chemie-Proteomik-Workflow zur Kartierung der Dynamik der Protein‑Citrullinierung
Warum das Verändern von Proteinbausteinen wichtig ist
Unsere Zellen justieren ständig das Verhalten von Proteinen, indem sie nach deren Synthese kleine chemische Modifikationen anbringen. Eine solche Modifikation, die Citrullinierung genannt wird, verändert subtil die Ladung einer häufigen Aminosäure und kann die Faltung von Proteinen, ihre Bindung an DNA oder ihre Wechselwirkungen mit anderen Molekülen beeinflussen. Diese winzigen Anpassungen werden zunehmend mit Autoimmunerkrankungen, Infektionen, Krebs und Gehirnfunktionen in Verbindung gebracht — sie sind jedoch notorisch schwer nachzuweisen. Diese Studie stellt einen Hochdurchsatz-Laborworkflow vor, der es erstmals ermöglicht, Citrullinierung über Tausende von Proteinen hinweg zu kartieren und aufzuzeigen, wann und wo sie in Geweben und Immunzellen auftritt.
Ein verborgener Schalter an Proteinen
Citrullinierung tritt auf, wenn Enzyme namens PADs die Aminosäure Arginin chemisch modifizieren und deren positive Ladung entfernen. Diese scheinbar kleine Veränderung kann die Packung der DNA lockern, die Steifigkeit struktureller Proteine verändern oder die Erkennung körpereigener Gewebe durch das Immunsystem beeinflussen. Abnorme Citrullinierung wird mit rheumatoider Arthritis, neurodegenerativen Erkrankungen, Virusinfektionen und Krebs in Verbindung gebracht. Citrullinierte Proteine sind jedoch selten und lassen sich leicht mit anderen, häufigeren Modifikationen verwechseln, weshalb gängige Massenspektrometriemethoden sie oft übersehen. Das Ergebnis ist, dass Forschende nur eine fragmentarische Sicht auf das gesamte „Citrullinom“ — die Gesamtheit citrullinierter Proteine — hatten.
Eine zweistufige „Tag‑and‑Catch“-Strategie
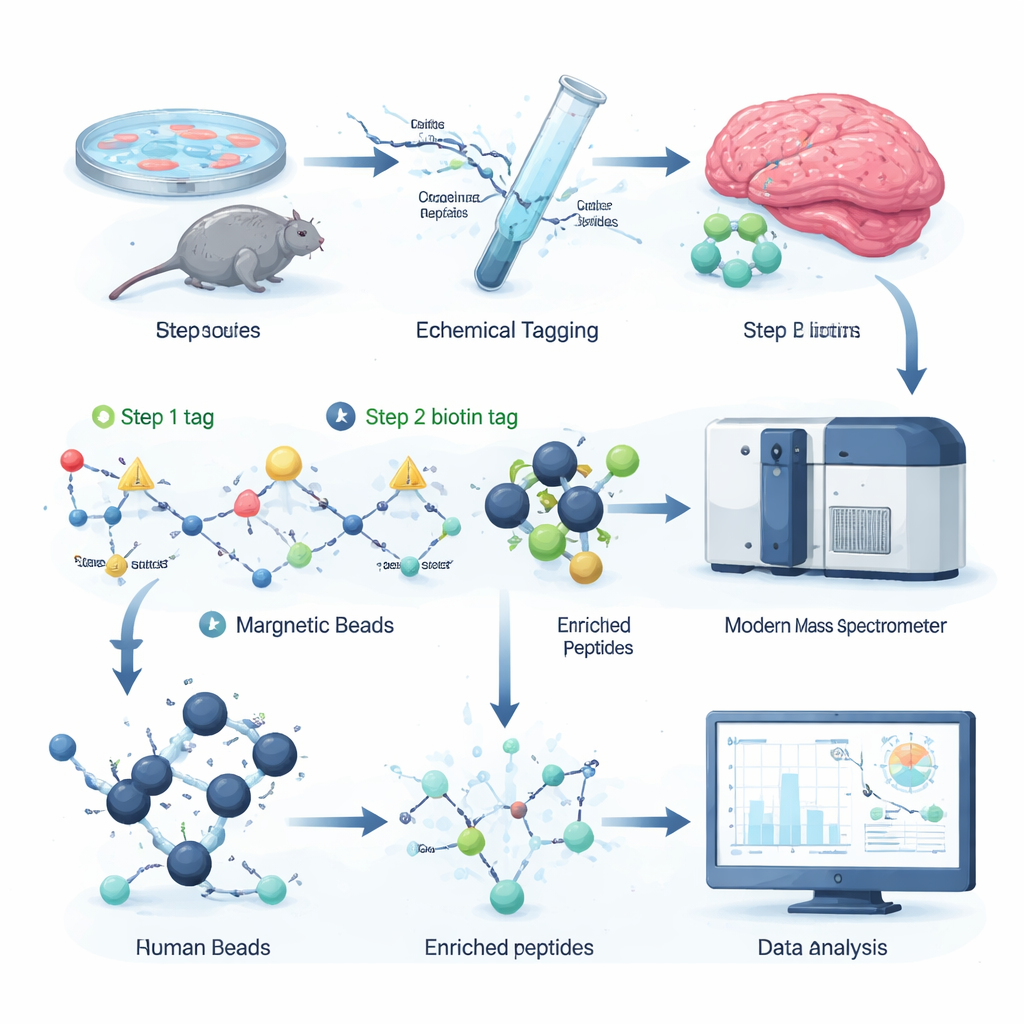
Die Autorinnen und Autoren entwickelten eine chemische Markierungsstrategie, die selektiv einen abnehmbaren „Griff“ an citrullinierte Stellen in Peptiden anbringt — den Proteinfragmenten, die in der Massenspektrometrie analysiert werden. Im ersten Schritt erkennt ein kleines reaktives Molekül Citrullin und bindet ein winziges Tag. Im zweiten Schritt wird ein größeres Biotin‑Tag per Click‑Chemie angebracht, sodass die markierten Peptide mit Streptavidin‑Beads — einem gebräuchlichen biochemischen Werkzeug — aus einer komplexen Mischung herausgefangen werden können. Eine schonende chemische Behandlung entfernt dann den sperrigen Teil des Tags und hinterlässt eine kleine, klar definierte Massenverschiebung, die das Massenspektrometer leicht detektieren kann. Da alle Reagenzien kommerziell verfügbar sind und das gesamte Protokoll in 96‑Well‑Platten passt, ist der Workflow schnell, skalierbar und mit bestehenden Proteomik‑Setups kompatibel.
Mehr vom Citrullinom sichtbar machen
Indem das Team bekannte citrullinierte Peptide in Zellextrakte einspikte und systematisch verdünnte, zeigte es, dass ihre Anreicherungsstrategie das Signal citrullinierter Peptide mehr als verzehnfacht — selbst wenn diese weniger als eines von tausend Molekülen ausmachen. In komplexen Proben stieg nach der Anreicherung sowohl die Zahl der detektierten citrullinierten Stellen als auch ihre gemessenen Intensitäten dramatisch an. Die Anwendung der Methode auf Mausgehirngewebe ergab zwei- bis dreimal mehr verschiedene Citrullinierungsstellen als ein vorheriger Stand‑der‑Technik-Ansatz, darunter viele an dem Myelin‑Basic‑Protein, das Nervenfasern isoliert, und an Proteinen, die an der synaptischen Kommunikation beteiligt sind. Dies deutet darauf hin, dass Citrullinierung sowohl die Signalübertragung von Nervenzellen als auch die Erhaltung der Gehirnverdrahtung beeinflussen könnte.
Immunzellen, die klebrige Proteinnetze auswerfen
Neutrophile, eine vorderste weiße Blutkörperchen‑Population, können Eindringlinge bekämpfen, indem sie klebrige Netze aus DNA und Proteinen ausstoßen, sogenannte neutrophile extrazelluläre Netze (NETs). Die NET‑Bildung hängt von PAD4 ab, einem citrullinierenden Enzym, das Chromatin auflockert, sodass DNA entweichen kann. Mithilfe ihres neuen Workflows verfolgten die Forschenden, wie sich Citrullinierung in menschlichen Neutrophilen veränderte, die zunehmenden Dosen eines chemischen Aktivators ausgesetzt waren. Sie detektierten bis zu 1.700 citrullinierte Peptidfragmente in 580 Proteinen, wobei Hunderte von Stellen dosisabhängig anstiegen oder abnahmen, während die Gesamtproteinmengen konstant blieben. Histone — die Proteine, die DNA verpacken — zeigten weitverbreitete Citrullinierung, nicht nur an wenigen klassischen Stellen, und Varianten des Linkerhistons H1 waren besonders modifiziert. Strukturproteine wie Aktinregulatoren und Lamin B, das die Kernhülle formt, waren ebenfalls stark citrulliniert, was auf ein koordiniertes Erweichen sowohl des Chromatins als auch des zellulären Gerüsts während der NET‑Freisetzung hindeutet.
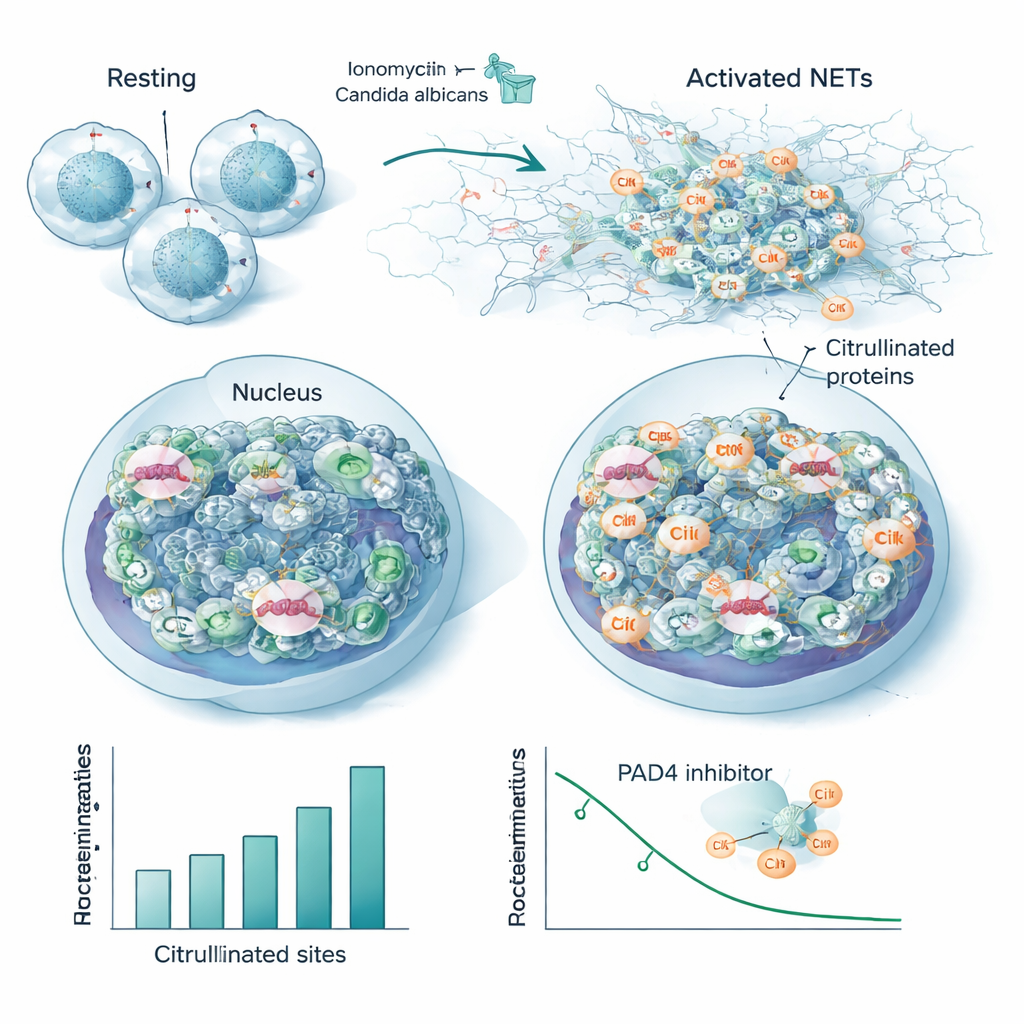
Eine Kern‑Citrullinierungs‑Signatur bei Infektionen
Um eine echte Infektion zu simulieren, stimulierte das Team Neutrophile mit hitzeinaktiviertem Candida albicans, einem häufigen Pilzpathogen. Obwohl dies insgesamt weniger modifizierte Stellen erzeugte als der starke chemische Aktivator, überschritten sich die überwiegende Mehrheit der citrullinierten Proteine und Positionen zwischen den beiden Auslösern. Diese Überlappung definiert ein konserviertes „Kern‑Citrullinom“, das mit der NET‑Bildung assoziiert ist, darunter viele nukleäre und zytoskelettale Proteine sowie mehrere bekannte Autoantigene — genau die Ziele von Antikörpern bei Autoimmunerkrankungen. Als die Forschenden ein PAD4‑blockierendes Medikament hinzugaben, verloren viele dieser Stellen dosisabhängig ihre Citrullinierung, was sie direkt mit der Aktivität des Enzyms verknüpft und darauf hindeutet, dass sie als empfindliche Messgrößen für die PAD4‑Hemmung dienen könnten.
Was das für Gesundheit und Krankheit bedeutet
Indem dieser Workflow eine schwer fassbare Modifikation in ein messbares Signal verwandelt, macht er es möglich, zu kartieren, wo und wann Citrullinierung in Geweben, Immunantworten und Krankheitsmodellen auftritt. Für Nicht‑Spezialisten lautet die zentrale Botschaft, dass Citrullinierung wie ein subtiler molekularer Dimmer an Proteinen wirkt — und die Fähigkeit, ihre Muster in hoher Auflösung zu sehen, könnte helfen zu erklären, wie Autoimmunerkrankungen entstehen, wie Infektionen Immunzellen umgestalten und wie sich Gehirnproteine im Laufe der Zeit verändern. Die Skalierbarkeit der Methode und die Nutzung gängiger Laborausrüstung bedeuten, dass sie breit übernommen werden kann, was die Tür zu neuen Wirkstoffzielen, präzisen Diagnosen und einem tieferen Verständnis dafür öffnet, wie kleine chemische Änderungen große biologische Folgen haben können.
Zitation: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Schlüsselwörter: Citrullinierung, Autoimmunerkrankung, Neutrophile extrazelluläre Netze, Massenspektrometrie, posttranslationale Modifikation