Clear Sky Science · de
Mechanistische Einblicke in die Nichtgleichgewichts-Thermodynamik der Stickstofffixierung durch akustische Kavitation
Luft mit Schall in nutzbaren Dünger verwandeln
Stickstoff aus der Luft ist für Dünger und Nahrungsmittelproduktion unverzichtbar, aber die Umwandlung dieses hartnäckigen Gases in nutzbare Formen erfordert meist riesige Anlagen, extreme Hitze und hohen Druck. Diese Studie untersucht einen sehr anderen Ansatz: intensive Schallwellen erzeugen winzige, explodierende Blasen im Wasser, die Stickstoff unter weit vom Gleichgewicht entfernten Bedingungen „fixieren“ können. Durch Beobachtung und Modellierung dessen, was in diesen flüchtigen Hotspots geschieht, zeigen die Forscher, wie schallgetriebene Blasen einen neuen Weg eröffnen könnten, stickstoffhaltige Chemikalien ohne herkömmliche Katalysatoren oder gigantische Reaktoren herzustellen.
Warum Stickstofffixierung so schwierig ist
Unsere Atmosphäre besteht größtenteils aus Stickstoffgas, doch die Atome sind durch eine der stärksten chemischen Bindungen der Natur miteinander verbunden. Dieses Gebilde effizient aufzubrechen ist der Grund, weshalb der Haber–Bosch-Prozess leistungsstarke Anlagen benötigt und weltweit große Energiemengen verbraucht. Konventionelle Methoden müssen einen schwierigen Kompromiss finden: Temperaturen hoch genug, um Stickstoff zu aktivieren, aber nicht so hoch, dass die gewünschten Produkte zerfallen oder das Gleichgewicht die Reaktion rückwärts treibt. In diesem Papier wird argumentiert, dass es statt einer konstanten Temperaturführung effektiver sein kann, kurzzeitig zu überschiessen – mithilfe ultraschneller Hitzeimpulse – und dann so schnell abzukühlen, dass nützliche Produkte eingefroren werden, bevor sie zerfallen.
Ultraschall als Erzeuger winziger Reaktionskammern
Wenn starker Ultraschall durch Wasser läuft, entstehen mikroskopische Gasblasen, die wachsen und dann heftig kollabieren – ein Phänomen, das als akustische Kavitation bekannt ist. Jede kollabierende Blase verhält sich wie ein winziger, kurzlebiger Reaktor. In Milliardstel Sekunden wird das Gas im Inneren auf Temperaturen über 5000 Kelvin komprimiert und dann mit Abkühlraten nahe 1012 Kelvin pro Sekunde wieder abgekühlt. Unter diesen Bedingungen können Stickstoffmoleküle in der Blase in reaktive Fragmente zerfallen, die sich dann mit Sauerstoff-, Wasserstoff- oder wasserabgeleiteten Fragmenten zu Nitrit, Nitrat oder Ammonium verbinden. Die neuen Produkte werden anschließend in die umgebende Flüssigkeit geschleudert, wo sie sich im Laufe der Zeit ansammeln, während die nächste Generation von Blasen entsteht und kollabiert. 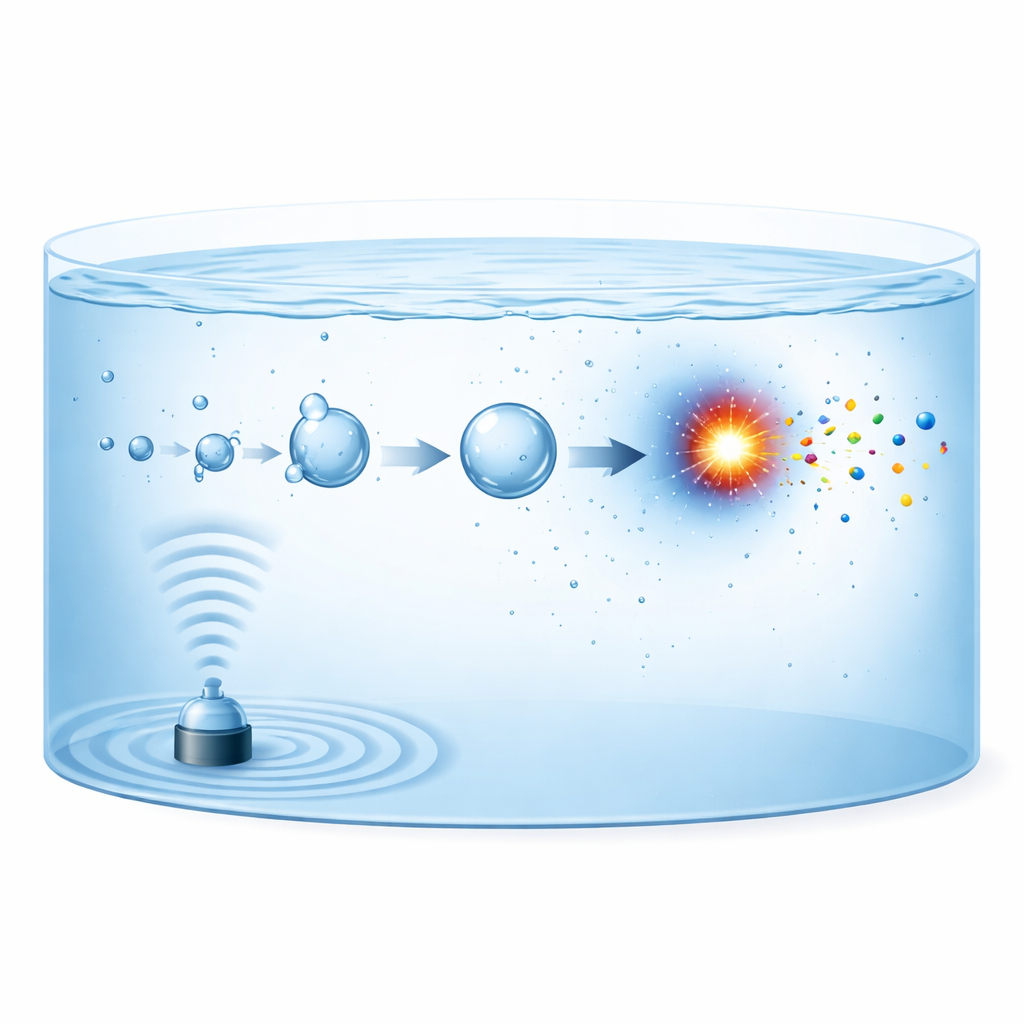
Bubbles abstimmen, um verschiedene Produkte zu wählen
Das Team variierte systematisch die Gase, die die Blasen speisten (Stickstoff plus Sauerstoff oder Wasserstoff), die Stärke und Frequenz des Ultraschalls sowie das Vorhandensein fester Partikel, die die Blasenbildung unterstützen. Bei Stickstoff–Sauerstoff-Gemischen erzeugte das System überwiegend oxidierte Produkte wie Nitrit und Nitrat; bei Stickstoff–Wasserstoff-Gemischen wurde Ammonium bevorzugt. Kleine Mengen Talkpartikel wirkten als Blasensamen, senkten die Kavitationsthresholds und machten die Reaktionen reproduzierbarer. Durch Anpassung des Schalldrucks und der Reaktionszeit konnten die Forschenden das Verhältnis von Nitrit zu Nitrat verschieben, was zeigt, dass ein Teil der Chemie im Inneren der kollabierenden Blase stattfindet und ein Teil in der umgebenden Flüssigkeit weiterläuft, während reaktive Fragmente langsam Nitrit in stärker oxidiertes Nitrat umwandeln.
Einblick in den nanoskaligen Wärmeimpuls
Um zu verstehen, warum so extreme, flüchtige Bedingungen dennoch stabile Produkte liefern, kombinierten die Autorinnen und Autoren Messungen mit detaillierten Simulationen und quantenchemischen Berechnungen. Diese zeigen, dass Stickstoff bei sehr hohen Temperaturen direkt in der Gasphase auseinanderbrechen kann und so Reaktionswege öffnet, die sonst nicht zugänglich sind. Dieselben Berechnungen zeigen aber auch, dass ein dauerhaft heißes Gas die Endprodukte instabil machen würde. Entscheidend ist das schnelle Abschrecken: Der Temperaturspike der Blase aktiviert Stickstoff, dann stabilisiert die nahezu sofortige Abkühlung Zwischenfragmente und fertige Moleküle wie Ammoniak und salpetrige Säure, bevor sie zerfallen oder wieder zu Stickstoff werden können. Die Modellierung einzelner Blasen, insbesondere wenn sie mit Argon dotiert sind, das die Kollapstemperaturen erhöht, bestätigte, dass höhere Spitzentemperaturen die Produktmischung verschieben und die Gesamtfixierraten steigern. 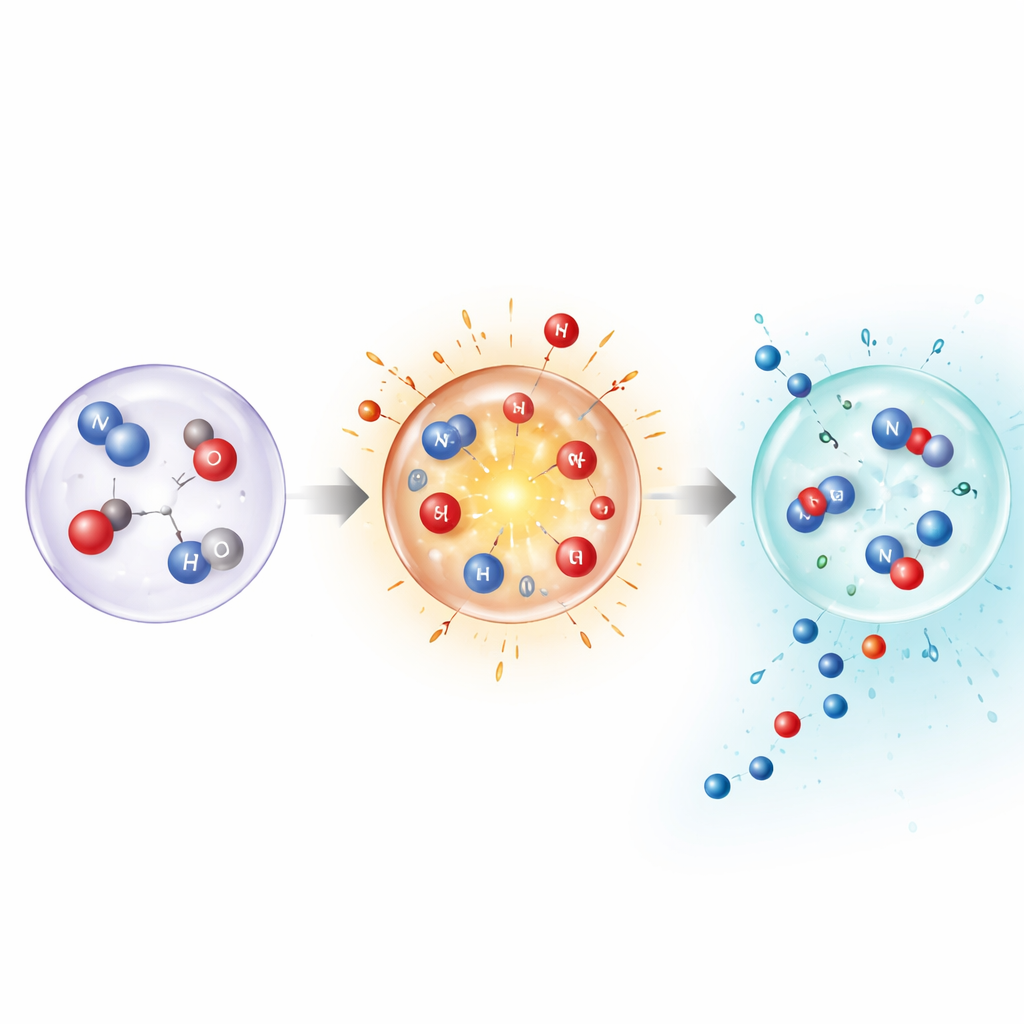
Energieverbrauch und zukünftige Möglichkeiten
Obwohl diese schallgetriebene Methode noch nicht so energieeffizient ist wie die besten industriellen Prozesse, liegt ihre Leistung bereits auf Augenhöhe mit historischen Lichtbogenverfahren und einigen modernen Plasmasystemen – und das bei Gesamtbedingungen nahe Raumtemperatur und ohne feste Katalysatoren. Wichtig ist, dass dieselben Kavitationsevents auch Wasser spalten und so Wasserstoff, Sauerstoff und Wasserstoffperoxid freisetzen können – energiereiche Nebenprodukte, die neben fixiertem Stickstoff genutzt werden könnten. Die Autorinnen und Autoren betonen, dass ihr Versuchsaufbau darauf ausgelegt ist, Mechanismen offenzulegen und nicht die Ausbeute zu maximieren, doch die Arbeit etabliert akustische Kavitation als einen eigenständigen Weg zur Stickstofffixierung, der extrem schnelle thermische Zyklungen in mikroskopischen Blasen ausnutzt. Für Nichtfachleute lautet die Quintessenz: Sorgfältig gesteuerter Schall kann gewöhnliches Wasser und Luft durch eine Abfolge winziger, unsichtbarer Explosionen in Düngerbausteine verwandeln und deutet auf grünere und flexiblere Wege zur Herstellung lebenswichtiger Stickstoffchemikalien in der Zukunft hin.
Zitation: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Schlüsselwörter: Stickstofffixierung, akustische Kavitation, Sonochemie, Düngerproduktion, Ultraschallchemie