Clear Sky Science · de
Plasmodium-ARK1 reguliert die Spindelbildung während atypischer Mitose und bildet einen abgewandelten chromosomalen Passenger-Komplex
Wie sich Malariaparasiten auf überraschende Weise teilen
Malariaparasiten wechseln ihr Leben lang zwischen Menschen und Mücken und vermehren sich rasant im Blut und im Mückendarm. Dazu teilen sie ihre Zellen auf Weisen, die deutlich von den Lehrbuchdarstellungen der menschlichen Zellteilung abweichen. Diese Studie enthüllt, wie ein Schlüsselenzym namens ARK1 diese ungewöhnlichen Teilungsprozesse steuert und warum es ein attraktives Ziel für neue Antimalaria-Wirkstoffe sein könnte.
Zwei sehr unterschiedliche Vermehrungsmodi
Die Malariaparasiten der Gattung Plasmodium nutzen mindestens zwei auffallend verschiedene Formen der Zellteilung. Innerhalb menschlicher roter Blutkörperchen durchlaufen sie die Schizogonie: Ein Parasitennukleus teilt sich vielfach, ohne dass die Zelle sich spaltet, sodass ein Bündel von Kernen entsteht, aus dem später Dutzende neue Parasiten abschnüren. In der Mücke durchlaufen die männlichen Geschlechtszellen eine blitzschnelle Teilung, die als männliche Gametogonie bezeichnet wird: Die DNA wird in wenigen Minuten dreimal repliziert und bildet ein achtfaches Genom, das dann schnell in acht spermienähnliche, Geißel tragende Zellen verpackt wird. Beide Teilungsformen finden innerhalb eines intakten Zellkerns statt und beruhen auf einer spezialisierten Struktur, dem mikrotubulus-organisierenden Zentrum (MTOC), das die winzigen Fasern aufbaut, die die Chromosomen auseinanderziehen.
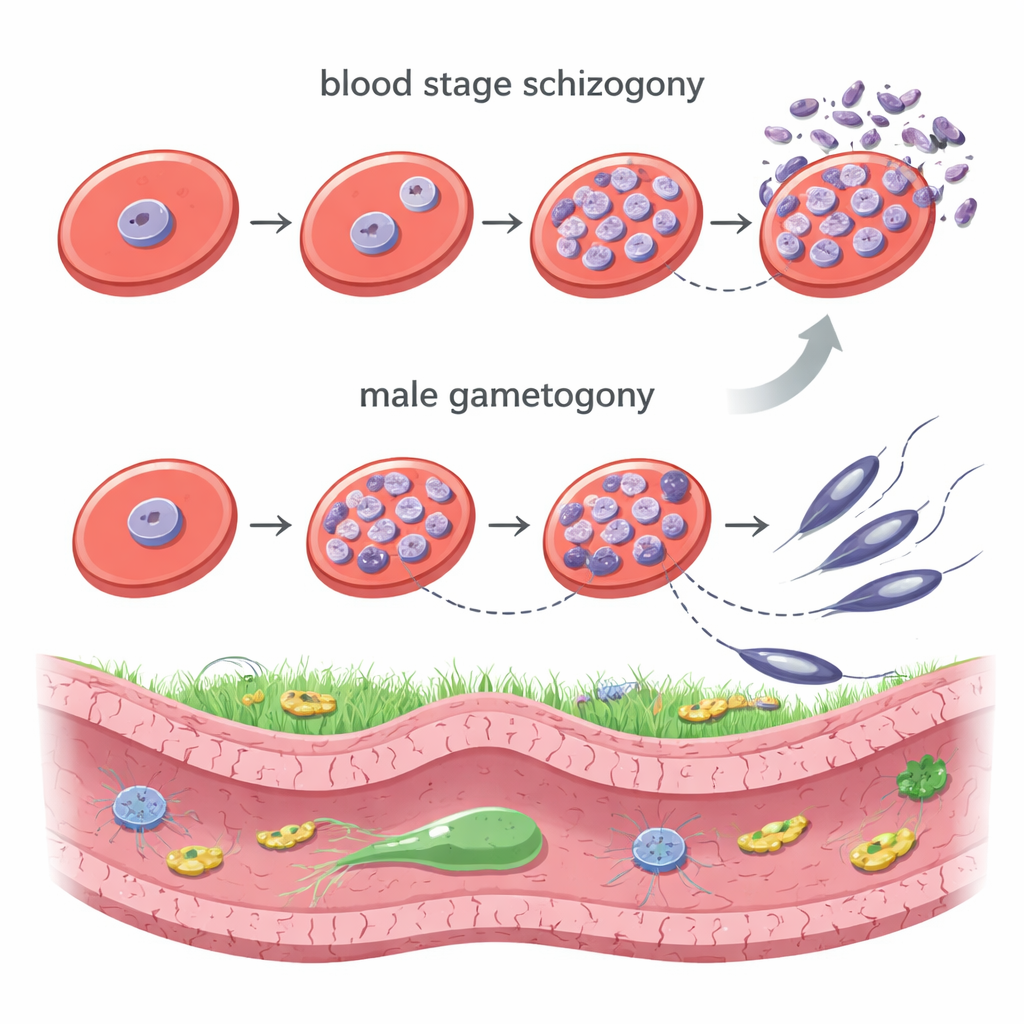
Ein Hauptschalter für den Aufbau der Teilungsmaschinerie
Die Autoren konzentrierten sich auf ein Enzym namens Aurora-verwandte Kinase 1 (ARK1), das zu einer Proteinfamilie gehört, die in vielen Organismen als Hauptschalter der Zellteilung fungiert. Mit genetischen Methoden in zwei Malariaarten — Plasmodium falciparum, das Menschen befällt, und Plasmodium berghei, das Nagetiere infiziert — markierten sie ARK1 mit fluoreszierenden Markern, um seine Lokalisation zu verfolgen, und entfernten es teilweise oder vollständig, um zu sehen, was zusammenbricht. Hochauflösende Lebendbildgebung und Expansionsmikroskopie zeigten, dass ARK1 nur auftritt, wenn sich Kerne aktiv teilen. Es konzentriert sich im inneren Bereich des MTOC und entlang der mitotischen Spindel — des Faserbündels, das die Chromosomen trennt — statt gleichmäßig im Zellvolumen verteilt zu sein.
Was passiert, wenn ARK1 fehlt
Als die Forschenden ARK1 in Blutstadien herunterfuhren, setzte die frühe Entwicklung weiter ein, aber Probleme traten auf, sobald die Parasiten ihre Kerne teilen und in einzelne Tochterzellen segmentieren wollten. Spindeln blieben verkürzt oder waren desorganisiert, Kerne trennten sich nicht korrekt, und die entstehenden Klumpen potenzieller Tochterparasiten blieben häufig verschmolzen oder missgestaltet. Unter dem Mikroskop erschienen wichtige Oberflächen- und Membranstrukturen, die normalerweise ordentliche, traubenartige Ansammlungen neuer Parasiten umreißen sollten, stattdessen lückig und chaotisch. Die Parasitenzahlen fielen in der nächsten Infektionsrunde deutlich ab, was zeigt, dass ARK1 für ein effizientes Wachstum im Blut erforderlich ist.
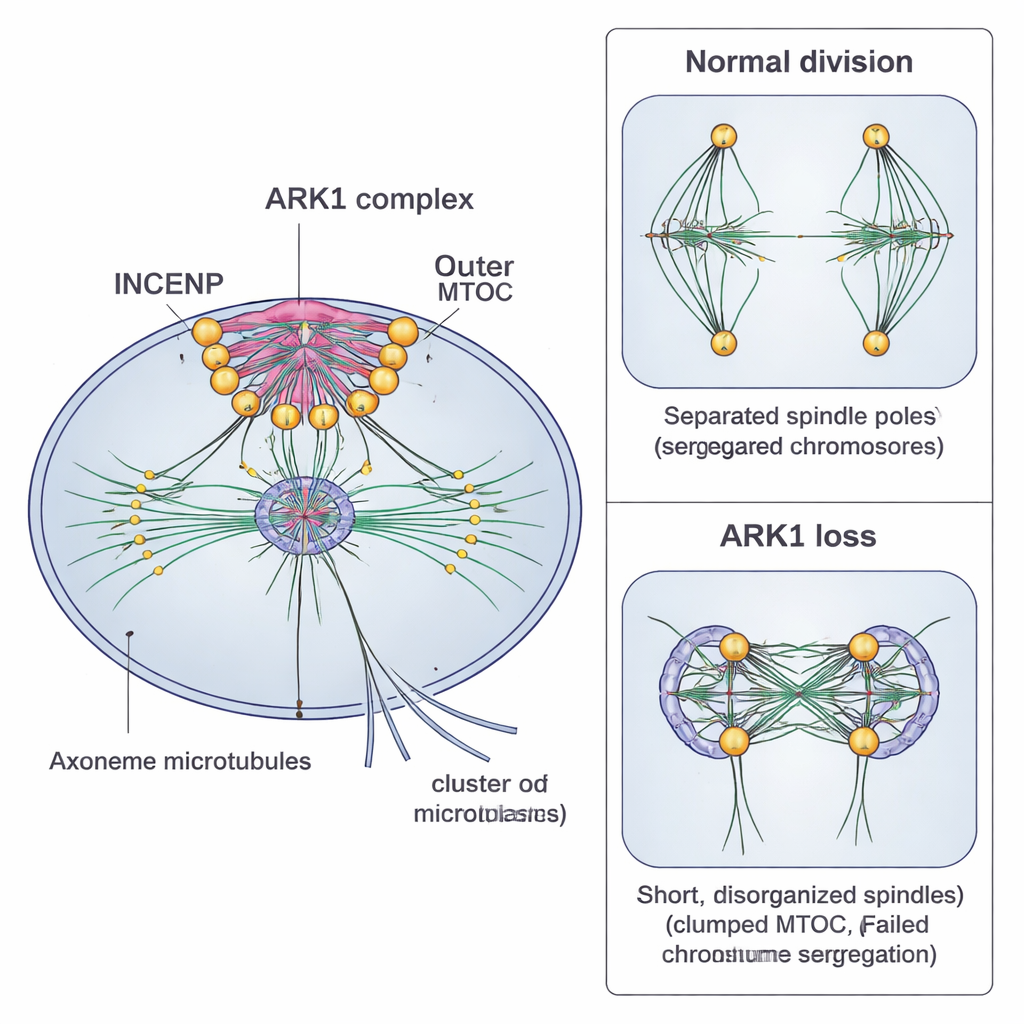
Blockade der Übertragung über die Mücke
Das Team reduzierte ARK1 auch während der sexuellen Entwicklung in der Mücke. In männlichen Gametozyten, die nach Aktivierung normalerweise innerhalb von etwa 15 Minuten flagellierte, spermienähnliche Zellen produzieren, führte die ARK1-Reduktion zu mehreren gleichzeitigen Ausfällen. Die inneren und äußeren Bereiche des MTOC klumpten statt sich zu trennen, Spindeln blieben kurz, und die langen, peitschenartigen Axoneme, die die Bewegung antreiben, waren schlecht ausgebildet. Infolgedessen entstanden sehr wenige funktionelle männliche Gameten, weniger befruchtete Eier entwickelten sich zu Ookineten und Oozysten, und deutlich weniger infektiöse Sporozoiten erreichten die Speicheldrüsen der Mücke. Die meisten Mücken, die diese geschwächten Parasiten trugen, übertrugen die Infektion nicht auf neue Mäuse.
Ein umgebauter Kontrollkomplex und neue Wirkstoffmöglichkeiten
Um zu verstehen, wie ARK1 gesteuert wird, isolierten die Forschenden es aus Parasiten und identifizierten Partnerproteine mittels Massenspektrometrie. Sie entdeckten, dass ARK1 den Kern eines ungewöhnlichen "chromosomalen Passenger"-Komplexes mit zwei Gerüstproteinen bildet, die INCENP-A und INCENP-B genannt wurden. In vielen anderen Organismen umfasst dieser Komplex zudem zwei zusätzliche Untereinheiten, Survivin und Borealin, die helfen, ihn an Chromosomen zu richten. Plasmodium und verwandte Parasiten scheinen diese Komponenten verloren zu haben und stattdessen das INCENP-Gerüst dupliziert zu haben, wodurch der Komplex um ARK1 und das innere MTOC neu angeordnet wurde. Vergleichende Genomanalysen deuten darauf hin, dass diese Umstrukturierung in verschiedenen Parasitenlinien wiederholt aufgetreten ist und verdeutlichen, wie flexibel das Werkzeugset der Zellteilung in der Evolution sein kann.
Warum das wichtig für die Bekämpfung von Malaria ist
Für Nichtfachleute ist die zentrale Botschaft, dass Malariaparasiten Kontrollsysteme für die Teilung nutzen, die sowohl essentiell als auch verschieden von denen des Menschen sind. ARK1 steht im Zentrum dieser parasitespezifischen Teilungsmaschinerie und koordiniert, wie Chromosomen getrennt und wie infektiöse Stadien sowohl im Menschen als auch in der Mücke gebildet werden. Da die Blockade von ARK1 das Parasitenwachstum im Blut stört und die Übertragung über Mücken nahezu zum Erliegen bringt, könnten Wirkstoffe, die auf den ARK1–INCENP-Komplex abzielen, prinzipiell in mehreren Lebenszyklusphasen wirken. Das macht ARK1 zu einem vielversprechenden Kandidaten für künftige antimalariale Strategien, die nicht nur Krankheit behandeln, sondern auch die Ausbreitung verringern.
Zitation: Nagar, A., Yanase, R., Zeeshan, M. et al. Plasmodium ARK1 regulates spindle formation during atypical mitosis and forms a divergent chromosomal passenger complex. Nat Commun 17, 1598 (2026). https://doi.org/10.1038/s41467-026-69460-7
Schlüsselwörter: Malaria-Zellteilung, Aurora-Kinase ARK1, Plasmodium-Mitose, chromosomaler Passenger-Komplex, Antimalaria-Wirkstoffziele