Clear Sky Science · de
Dreifache Zielsteuerung von STING, TGF-β und PD-L1 verstärkt CXCL16–CXCR6-Signale für eine starke Antitumorantwort
Kalte Tumoren erhitzen
Die Krebsimmuntherapie hat die Behandlung für einige Patientinnen und Patienten revolutioniert, doch viele Tumoren sind gegenüber diesen starken Wirkstoffen weiterhin resistent. Diese Studie untersucht, warum bestimmte Krebsarten modernen Immun-„Checkpoint“-Medikamenten trotzen, und schlägt einen intelligenteren, dreigleisigen Angriff vor, der die körpereigenen Abwehrkräfte weckt, hochspezialisierte Killer-T-Zellen anzieht und sie direkt im Tumor aktiv hält.
Warum aktuelle Immunmedikamente nicht ausreichen
Die meisten zugelassenen Immuntherapien richten sich gegen eine einzelne Bremse der Immunzellen, etwa den PD-1/PD-L1-Signalweg. Eine neuere Wirkstoffklasse versucht weiterzugehen, indem sie zusätzlich TGF-β blockiert, ein Molekül, das in fortgeschrittenen Tumoren die Immunantwort stark unterdrückt. Ein solcher Wirkstoff, YM101, kombiniert TGF-β- und PD-L1-Blockade in einem einzelnen Antikörper und zeigte vielversprechende Ergebnisse in Mäusen. Dennoch schrumpften manche Tumoren selbst bei genetisch identischen Tieren kaum. Beim Vergleich von ansprechenden und resistenten Tumoren fanden die Forschenden, dass erfolgreicher Therapieerfolg oft mit starker „angeborener“ Immunaktivierung einherging, insbesondere über den STING-Signalweg, der ungewöhnliche DNA erkennt und antiviralen Alarm auslöst.
Eine dritte Stellschraube: der STING-Weg
Da schwache angeborene Aktivierung als fehlendes Element vermutet wurde, kombinierten die Forschenden YM101 mit einem oral verabreichbaren STING-Agonisten namens MSA-2 in mehreren Maus-Tumormodellen, darunter typischerweise schwer zu behandelnde „kalte“ Tumoren. Der dreifache Ansatz — STING-Aktivierung plus TGF-β- und PD-L1-Blockade — verkleinerte Tumoren effektiver, verlängerte das Überleben und schützte Mäuse oft vor erneutem Tumorwachstum nach Wiederherausforderung, was auf langlebiges immunologisches Gedächtnis hindeutet. Dies übertraf die konventionellere Kombination eines STING-Agonisten mit alleiniger PD-L1-Blockade und verbesserte sogar die STING-Agonisten-Therapie, wenn nur TGF-β blockiert wurde, was zeigt, dass TGF-β selbst eine bedeutende Bremse für STING-getriebene Immunität darstellt. 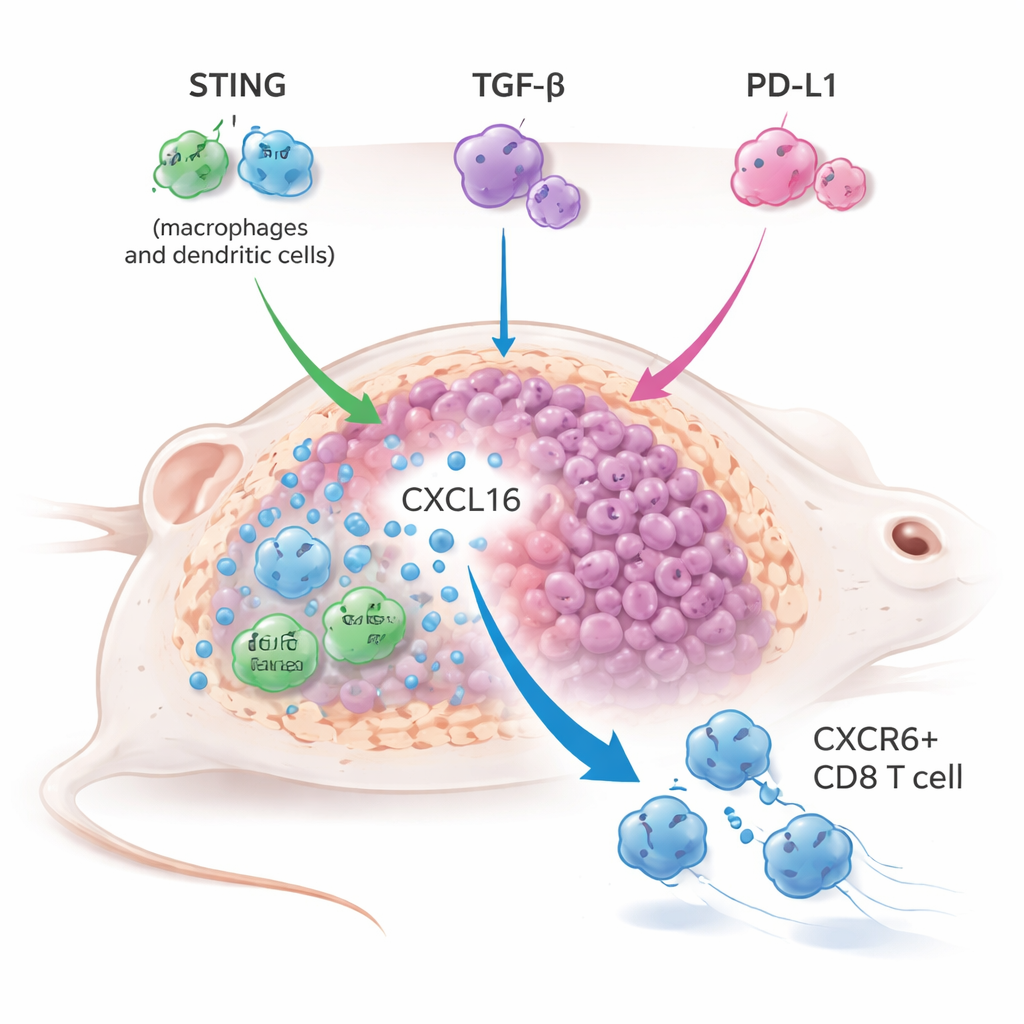
Rekrutierung einer spezialisierten Killertruppe
Um zu verstehen, wie diese Dreifachstrategie wirkt, nutzten die Forschenden Einzelzell-RNA-Sequenzierung und detailliertes Immunprofiling der behandelten Tumoren. Sie entdeckten eine auffällige Expansion einer bestimmten Killer-T-Zell-Untergruppe, die durch den Rezeptor CXCR6 gekennzeichnet ist. Diese CXCR6+ CD8-T-Zellen waren hoch gerüstet, mit starkem Ausdruck von Granzymen, Perforin und entzündungsfördernden Molekülen, und zeigten ausgeprägte Aktivierungs- und Proliferationszeichen. Gleichzeitig steigerten tumorzellassoziierte Makrophagen und dendritische Zellen die Produktion einer Chemokine namens CXCL16, die an CXCR6 bindet und hilft, diese T-Zellen im Tumor zu halten. Wenn die CXCL16–CXCR6-Verbindung unterbrochen wurde — entweder durch Blockade von CXCL16 oder durch genetisches Entfernen von CXCR6 in T-Zellen — verlor die kombinierte Behandlung weitgehend ihre antitumorale Wirkung, was beweist, dass diese Achse zentral für den Therapieerfolg ist.
Wie die Signalkaskade eingeschaltet wird
Tiefergehend fragten die Forschenden, wie STING-Aktivierung und TGF-β-Blockade gemeinsam CXCL16 steigern. In menschlichen und Maus-Immunzellen erhöhten STING-Agonisten stark CXCL16 und das antivirale Zytokin IFN‑β, während zugeführtes TGF-β beides deutlich reduzierte. Die Forschenden zeigten, dass STING IFN‑I-Signale auslöst, die den Transkriptionsfaktor STAT1 aktivieren; STAT1 bindet dann direkt an die Kontrollregion des CXCL16-Gens und schaltet es ein. TGF-β unterbricht diese Kette, indem es einen Schlüssel-Schritt der STING-Signalgebung stört, vermutlich über ein Protein namens HDAC4 und reaktive Sauerstoffspezies, wodurch IRF3-Aktivierung und nachfolgende IFN‑β- und CXCL16-Produktion abgeschwächt werden. Die Blockade von TGF-β entfernt diese Bremse, so dass STING-Agonisten den STAT1–CXCL16-Weg in myeloiden Zellen vollständig entzünden können und damit CXCR6+ T-Zellen die Signale liefern, die sie brauchen, um im Tumor zu verbleiben und zu kämpfen.
Bau eines einzelnen Präzisionswirkstoffs
Um dieses komplexe Regime praktischer und tumorfokussierter zu gestalten, konstruierten die Forschenden ein einzelnes „immunstimulierendes Antikörper-Konjugat“ namens Y101S. Dieses Molekül kombiniert den dualen TGF-β/PD-L1-blockierenden Antikörper mit einem STING-Agonisten, der über einen spaltbaren Linker angekoppelt ist. Y101S steuert PD-L1-positive myeloide Zellen im Tumor an, wird internalisiert und setzt dann das STING-Wirkstofffragment innerhalb dieser Zellen frei. In mehreren Maus-Tumoren erreichte Y101S die Wirksamkeit der Gabe von YM101 plus einem hoch dosierten freien STING-Agonisten oder übertraf sie sogar, obwohl es nur einen winzigen Bruchteil dieser STING-Dosis trug. Es steigerte CXCL16+ Makrophagen und dendritische Zellen, erweiterte CXCR6+ CD8-T-Zellen, induzierte dauerhaftes immunologisches Gedächtnis und konzentrierte entzündliche Signale im Tumor bei gleichzeitiger Schonung gesunder Organe, mit einem günstigen Sicherheitsprofil in Mäusen. 
Was das für die zukünftige Krebsbehandlung bedeutet
Für Laien ist die zentrale Botschaft, dass ein Angriff auf Krebs mit nur einem oder zwei Immun-Schaltern möglicherweise nicht ausreicht — besonders wenn Tumoren frühzeitige Alarmsysteme aktiv stilllegen. Diese Arbeit zeigt, dass die Kombination von STING-Aktivierung mit der Blockade von TGF-β und PD-L1 die Tumorumgebung umprogrammieren kann, gezielt eine spezialisierte Gruppe von Killer-T-Zellen anzieht und erhält und in präklinischen Modellen tiefere, langlebigere Antworten erzielt. Der dreifach zielgerichtete Antikörper–Wirkstoff Y101S verkörpert diese Strategie in einem einzigen, zielgerichteten Medikament und bietet eine Roadmap für die nächste Generation von Immuntherapien gegen Tumoren, die derzeit gegen Standard-Checkpoint-Medikamente resistent sind.
Zitation: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Schlüsselwörter: Krebsimmuntherapie, STING-Weg, TGF-beta-Blockade, PD-L1-Antikörper, CXCL16 CXCR6 T-Zellen