Clear Sky Science · de
Positive Kooperativität zwischen RAS-bindenden und cysteinhaltigen Domänen reguliert die RAF‑Membranbindungskinetik über laterales Wiederanheften
Warum dieser winzige molekulare Tanz wichtig ist
Im Inneren unserer Zellen werden Entscheidungen von Leben und Tod über Wachstum, Teilung und Überleben häufig an der Oberfläche der Zellmembran getroffen. Ein Schlüsselfaktor in diesen Entscheidungen ist ein Protein namens RAF, das Wachstumssignale weiterleitet und bei Krebs oft fehlerhaft geschaltet ist. Diese Studie enthüllt in beispielloser kinetischer Detailtiefe, wie RAF an Zellmembranen andockt, wie lange es dort verweilt und warum dichte Ansammlungen eines anderen Proteins, RAS, RAF länger aktiv halten können als erwartet.
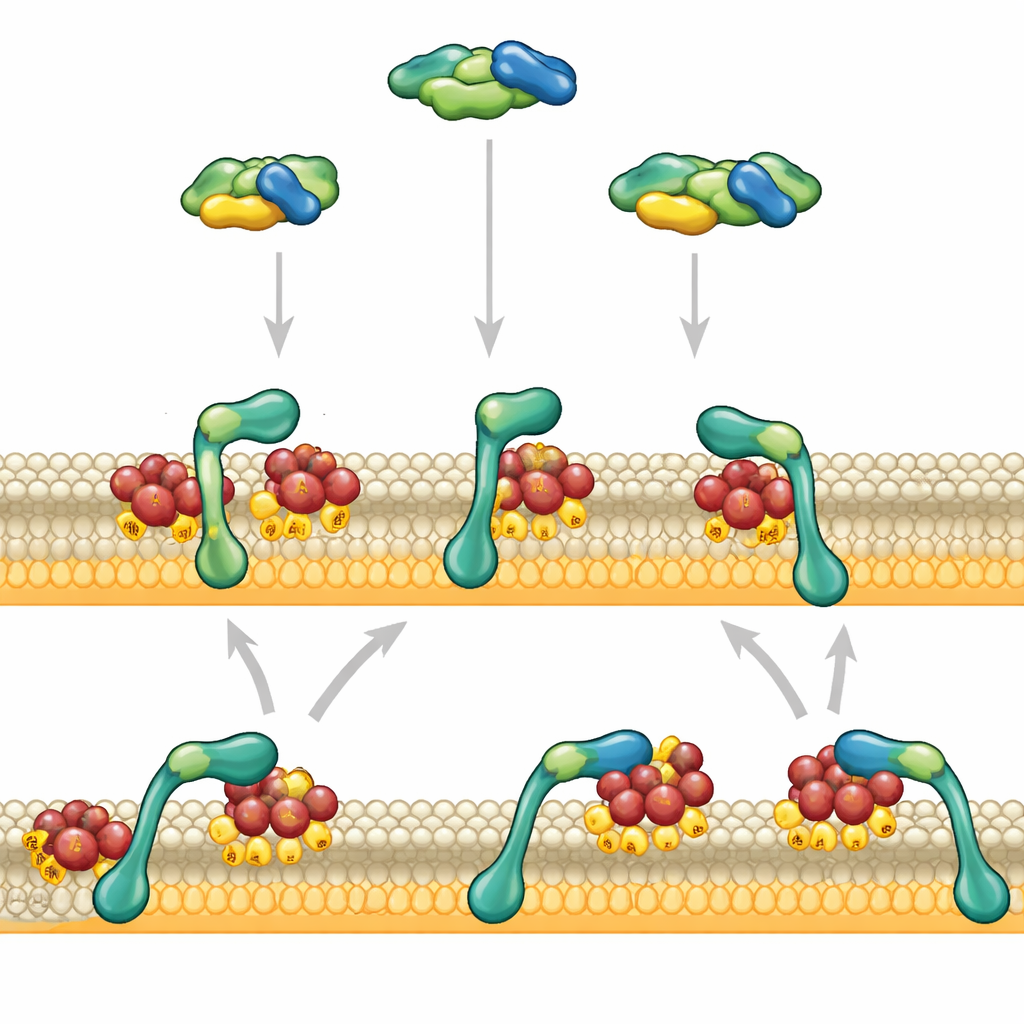
Signale treffen an der Zelloberfläche zusammen
RAF wirkt in einer wichtigen Signalstraße, bekannt als MAPK‑Pathway, die äußere Reize wie Wachstumsfaktoren mit Veränderungen der Genaktivität verknüpft. In seiner Ruhestellung schwimmt RAF gefaltet und selbstinhibiert im Zellinneren. Es wird nur eingeschaltet, wenn es auf RAS trifft, einen kleinen molekularen Schalter, der an der inneren Membranoberfläche verankert ist. RAS muss in seinem „ein“-Zustand sein und in der richtigen Lipidumgebung sitzen, damit RAF rekrutiert und aktiviert werden kann. Da RAF‑Moleküle im Vergleich zu vielen anderen Signalbestandteilen relativ selten sind, beeinflusst genau, wie sie mit der Membran interagieren und ein vorzeitiges Lösen vermeiden, stark, ob eine Zelle schwach oder stark auf ein Wachstumsignal reagiert.
Zwei Hände, um die Membran zu greifen
Die Autor:innen konzentrierten sich auf zwei Bereiche am Vorderende von RAF: einen, der RAS greift, und einen, der negativ geladene Membranlipide bevorzugt. Mit künstlichen Membranen und gereinigten Proteinen beobachteten sie einzelne RAF‑Fragmente, die mit fortschrittlicher Mikroskopie an RAS‑verzierten Oberflächen binden. Wenn die RAS‑bindende Region allein arbeitete, berührte sie die Membran nur kurz und löste sich in etwa einer Sekunde wieder. Die lipidliebende Region allein blieb praktisch gar nicht haften. Waren diese beiden Regionen jedoch verbunden, veränderte sich ihr Verhalten deutlich: RAF heftete jetzt stärker an und verharrte für Dutzende von Sekunden auf der Membran, besonders wenn die Membran viele negativ geladene Lipide trug, wie sie in echten Zellen vorkommen.
Zusammenarbeit, die das Verlieren verlangsamt
Diese dramatische Veränderung ergab sich nicht, weil RAF die Membran schneller fand, sondern weil es langsamer wieder verschwand. Zuerst erkennt die RAS‑bindende Sequenz von RAF aktiviertes RAS und verankert RAF an der Membran. Erst nach diesem ersten Händedruck bindet die lipidbindende Region vollständig an die umgebenden Lipide, was die seitliche Bewegung von RAF verlangsamt und es fester verankert. Dieser zweite Kontakt stabilisiert wiederum die ursprüngliche RAS–RAF‑Interaktion und schafft eine positive Rückkopplung zwischen Protein‑Protein‑ und Protein‑Lipid‑Kontakten. Experimente, in denen der kurze Linker verändert wurde, der die beiden Regionen verbindet, zeigten, dass ihre enge räumliche Koordination entscheidend ist: Wird der Linker flexibler oder länger, schwächt das RAFs Fähigkeit, auf der Membran zu verweilen.
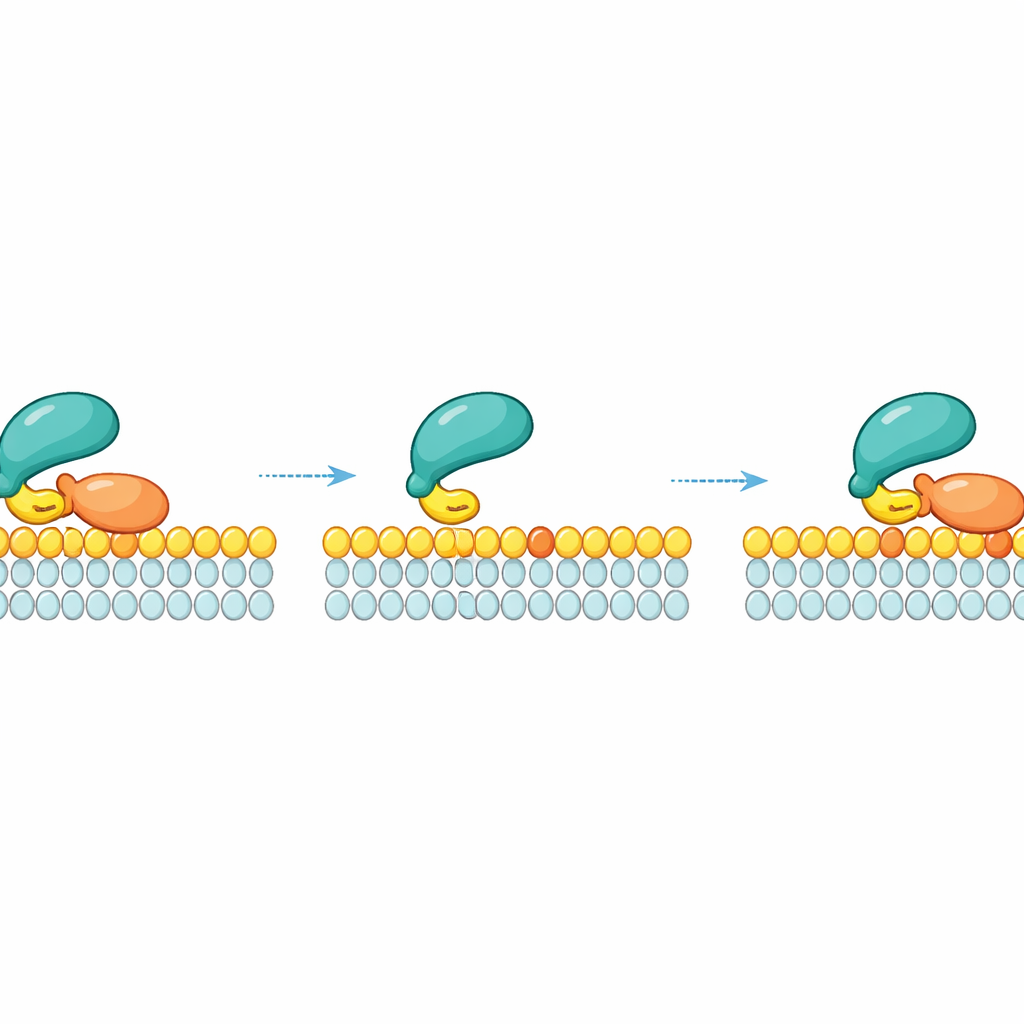
Laterales Wiederanheften: Gleiten statt Abfallen
Eine zentrale Einsicht der Arbeit ist, dass RAF sich nicht einfach in die umgebende Flüssigkeit löst, sobald es ein bestimmtes RAS‑Molekül verliert. Stattdessen kann RAF, nachdem RAS loslässt, kurz über seinen schwachen Lipidkontakt an der Membran verankert bleiben und seitwärts gleiten. In diesem transienten Zustand kann es ein benachbartes RAS‑Molekül auf demselben Membranpatch „wiederergreifen“. Dieses laterale Wiederanheften schafft ein kinetisches Sicherheitsnetz: Bei hoher lokaler RAS‑Dichte – etwa in Nanoklustern, in denen RAS‑Moleküle dicht gepackt sind – hat RAF viele Chancen, RAS erneut zu binden, bevor es wegdriftet. Messungen und Simulationen zeigten, dass je höher die Dichte aktiven RAS auf der Membran ist, desto länger verbleibt RAF durch diese wiederholten lokalen Wiederanheftungen an der Membran.
Von verlängerten Aufenthalten zu verlässlicher Aktivierung
Die verlängerte Verweildauer von RAF an der Membran hat wichtige Folgen. RAF‑Aktivierung ist kein einziger Akt, sondern eine mehrstufige Abfolge, die Formänderungen, Entfernung inhibitorischer Markierungen und die Paarung zweier RAF‑Moleküle zu einem aktiven Dimer umfasst. Die Studie legt nahe, dass nur RAF‑Moleküle, die lange genug auf der Membran verweilen, diese Abfolge abschließen können – eine Form des „kinetischen Proofreadings“, die Zellen hilft, versehentliche Aktivierung durch flüchtige, schwache Signale zu vermeiden. Indem sie offenlegt, wie das Zusammenspiel von RAS‑Bindung, Lipid‑Engagement und lateralem Wiederanheften RAFs Membranverweildauer bestimmt, skizziert die Arbeit eine allgemeine Strategie, mit der Zellen viele kleine, schwache Wechselwirkungen an Membranen nutzen können, um starke Signalwege fein zu justieren.
Zitation: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Schlüsselwörter: RAS, RAF‑Kinase, Signalübertragung an der Zellmembran, laterales Wiederanheften, kinetisches Proofreading