Clear Sky Science · de
Fehlen von MDA5 verzögert die hämatopoetische Alterung durch Modulation von Inflammaging und Proteostase bei Mäusen
Warum es wichtig ist, das Blut im Alter jung zu halten
Mit dem Alter verschleißt das System, das unsere Blutzellen herstellt, langsam. Stammzellen im Knochenmark, die normalerweise rote Blutkörperchen, Immunzellen und Blutplättchen erneuern, werden anfälliger für Entzündungen und produzieren eher bestimmte Zelltypen auf Kosten anderer. Diese Verschiebung trägt zu Anämie, geschwächter Immunantwort und einem höheren Krebsrisiko im Alter bei. Die hier zusammengefasste Studie untersucht einen überraschenden Akteur in diesem Prozess: einen antiviralen Sensor namens MDA5. Indem die Forschenden dieses einzelne Molekül bei Mäusen ausschalteten, konnten sie zeigen, dass sich die blutbildenden Stammzellen funktionell länger jünger verhielten.
Ein zur Virenabwehr gebauter Sensor, der mit dem Alter nachteilig wirkt
MDA5 ist ein angeborener Immun-Sensor, der doppelsträngige RNA erkennt, ein molekulares Muster, das bei Viren häufig ist, aber auch aus unseren eigenen Genomen stammt – insbesondere von mobilen genetischen Elementen, deren Aktivität im Alter zunimmt. Erkennt MDA5 solche RNA, löst er eine Kaskade entzündlicher Signale und antiviraler Antworten aus. Das Team fragte, ob diese konstante Niedrigstaktivierung in älteren Tieren das sogenannte „Inflammaging“ – die anhaltende, schwelende Entzündung, die mit dem Altern einhergeht – im Knochenmark antreiben könnte. Im Vergleich zwischen normalen Mäusen und Mäusen ohne MDA5 bestimmten sie viele Immun-Signalstoffe in der Knochenmarkflüssigkeit. Ältere Mäuse ohne MDA5 wiesen deutlich niedrigere Konzentrationen zentraler entzündlicher Zytokine auf, darunter Interferon-β und Interleukin-1, und zeigten eine verringerte Aktivierung entzündlicher DNA-Regionen in Stammzellen, was auf eine ruhigere, weniger entzündete Umgebung hindeutet.
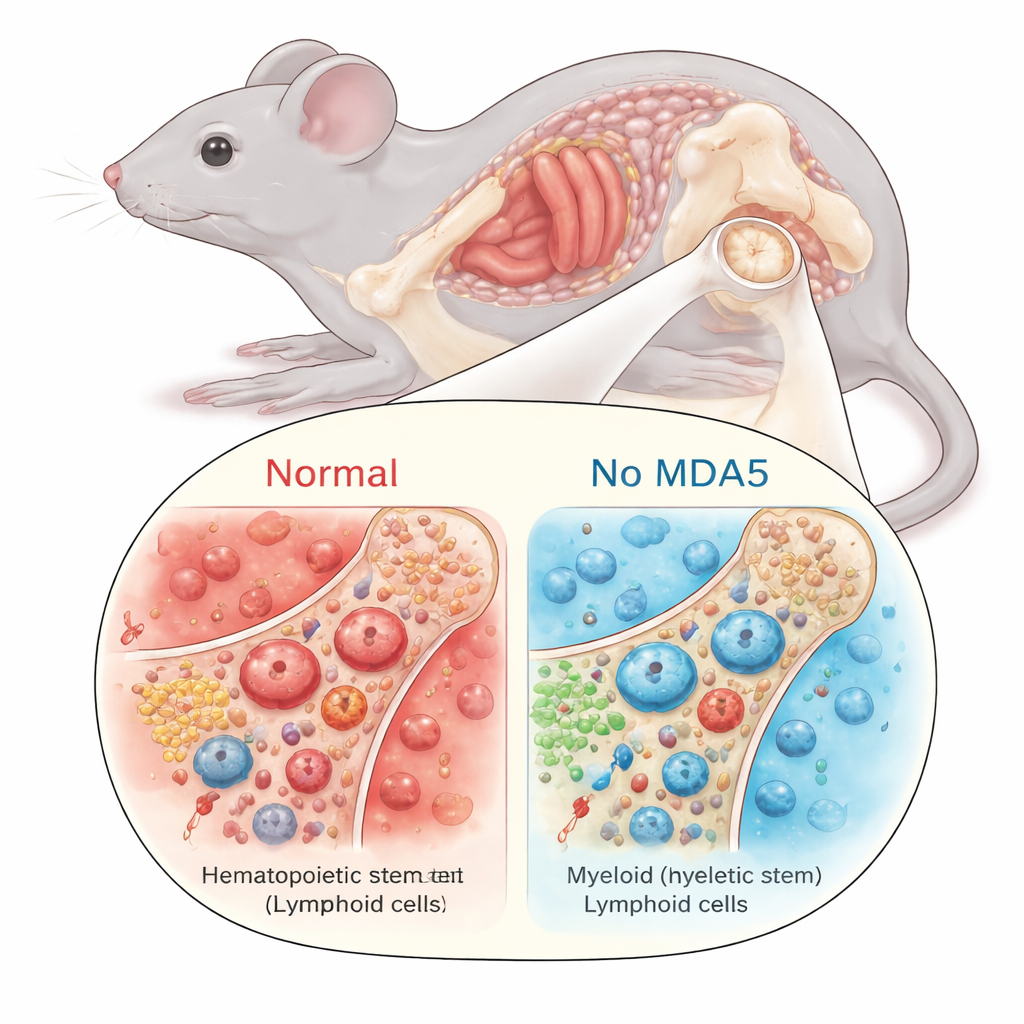
Jüngeres Verhalten alternder blutbildender Stammzellen
Bei geringerer Entzündung im Mark verhielten sich die blutbildenden Stammzellen anders. Bei normaler Alterung neigen diese hämatopoetischen Stammzellen (HSCs) dazu, sich in der Zahl anzusammeln, aber an Qualität zu verlieren: Sie teilen sich häufiger, verlieren ihre langfristige Regenerationskapazität und entwickeln eine Neigung zur Produktion myeloider Zellen (wie bestimmter weißer Blutkörperchen) statt lymphoider Zellen, die die adaptiven Abwehrkräfte unterstützen. Bei gealterten Mäusen ohne MDA5 war dieses typische Muster abgeschwächt. Ihre HSCs vermehrten sich weniger, zeigten eine reduzierte myeloide Voreinstellung und blieben ruhiger – sie verbrachten mehr Zeit in einem Ruhezustand statt im Zellzyklus. Als die Forschenden gleiche Zellzahlen von Stammzellen in bestrahlte Empfängermäuse transplantierten, konnten gealterte, MDA5-defiziente HSCs das Blutssystem in nicht-wettbewerblichen Einstellungen besser wiederaufbauen, was auf überlegene funktionelle Reserven im Vergleich zu gleichaltrigen normalen HSCs hinweist.
Metabolismus und Proteinqualitätskontrolle bleiben jünger
Über Zellzahlen und Verhalten hinaus untersuchten die Forschenden die inneren Abläufe dieser Stammzellen. Mithilfe von Genexpressionsanalysen, Chromatinzugänglichkeit, Metabolitenprofilen und Einzelzellanalyse fanden sie, dass der Verlust von MDA5 ein jüngeres Stoffwechsel- und Proteinwartungsprofil bewahrt. Gealterte MDA5-defiziente HSCs wiesen gesündere Redox-Marker auf, etwa niedrigere Spiegel von oxidiertem Glutathion und höhere Niveaus von NAD und NADP, Molekülen, die mit zellulärer Widerstandsfähigkeit verbunden sind. In diesen Zellen waren fehlgefaltete und entfaltete Proteine – ein Kennzeichen von Alterung und Stress – reduziert, während Marker der Autophagie, des Prozesses, mit dem Zellen beschädigte Komponenten recyceln, erhöht waren. Die Proteinsynthese war gedrosselt und Aminosäuren häuften sich an, was mit einer Hinwendung zu sorgfältiger Proteinqualitätskontrolle statt schneller, fehleranfälliger Produktion übereinstimmt.
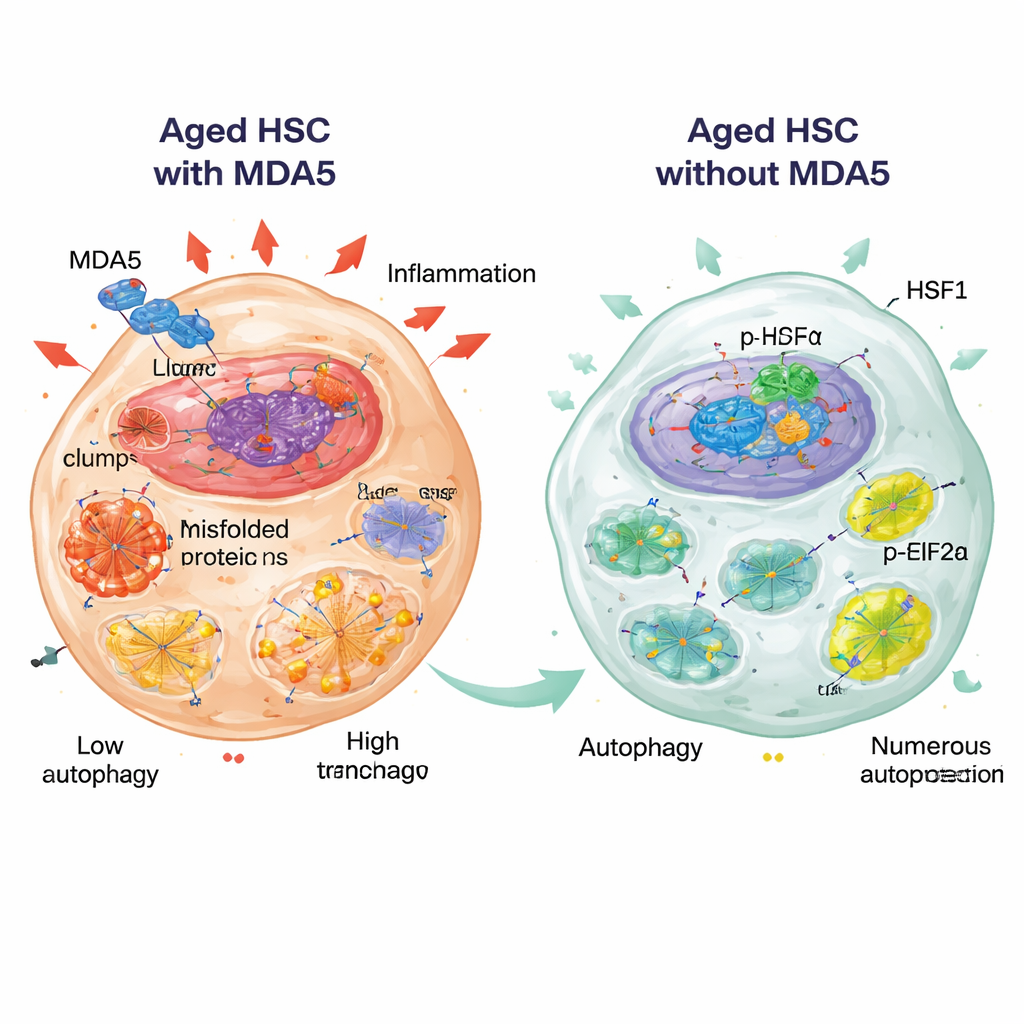
HSF1 und eIF2α: Wächter der Proteostase
Zwei molekulare Regulatoren traten als zentral für diesen Schutzzustand hervor: HSF1, ein übergeordneter Transkriptionsfaktor, der die Produktion von Chaperonen und anderen protektiven Faktoren erhöht, und eIF2α, ein Initiationsfaktor der Translation, dessen phosphorylierte Form (p-eIF2α) die Proteinsynthese bei Stress verlangsamt. In gealterten, MDA5-defizienten HSCs waren HSF1-Proteinspiegel und seine nukleare Lokalisation erhöht, und p-eIF2α war gesteigert, was zu einem aktiven Stressschutzprogramm passt. Die Autorinnen und Autoren fanden, dass MDA5 in die Nähe von HSF1 gelangen kann und bei Überexpression HSF1 im Zytoplasma zurückhalten kann, was nahelegt, dass aktives MDA5 HSF1s nützliche nukleare Funktionen einschränken könnte. Wichtig ist, dass bei pharmakologischer Aktivierung von HSF1 in gealterten normalen HSCs durch ein kleines Molekül diese Zellen ruhiger wurden und ihre Fähigkeit, über wiederholte Kulturrunden Kolonien zu bilden, besser bewahrten — was teilweise die jugendlichen Merkmale nachahmt, die beim Fehlen von MDA5 beobachtet wurden.
Was das für die gesunde Alterung des Bluts bedeutet
Zusammen zeichnen diese Befunde das Bild, dass die chronische Aktivierung eines antiviralen Sensors, MDA5, Blut bildende Stammzellen allmählich in Richtung Entzündung, metabolischen Stress und Proteinschäden drängt. Das Entfernen von MDA5 bei Mäusen unterbricht diesen Kreislauf: Entzündungssignale im Knochenmark werden gedämpft, HSCs bleiben ausgeruhter und weniger voreingenommen, und ihre internen Systeme zur Proteinqualitätskontrolle bleiben robust. Da das direkte Ausschalten von MDA5 beim Menschen wegen seiner Rolle in der Infektionsabwehr riskant wäre, hebt diese Arbeit das allgemeinere Prinzip hervor, dass die gezielte Bekämpfung altersbedingter Entzündung und die Stärkung der Proteostase helfen könnten, die Funktion hämatopoetischer Stammzellen im Alter zu bewahren. Langfristig könnten sicherere Wege, MDA5-assoziierte Signalwege zu modulieren oder HSF1- und eIF2α-getriebene Stressantworten zu stärken, Strategien bieten, um die gesunde Lebensspanne unseres Bluts und Immunsystems zu verlängern.
Zitation: Bergo, V., Bousounis, P., To Vu, G. et al. Lack of MDA5 delays hematopoietic aging by modulating inflammaging and proteostasis in mice. Nat Commun 17, 1645 (2026). https://doi.org/10.1038/s41467-026-69424-x
Schlüsselwörter: hämatopoetische Stammzellen, Inflammaging, MDA5, Proteostase, alterndes Blut