Clear Sky Science · de
Strukturelle und molekulare Grundlage der allosterischen Regulation und katalytischen Kopplung der humanen Phosphoribosylformylglycinamidin-Synthase
Warum dieses Enzym für die Gesundheit wichtig ist
Jede Zelle in Ihrem Körper ist auf Purine angewiesen, kleine Moleküle, die Reaktionen antreiben, Energie speichern und genetische Information tragen. Krebszellen, die sich rasch teilen, haben besonders hohen Bedarf an Purinen und verändern häufig die Art und Weise, wie diese hergestellt werden. Diese Studie konzentriert sich auf ein menschliches Enzym namens FGAMS, einen Schlüsselakteur beim de‑novo‑Aufbau von Purinen. Durch die Aufklärung der dreidimensionalen Struktur von FGAMS und der Bewegungen und Kommunikation seiner Teile zeigen die Autorinnen und Autoren, wie das Enzym ein‑ und ausgeschaltet wird und wie man es womöglich angreifen kann, um das Tumorwachstum zu bremsen.
Bausteine des Lebens unter Kontrolle
Zellen synthetisieren Purine über eine anspruchsvolle Produktionsstraße, den de‑novo‑Weg, der Energie verbraucht und mehrere Enzyme nutzt, um einen komplexen Ring aufzubauen. FGAMS katalysiert den vierten Schritt dieser Sequenz und steht im Zentrum eines größeren Enzymkomplexes, des sogenannten Purinosoms, das die Zutaten effizient weiterreicht. Da schnell wachsende Krebszellen diesen Weg oft hochfahren, sind Enzyme wie FGAMS attraktive Wirkstoffziele: Ihre Hemmung kann Tumoren der benötigten Nukleotide berauben, während gesunde Zellen auf Recyclingwege zurückgreifen können.
Eine formwandelnde molekulare Maschine
FGAMS besteht aus drei miteinander verbundenen Domänen, die jeweils eine andere Aufgabe erfüllen und in präziser Abfolge zusammenarbeiten müssen. Eine Domäne spaltet Ammoniak aus der Aminosäure Glutamin ab, eine andere verwendet dieses Ammoniak, um ein kleiners zuckerbasiertes Molekül zu modifizieren, und eine dritte Domäne fungiert als Regulationszentrum. Mithilfe hochauflösender Kryo‑Elektronenmikroskopie hielten die Forschenden FGAMS in drei unterschiedlichen Funktionszuständen fest: mit einem energiereichen Molekül gebunden, mit einem kurzlebigen Reaktionszwischenprodukt eingefangen und mit mehreren Substraten und Intermediaten gleichzeitig. Der Vergleich dieser Zustände zeigte, dass flexible Schleifen und ein N‑terminaler „Arm“ sich dramatisch bewegen und das Enzym während des Ablaufs der Chemie umgestalten.
Verborgener Tunnel und molekulare Tore
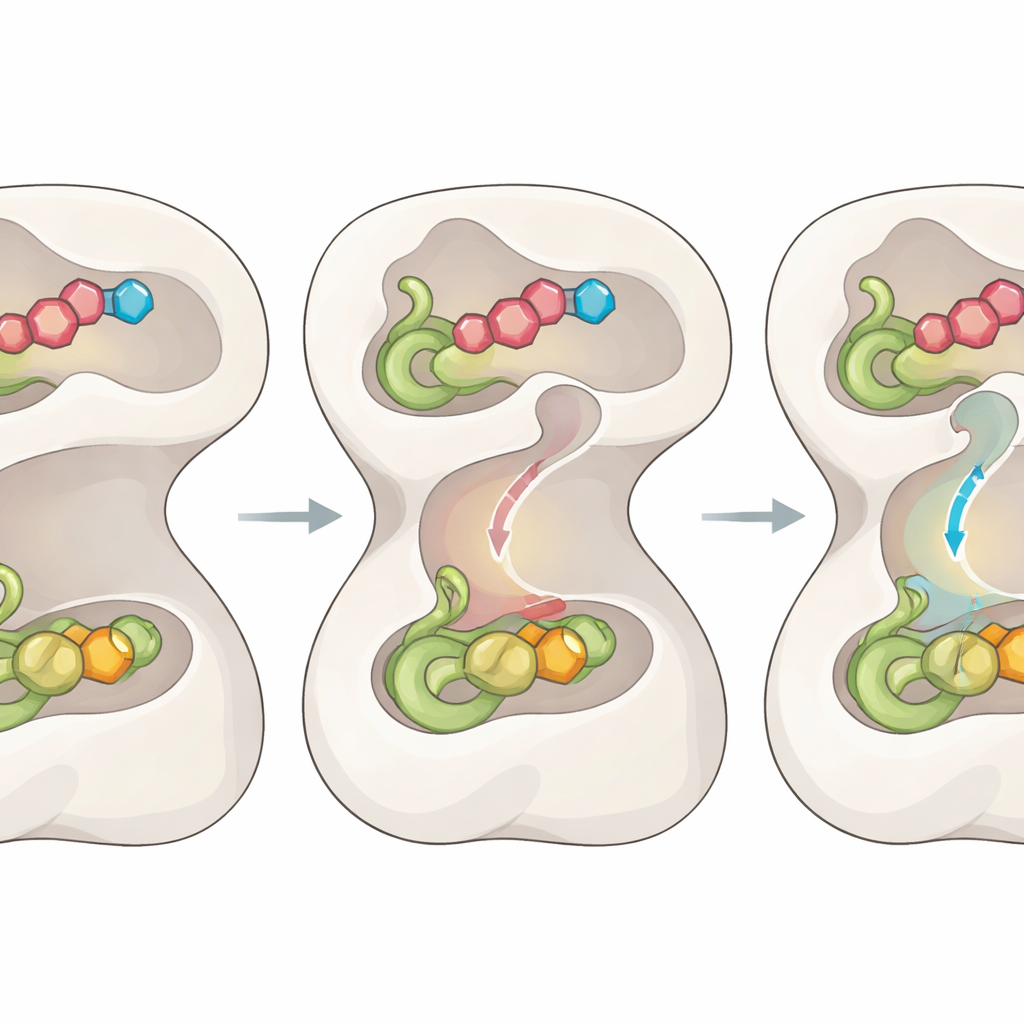
Ein zentrales Rätsel war, wie das in einer Domäne freigesetzte Ammoniak sicher zur entfernten Stelle gelangt, wo es gebraucht wird, ohne zu entweichen und Schaden anzurichten. Die neuen Strukturen legen einen bislang verborgenen internen Tunnel frei, der die beiden Stellen verbindet, sowie eine Reihe von „Toren“, die durch spezifische Aminosäuren gebildet werden. Wenn die richtigen Substrate binden und das Zwischenprodukt entsteht, klappt eine zentrale Schleife in eine geordnete Position, zieht an der N‑terminalen Domäne und reorganisiert benachbarte Schleifen in der katalytischen Domäne. Diese Choreografie öffnet zwei Eingangstore, sodass Glutamin verarbeitet werden kann, und formt vorübergehend eine Region um, die das energiereiche Zwischenprodukt stabilisiert, das für die Spaltung notwendig ist.
Kopplung der Chemie durch Bewegung
Während die Reaktion fortschreitet, verharrt das Enzym nicht passiv; es nutzt jeden chemischen Schritt als Signal. Sobald ein kovalentes Thioesterzwischenprodukt in der ammoniakproduzierenden Domäne gebildet ist, werden frühere Bewegungen teilweise wieder rückgängig gemacht. Das entspannt die zentrale Schleife und repositioniert die Tore, sodass Fluchtwege verschlossen werden, während an beiden Enden des Tunnels zwei zusätzliche Tore aufschwingen. Subtile Verschiebungen einiger weniger „Engpass“-Reste weiten den inneren Durchgang, wodurch ein Ammoniakmolekül direkt durch den Tunnel in das zweite aktive Zentrum gelangen kann, wo es mit dem eingefangenen Zwischenprodukt reagiert und das Endprodukt entsteht. Mutationen an den Torresten führen zum Austreten von Ammoniak oder zur Entkopplung der beiden Reaktionshälften und bestätigen, dass dieses Tor‑und‑Kanal‑System für effiziente Katalyse essenziell ist.
Von strukturellem Einblick zu therapeutischen Ansätzen
Indem die Studie FGAMS durch seinen katalytischen Zyklus verfolgt, liefert sie ein detailliertes Bild davon, wie Domänenbewegungen, flexible Schleifen, interne Tore und ein transitorischer Tunnel miteinander verkabelt sind, um die Chemie zu koordinieren. Für ein allgemeines Publikum lautet die Kernaussage: Das Enzym funktioniert wie eine winzige programmierbare Fabrik — es öffnet Türen und das innere Förderband nur, wenn alle richtigen Teile vorhanden sind, und sorgt so für Geschwindigkeit und Sicherheit. Da FGAMS die Purinproduktion in Krebszellen unterstützt und mit schlechterem Überleben bei Lebertumoren assoziiert ist, bieten die strukturellen Blaupausen und die neu identifizierten Kontrollpunkte mehrere Ansatzpunkte, um Wirkstoffe zu entwickeln, die den Tunnel blockieren, die Tore einfrieren oder wichtige Zwischenprodukte einklemmen — potenziell eine neue Klasse gezielter Krebsmedikamente.
Zitation: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Schlüsselwörter: Purinstoffwechsel, allosterische Regulation, Ammoniakkanalisierung, Krebsstoffwechsel, Cryo‑EM‑Struktur