Clear Sky Science · de
Negative Rückkopplungsregulierung der STING-Signalgebung durch TAX1BP1-gelenkte Golgiphagie
Wie Zellen eine Überreaktion des Immunsystems vermeiden
Unser Immunsystem muss einen schmalen Grat beschreiten: Es muss eindringende Viren und beschädigte DNA rasch erkennen, darf den Alarm aber nicht so lange laufen lassen, dass überschießende Entzündungen gesundes Gewebe schädigen. Diese Studie zeigt, wie ein wenig bekannter zellulärer Helfer, TAX1BP1, als eingebautes Bremssystem für einen starken Alarmweg namens cGAS–STING wirkt. Indem sie erklärt, wie Zellen diesen Alarm abbauen, nachdem er seine Aufgabe erfüllt hat, liefert die Arbeit Einblicke in Autoimmunerkrankungen, antivirale Abwehr und mögliche Krebstherapien.
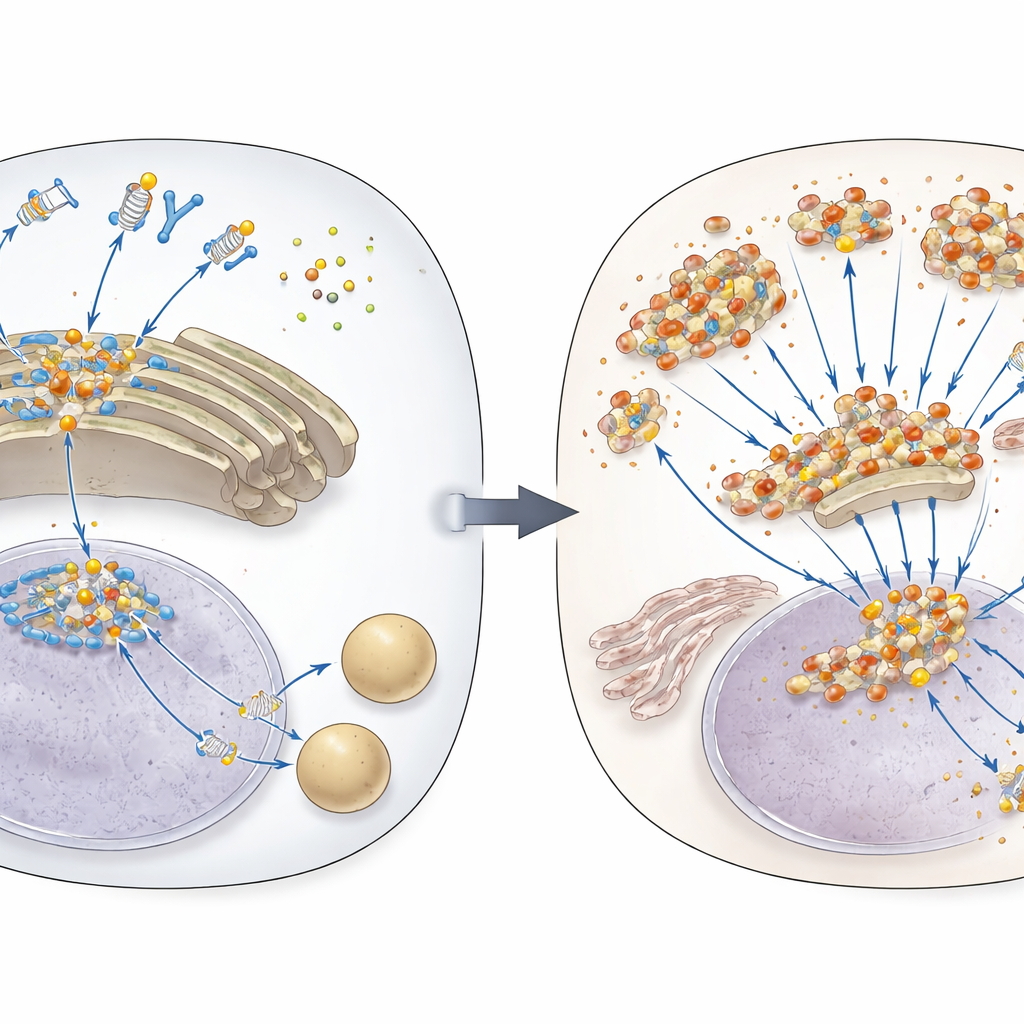
Das DNA-Alarmsystem der Zelle
Wenn fremde oder fehlplatzierte DNA in das Zellinnere gelangt, erkennt ein Sensorprotein namens cGAS diese und produziert ein kleines Botenmolekül. Dieses aktiviert STING, ein schalterähnliches Protein, das auf inneren Membranen sitzt. STING wandert dann zu einem zellulären Versandzentrum, dem Golgi, wo es sich zu Clustern zusammenlagert und die Produktion antiviraler Moleküle vom Typ I-Interferon sowie weiterer entzündlicher Signale auslöst. Weil diese Reaktion so stark ist, bauen Zellen STING nach einer kurzen Aktivitätsphase normalerweise wieder ab und führen es in zelluläre Recyclingzentren, die Lysosomen. Bislang war nur teilweise verstanden, wie STING für diesen Abschaltvorgang markiert wird.
Eine zelluläre Bremse mit vielen Aufgaben
TAX1BP1 war bisher als Multitasker bekannt, der dem zellulären Abfallentsorgungssystem, der Autophagie, hilft, unerwünschtes Material zu erkennen. Es kann sowohl an zum Abbau markierte Fracht als auch an die sich bildenden Bläschen binden, die diese Fracht aufnehmen. Die Autorinnen und Autoren fragten, ob TAX1BP1 auch den cGAS–STING-Alarm dämpfen könnte. An humanen immunähnlichen Zellen und Mausmakrophagen ohne TAX1BP1 stellten sie fest, dass die Aktivierung von cGAS oder STING weit höhere Interferon- und entzündliche Zytokinspiegel erzeugte als in normalen Zellen. Diese TAX1BP1-defizienten Zellen waren außerdem widerstandsfähiger gegen eine Infektion mit Herpes-simplex-Virus, was zu ihrer überstimulierten antiviralen Signalgebung passte.
Aufräumen von STING und einem gestressten Golgi
Tiefergehende Untersuchungen zeigten, dass STING ohne TAX1BP1 länger aktiv blieb und langsamer abgebaut wurde. Mikroskopie und biochemische Tests enthüllten, dass aktives STING große Aggregate bildet und dass diese Klumpen sich bei Fehlen von TAX1BP1 ansammeln. Gleichzeitig schwillt die Golgi-Struktur an und fragmentiert in Stücke. Das Team entdeckte, dass TAX1BP1 zusammen mit einem weiteren Recyclinghelfer, p62, diese beschädigten Golgi-Fragmente und die darauf befindlichen STING-Cluster zur Zerstörung in Lysosomen führt — eine spezialisierte Form der Bereinigung, die die Autorinnen und Autoren als „Golgiphagie“ bezeichnen. Dieser Prozess unterscheidet sich von der klassischen, großflächigen Autophagie und nutzt stattdessen selektivere Wege, um überlastete Golgi-Teile zu erfassen.
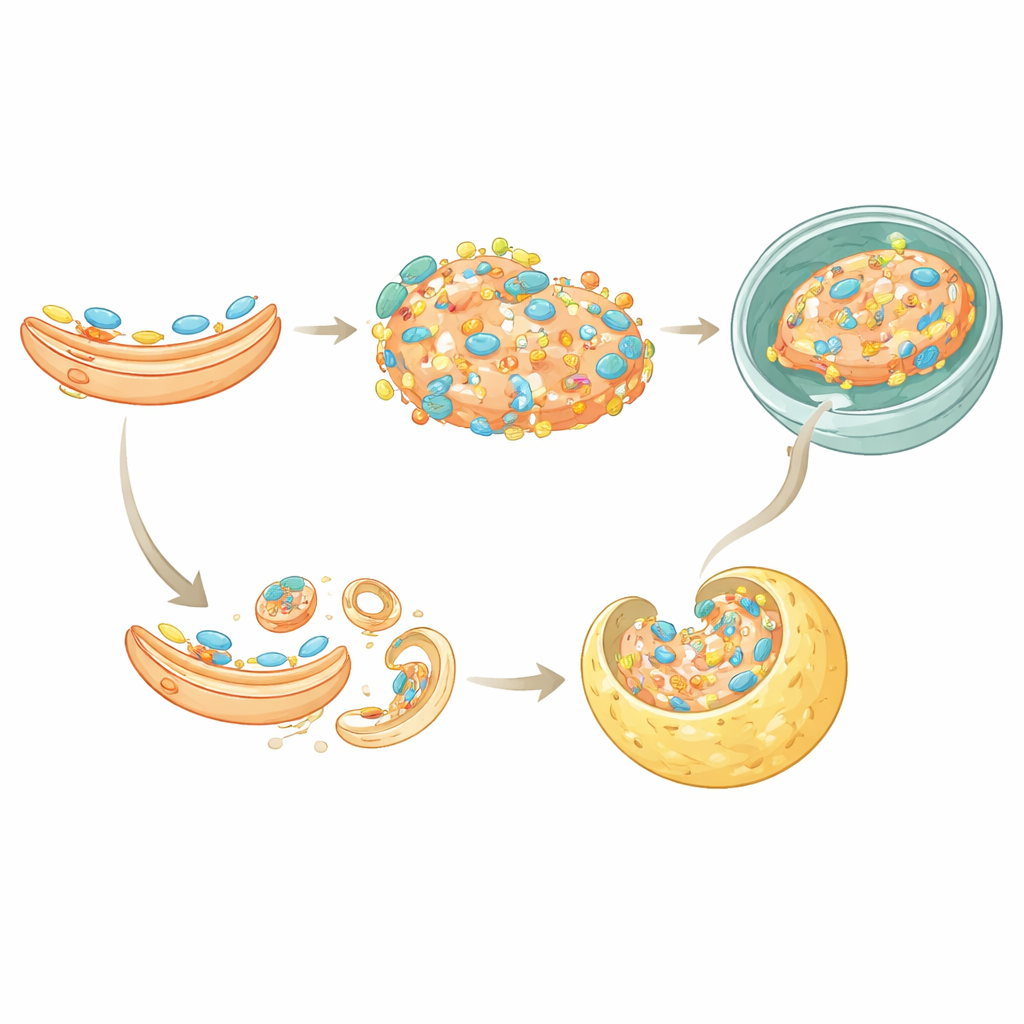
Zwei Wege, den Alarm abzuschalten
Die Studie enthüllte auch einen zweiten Weg, wie TAX1BP1 STING stilllegt. Normalerweise wird STING, nachdem es am Golgi signalisiert hat, in kleine Vesikel verpackt, die abschnüren und von einem Protein-Sortiersystem namens ESCRT erkannt werden, welches STING dann in Lysosomen liefert. TAX1BP1 bindet direkt an STING und erleichtert dessen Interaktion mit einer wichtigen ESCRT-Komponente, HGS. Wurde TAX1BP1 entfernt, war die Übergabe von STING an diese Sortiermaschinerie weniger effizient und sein Abbau verlangsamte sich. Dennoch trat ein gewisser Abbau weiterhin auf, was darauf hindeutet, dass TAX1BP1 zusammen mit p62 in dieser Mikroautophagie-Route arbeitet und Zellen damit teilweise redundante Wege zur Verfügung stellt, um zu gewährleisten, dass STING nicht zu lange verbleibt.
Warum das für Gesundheit und Krankheit wichtig ist
Um die Bedeutung dieser Bremse in lebenden Tieren zu prüfen, erzeugten die Forschenden Mäuse, denen TAX1BP1 gezielt in bestimmten Immunzellen fehlte. Wurden diese Mäuse mit einem STING-aktivierenden Wirkstoff stimuliert, zeigten sie höhere Interferon- und entzündliche Zytokinspiegel im Blut als normale Mäuse. Bei einer Infektion mit einem Pockenvirus trugen sie weniger Viruslast, was auf eine gesteigerte Resistenz hinweist. Zusammengenommen deuten diese Befunde darauf hin, dass TAX1BP1 den Moment der STING-Aktivierung am Golgi mit einer zeitlich gesteuerten Abschaltung koppelt, indem sowohl STING als auch beschädigte Golgi-Membranen gezielt zerstört werden. Für Laien lautet die Kernaussage: Zellen schlagen nicht nur Alarm, wenn sie gefährliche DNA entdecken, sie demontieren auch aktiv Teile ihrer internen Verkabelung, um sicherzustellen, dass der Alarm wieder ausgeht. Das Verständnis und gegebenenfalls das Einstellen dieser inneren Bremse könnte bei der Entwicklung von Therapien gegen chronische Entzündungserkrankungen, zur Verbesserung antiviraler Abwehr oder zur Modulation von Immunantworten bei Krebs hilfreich sein.
Zitation: Suklabaidya, S., Mohanty, S., Reider, I.E. et al. Negative feedback regulation of STING signaling by TAX1BP1-directed Golgiphagy. Nat Commun 17, 2762 (2026). https://doi.org/10.1038/s41467-026-69422-z
Schlüsselwörter: angeborene Immunität, STING-Signalweg, Autophagie, Golgi-Apparat, antivirale Antwort