Clear Sky Science · de
Granulom-Mikroumgebungsgeführte Sono-Immuntherapie zur Behandlung und Vorbeugung des Rückfalls von Tuberkulose
Warum dieser neue Tuberkulose-Ansatz wichtig ist
Tuberkulose infiziert noch immer ein Viertel der Weltbevölkerung und kann nach langen Antibiotikagaben zurückkehren. Diese Studie beschreibt eine gezielte „Schall plus Immun“-Therapie, die nicht nur darauf abzielt, Tuberkulose-Bakterien tief in der Lunge zu töten, sondern auch das Immunsystem so umzuschulen, dass die Krankheit deutlich seltener wiederkehrt. Sie kombiniert Erkenntnisse aus Patientenproben mit einem intelligenten Nanopartikel-Wirkstoff, der durch medizinischen Ultraschall aktiviert wird.
Das verborgene Schlachtfeld in Lungenknoten
Wenn Tuberkulose-Erreger eindringen, kapseln sich Immunzellen in der Lungenwand zu dichten Gewebsballungen ab, den sogenannten Granulomen. Diese Strukturen sollen die Bakterien einsperren, schaffen aber zugleich eine geschützte Nische, in der die Mikroben unbemerkt überdauern und Antibiotika ausweichen können. Durch die Reanalyse von Einzelzell-RNA-Sequenzierungsdaten aus menschlichem Lungengewebe verglichen die Forscher gewöhnliche nicht-tuberkulöse Granulome mit echten tuberkulösen Granulomen und mit gesundem Lungengewebe. Sie fanden, dass in tuberkulösen Läsionen wichtige „Ersthelfer“-Zellen — Makrophagen und dendritische Zellen — in einen gedämpften Zustand übergegangen waren. Molekulare Signalwege, die normalerweise Bakterien erkennen und Alarm auslösen, waren herunterreguliert, während Gene, die die Immunaktivität dämpfen, hochreguliert waren.
Wenn das Immunsystem auf die Bremse tritt
Das Team betrachtete dann Blutproben von Menschen mit medikamentenresistenter versus medikamentenempfindlicher Tuberkulose und von Patienten, deren Erkrankung entweder erneut auftrat oder geheilt blieb. In allen Gruppen zeigte sich dasselbe Muster: Gene und Signalwege, die die Immunantwort negativ regulieren, waren bei Patienten mit Medikamentenresistenz und Rückfall stärker aktiv. Signale, die Immunzellen helfen sollten, Bakterien zu erkennen und zu beseitigen, waren schwächer. Das deutet darauf hin, dass ein Therapieversagen nicht nur an den Arzneimitteln oder den Bakterien liegt, sondern auch an einer Immunumgebung, die in einen übermäßig gehemmteten, „toleranten“ Modus gedrängt wurde — besonders innerhalb der Granulome.
Entwicklung eines schallaktivierten Helferpartikels
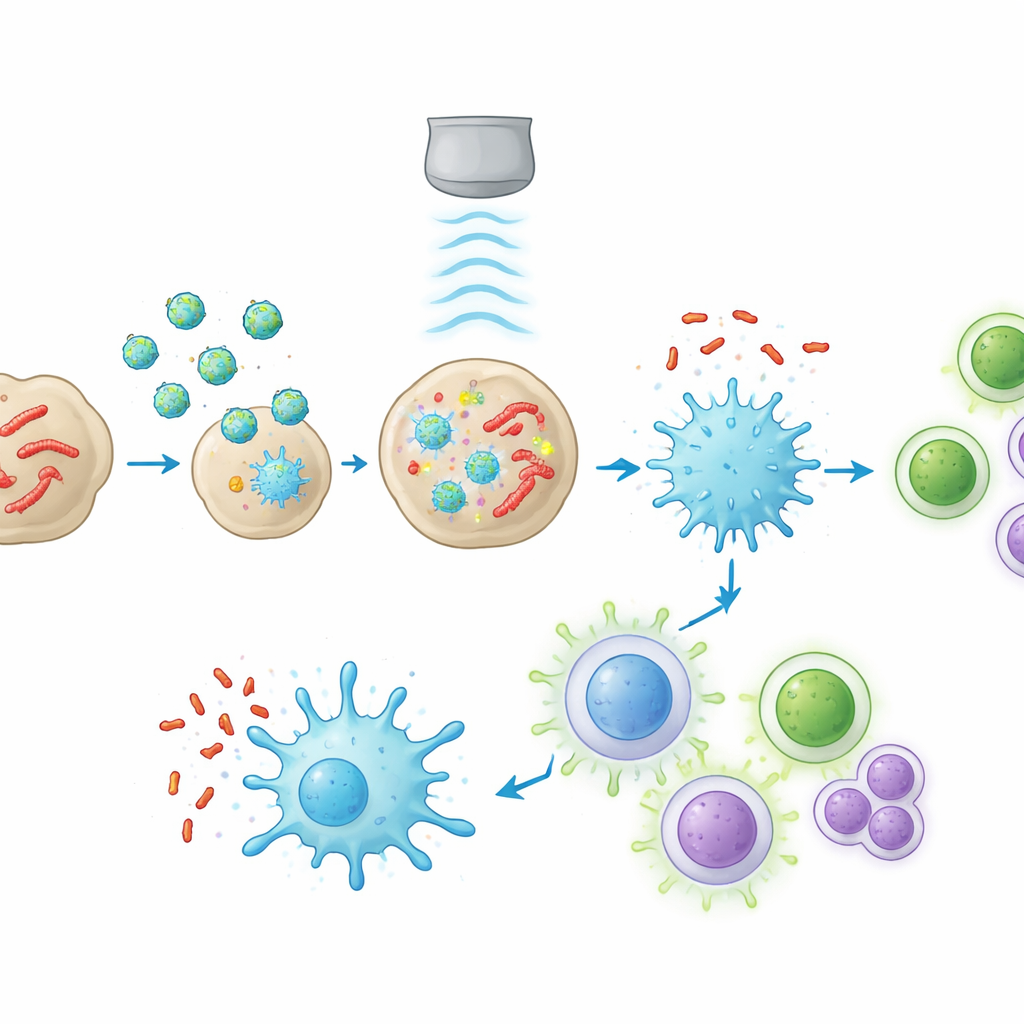
Angeleitet von diesem Bild der Immunparalyse konstruierten die Forscher einen Nanopartikel namens manSNI. Er besteht aus einem organischen halbleitenden Polymer, das bei Ultraschalleinwirkung Schübe reaktiver Sauerstoffspezies (ROS) erzeugen kann, einer Mannose-Beschichtung, die die Anreicherung in Makrophagen begünstigt, und einem kleinen immunaktivierenden Molekül, das einen Toll-like-Rezeptor auf diesen Zellen stimuliert. In Reagenzgläsern lagerten sich manSNI-Partikel in den Lysosomen infizierter Makrophagen an und erzeugten unter Ultraschall genug ROS, um mehr als 99 % der Tuberkulose-Modellbakterien zu zerstören, selbst wenn der Ultraschall mehrere Zentimeter Gewebe durchdringen musste. Die ROS rissen außerdem bakterielle Membranen auf und setzten bakterielle Proteine frei, die als Antigene wirken können.
Ein kaltes Granulom in ein heißes Immunzentrum verwandeln
Bei Mäusen mit tuberkuloseähnlicher Lungenerkrankung reicherte sich manSNI deutlich besser in Granulomen an als ähnliche Partikel ohne Mannose-Zielgruppe. Wurden die Lungen kurz Ultraschall ausgesetzt, sanken die Bakterienzahlen in der Lunge nahezu auf null. Gleichzeitig veränderte sich die lokale Immunlandschaft. Makrophagen verschoben sich in einen proinflammatorischen, bakterienbekämpfenden Zustand; dendritische Zellen reiften und transportierten Antigeninformationen in nahegelegene Lymphknoten; und tuberkulose-spezifische T-Zellen sowie antikörperproduzierende B-Zellen vermehrten sich. Die Genexpressionsanalyse des Lungengewebes zeigte, dass mehrere Schlüsselpfade der Erkennung und Abwehr, die zuvor in menschlichen Granulomen unterdrückt waren, nun stark reaktiviert wurden.
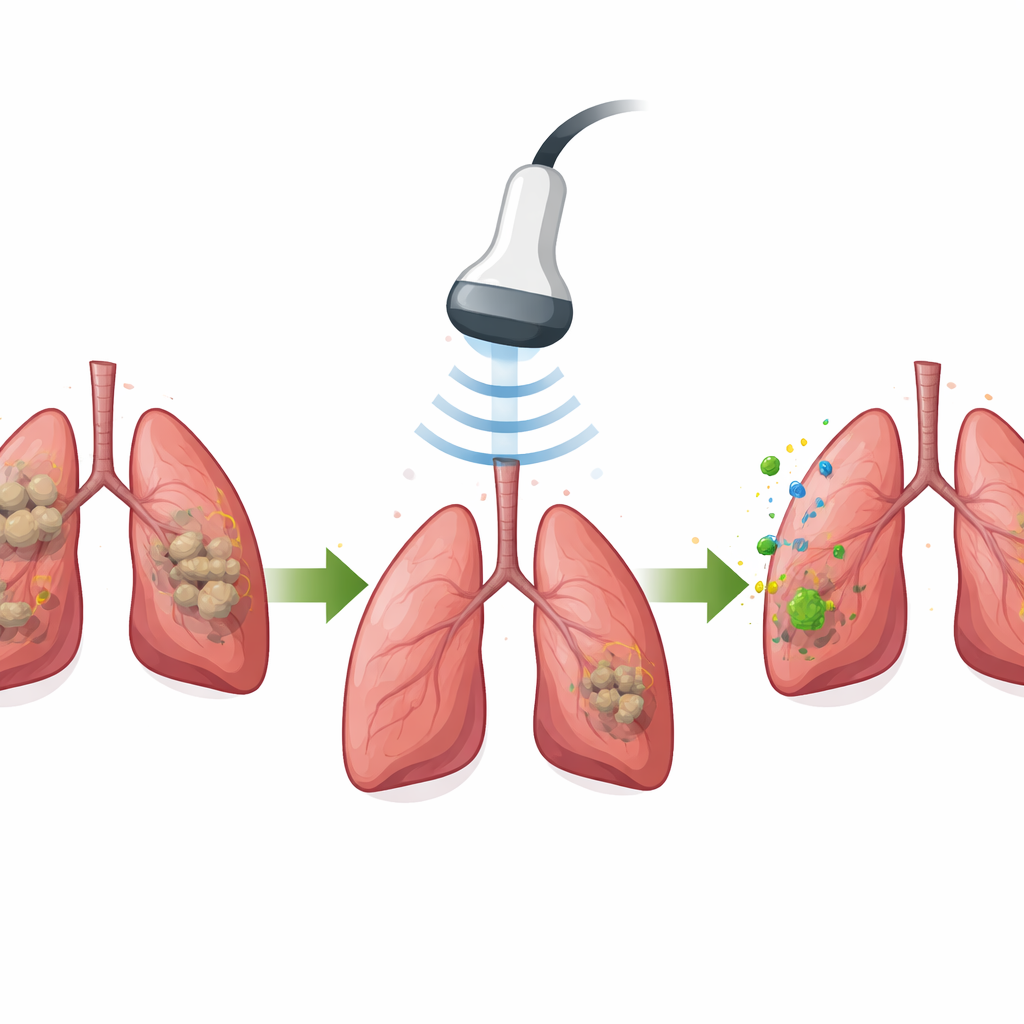
Langfristigen Schutz gegen Rückfall und Reinfection aufbauen
Das Eliminieren der Erstinfektion ist nur ein Teil der Herausforderung; viele Patienten erleiden Tuberkulose erneut, sei es durch verbliebene Bakterien oder durch neue Exposition. In Langzeitstudien an Mäusen verglichen die Autoren ein Standardantibiotikum (Rifampicin) mit manSNI plus Ultraschall. Beide Behandlungsschemata eliminierten zunächst nachweisbare Bakterien, doch nach alleinigen Antibiotika waren Rückfälle häufig, während sie nach Sono-Immuntherapie selten waren. Tiere, die manSNI erhielten, entwickelten höhere Anteile an gewebsansässigen Gedächtnis-T-Zellen in der Lunge, zentrale und Effektormemory-T-Zellen in lymphatischen Organen sowie langlebige Gedächtnis-B-Zellen und Antikörper im Blut. Wurden diese Mäuse gezielt erneut den Tuberkulose-Modellbakterien ausgesetzt, widerstanden die meisten einer Neuinfektion oder zeigten nur milde, vorübergehende Läsionen.
Was das für die künftige Tuberkuloseversorgung bedeuten könnte
Für Nicht-Fachleute ist die Kernbotschaft, dass diese Arbeit eine zweigleisige Strategie bietet: Bakterien direkt in schwer erreichbaren Lungenknoten zerstören und gleichzeitig die lokale Immunumgebung von „aus“ auf „an“ zurücksetzen. Der Ansatz nutzt Ultraschall — bereits in Kliniken gebräuchlich —, um nichtinvasiv einen präzise zielgerichteten Nanopartikel zu aktivieren, der sowohl Keime tötet als auch wie ein eingebauter Impfverstärker wirkt. Obwohl die Experimente an Mäusen und mit ungefährlicheren Modellstämmen statt mit den gefährlichsten Tuberkuloseerregern durchgeführt wurden, deuten die Ergebnisse auf einen Weg zu kürzeren, wirksameren Therapien hin, die nicht nur Tuberkulose heilen, sondern auch die Wahrscheinlichkeit ihres Wiederauftretens deutlich reduzieren.
Zitation: Wang, W., Li, F., Mo, W. et al. Granulomas microenvironment-guided sono-immunotherapy to treat and prevent recurrence of tuberculosis. Nat Commun 17, 2595 (2026). https://doi.org/10.1038/s41467-026-69420-1
Schlüsselwörter: Tuberkulose, Sono-Immuntherapie, Nanopartikel, Granulome, Ultraschalltherapie