Clear Sky Science · de
Molekularer Wirkmechanismus des kleinen Moleküls SMT-738 auf den bakteriellen Lipoprotein-Transporter LolCDE
Warum dieses neue Antibiotikum wichtig ist
Da immer mehr Krankenhausinfektionen unseren besten Antibiotika trotzen, brauchen Ärztinnen und Ärzte dringend Wirkstoffe, die gefährliche Bakterien abtöten, ohne die nützlichen Mikroben, die wir mit uns tragen, zu zerstören. Diese Studie legt dar, wie eine vielversprechende experimentelle Verbindung namens SMT-738 eine entscheidende Transportmaschine in der äußeren Hülle bestimmter schwer zu behandelnder Bakterien lahmlegt. Indem sie genau zeigt, wo und wie dieses Mittel die Maschinerie blockiert, weist die Arbeit den Weg zu gezielteren Antibiotika, die Superkeime treffen und gleichzeitig einen Großteil des Darmmikrobioms schonen.
Die äußere Rüstung schlechter Bakterien
Viele der beunruhigendsten Krankenhauskeime gehören zu den sogenannten gramnegativen Bakterien. Sie sind schwer zu töten, weil sie sich in einer doppellagigen äußeren Hülle verpacken. Diese Außenhaut wird von mehreren molekularen Maschinen aufgebaut und erhalten, die entscheidende Bausteine von der inneren Membran, wo sie synthetisiert werden, an die Oberfläche transportieren. Zu den wichtigen Ladungen gehören Lipoproteine, die die äußere Hülle stabilisieren und Prozesse wie Nährstoffaufnahme und Antibiotikaresistenz unterstützen. Ein Transportsystem, der Lol-Weg, und speziell eine Pumpe namens LolCDE extrahiert Lipoproteine aus der inneren Membran und übergibt sie an Chaperone, die sie zur äußeren Oberfläche bringen. Da diese Schritte essentiell sind, stellen sie attraktive Ziele für neue Antibiotika dar.
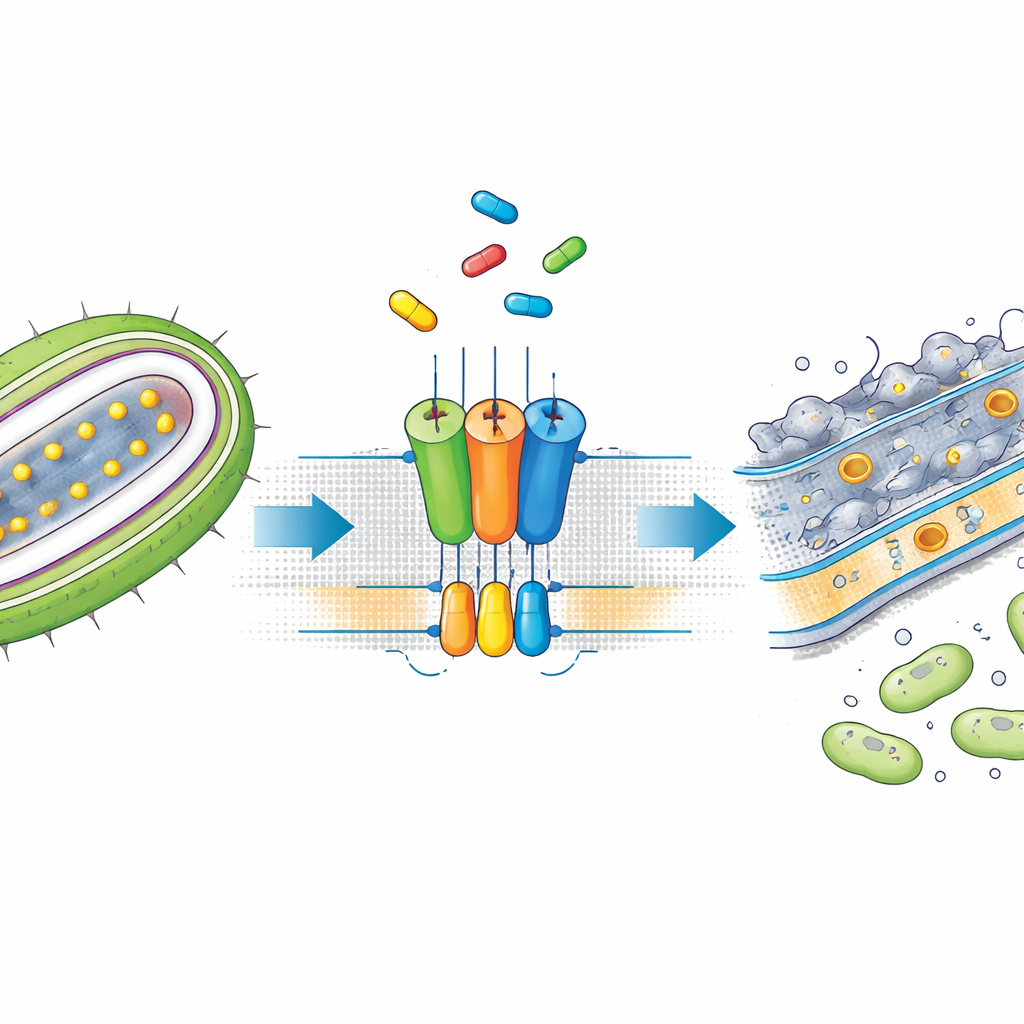
Ein kleines Molekül, das das Förderband stoppt
SMT-738 tauchte in früheren Screens als potenter Hemmstoff gegen gramnegative Krankheitserreger der Familie Enterobacteriaceae auf, darunter multiresistente Stämme von Escherichia coli und Klebsiella pneumoniae. Sein genauer Wirkmechanismus war jedoch unklar. Die Autoren zeigten zunächst, dass SMT-738 verhindert, dass ein Test-Lipoprotein von LolCDE in gentechnisch veränderten Bakterien freigesetzt wird, was bestätigt, dass das Mittel tatsächlich den Transportschritt stoppt. Wichtig ist, dass Bakterien mit bestimmten Mutationen in den Genen des LolCDE-Komplexes gegenüber SMT-738 resistent wurden, was darauf hindeutet, dass das Medikament direkt an diese Pumpe bindet. Diese Beobachtungen bereiteten den Weg für einen strukturellen Tiefenblick darauf, wie die Verbindung mit dem Transporter interagiert.
Die Pumpe von innen verklemmen
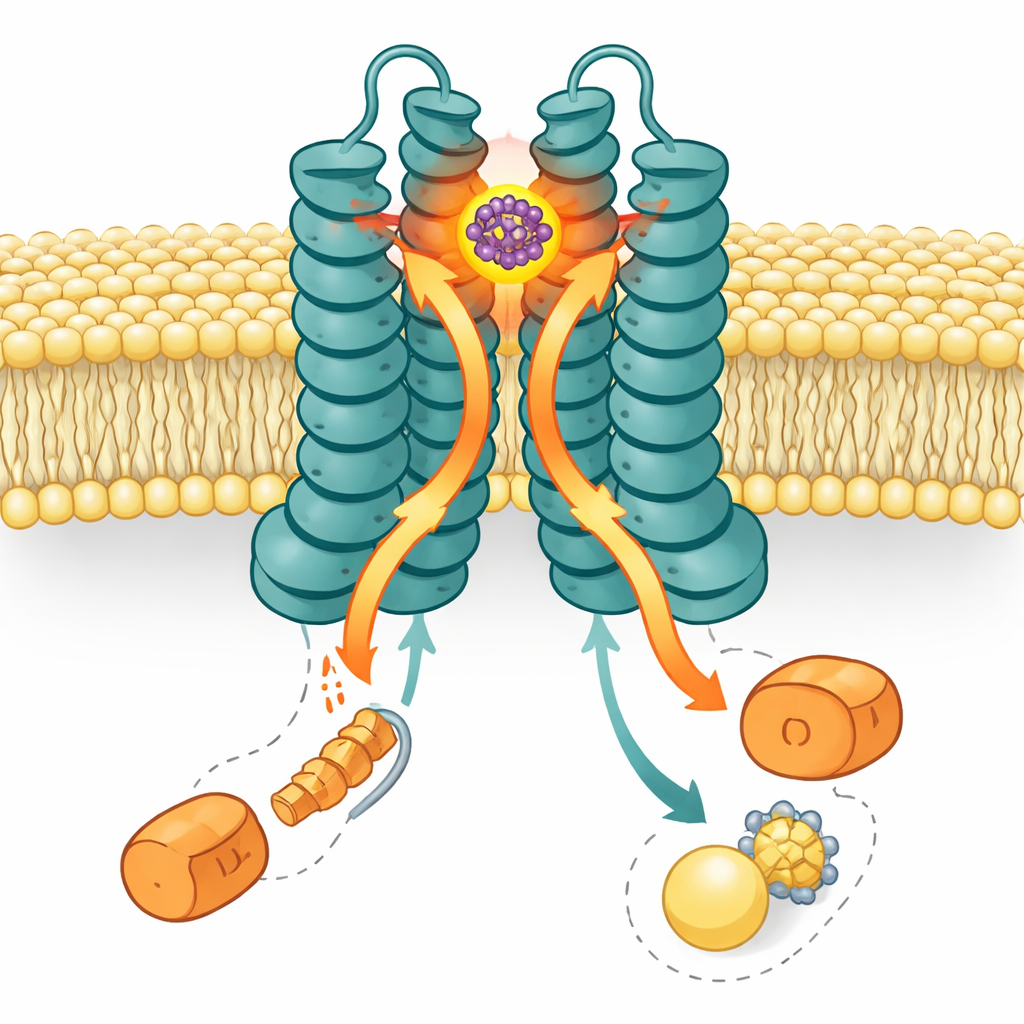
Mithilfe hochaufgelöster Kryo-Elektronenmikroskopie erstellten die Forschenden ein dreidimensionales Bild von LolCDE mit eingeklemmtem SMT-738. Die Struktur zeigt das Medikament keilförmig in einer Tasche am periplasmatischen Ende—der Seite, die dem Raum zwischen innerer und äußerer Membran zugewandt ist—zwischen zwei Kernuntereinheiten, LolC und LolE. Dieser Ort überlappt den normalen Andockbereich für Lipoprotein-Fracht. Wenn SMT-738 diese Tasche besetzt, verschieben sich umliegende Aminosäuren in LolC und LolE um bis zu etwa einem Nanometer. Diese Bewegungen erzeugen sterische Kollisionen mit der Position, die Lipoprotein und seine Fettschwänze normalerweise einnehmen würden, und blockieren so effektiv das Eindringen der Fracht in die Pumpe. Mutationen vieler dieser taschenbildenden Reste schwächten entweder die Wirkstoffbindung oder machten die Bakterien resistent, was gut zum strukturellen Befund passt.
Auslösen eines einseitigen Zusammenbruchs
Die Geschichte endet nicht an der Bindungsstelle. LolCDE wird von zwei Kopien einer Motoruntereinheit namens LolD angetrieben, die auf der zytoplasmatischen Seite sitzen und ATP verbrennen, um den Transport zu liefern. Auffällig ist, dass in der SMT-738-gebundenen Struktur nur ein LolD verbleibt; der Partner-LolD hat sich gelöst. Biochemische Gele und ATPase-Assays bestätigten, dass die Bindung von SMT-738 zum Verlust eines LolD führt und die energieumsetzende Aktivität der Pumpe stark verringert. Computersimulationen des Transporters in einer Membran untermauerten dieses Bild: Während SMT-738 in seine Tasche einsank, breiteten sich Konformationsänderungen nach unten aus und schoben die Kopplungshelix, die LolC und LolE mit LolD verbindet. Diese Verschiebungen drängten das an LolC gebundene LolD in eine ungünstige Kollision, wodurch es sich löste, während das an LolE gebundene LolD erhalten blieb. Das Ergebnis ist eine asymmetrische, „verriegelte“ Maschine, die Lipoproteine nicht mehr transportieren kann.
Warum einige Bakterien getroffen werden und andere verschont bleiben
SMT-738 besitzt eine wünschenswerte Eigenschaft: Es greift resistente Enterobacteriaceae stark an, lässt jedoch viele andere gramnegative Arten im Darm weitgehend unberührt. Um diese Selektivität zu verstehen, verglichen die Forschenden Sequenzen von LolE aus empfindlichen und resistenten Bakterien und konzentrierten sich auf Positionen, die SMT-738 kontaktieren. Zwei Reste in LolE, insbesondere einer, der der Position D264 in E. coli entspricht, fielen auf. In empfindlichen Erregern stimmten diese Positionen mit der wirkstoffkontaktierenden Version in E. coli überein, während sie in vielen resistenten Darmkommensalen durch andere Aminosäuren ersetzt waren. Als die Forschenden E. coli so veränderten, dass sie diese Substitutionen trugen, wurden die Bakterien hochresistent gegen SMT-738, zeigten jedoch weiterhin LolCDE-Expression. Simulationen deuteten darauf hin, dass diese Veränderungen die lokale Flexibilität rund um die Tasche verändern und die Fähigkeit von SMT-738 zu binden verringern. Interessanterweise stützte sich ein anderer LolCDE-Inhibitor, Lolamicin, auf nur teilweise überlappende Kontaktpunkte und zeigte ein anderes Resistenzmuster, was auf unterschiedliche Möglichkeiten hinweist, dieselbe Pumpe anzugreifen.
Neue Blaupausen für künftige Antibiotika
Durch die Kombination struktureller Abbildungen, Mutationsanalysen, biochemischer Tests und Computersimulationen zeigt diese Arbeit, dass SMT-738 nicht bloß ein Stöpsel in einem Kanal ist. Stattdessen heftet es sich an die periplasmatische Seite der LolCDE-Pumpe, blockiert die Eintrittsöffnung für Lipoproteine und löst dann langreichweitige Verschiebungen aus, die eine der beiden Motor-Einheiten abwerfen und den Transporter in einen nicht funktionierenden Zustand einfrieren. Dieser „allosterische Stillstand“-Mechanismus stellt eine neue Möglichkeit dar, eine bakterielle Maschine lahmzulegen, und erklärt, warum SMT-738 gefährliche Erreger gezielt angreifen kann, während ein Großteil des Mikrobioms verschont bleibt. Die detaillierte Karte der Bindungstasche und die identifizierte Selektivitätsposition in LolE bieten nun eine rationale Grundlage für das Design der nächsten Antibiotika-Generation, die dieselbe Verwundbarkeit mit noch größerer Potenz und Präzision ausnutzen könnte.
Zitation: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Schlüsselwörter: Antibiotikaresistenz, Gramnegative Bakterien, Lipoprotein-Transport, LolCDE-Inhibitor, cryo-EM-Struktur