Clear Sky Science · de
Krebszell-intrinsisches Inflammasom-Protein ASC verbindet angeborene Immunität mit mitochondrialem Stoffwechsel und treibt Bauchspeicheldrüsenkrebs an
Warum diese Forschung wichtig ist
Bauchspeicheldrüsenkrebs zählt zu den tödlichsten Krebsarten und wird häufig zu spät entdeckt, als dass effektive Behandlungen möglich wären. Diese Studie deckt eine verborgene „Verschaltung“ in Tumorzellen der Bauchspeicheldrüse auf, die die ersten Abwehrmechanismen des Immunsystems mit der Energiegewinnung und -nutzung der Zellen verbindet. Indem sie zeigt, dass ein einzelnes Immunadaptorprotein namens ASC das Tumorwachstum fördert, indem es den Zellstoffwechsel umprogrammiert, weist die Arbeit auf ein neues, sehr spezifisches Ziel für künftige Therapien in einer Krebsform hin, die dringend bessere Optionen benötigt. 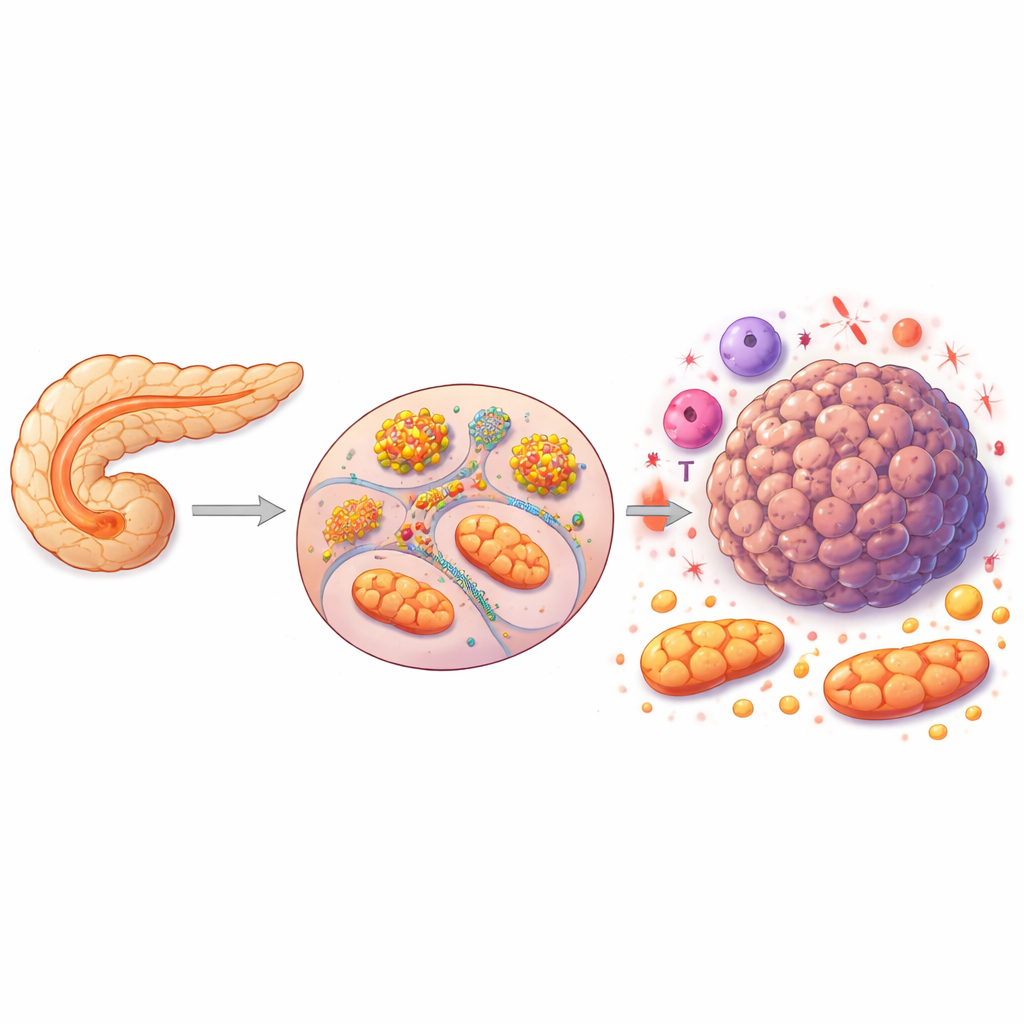
Eine tödliche Krebsform mit wenigen guten Optionen
Die meisten Bauchspeicheldrüsenkarzinome gehören zum Typ des duktalen Adenokarzinoms, das aus Zellen entsteht, die die kleinen Kanälchen der Bauchspeicheldrüse auskleiden. Diese Tumoren sind bei Entdeckung meist schon weit fortgeschritten, und die derzeitigen Chemo- und Immuntherapien bringen nur begrenzte Vorteile. Es ist bekannt, dass chronische Entzündung und eine immunsuppressive Tumorumgebung das Wachstum von Bauchspeicheldrüsenkrebs fördern, doch welche Moleküle die gestörte Immunität mit dem Tumorverhalten verbinden, blieb weitgehend unklar. Solche Moleküle zu identifizieren, könnte Behandlungen ermöglichen, die die Krankheit bremsen, indem sie entscheidende „Versorgungsleitungen“ innerhalb des Krebses unterbrechen.
Ein Immunadaptor, versteckt in Tumorzellen
Die Autoren konzentrierten sich auf ASC, ein Gerüstprotein, das normalerweise beim Zusammenbauen von Inflammasomen hilft—molekularen Maschinen, die Gefahr signalisieren und Entzündungsreaktionen aktivieren. Anhand mehrerer Patientendatensätze fanden sie, dass das Gen, das ASC kodiert (PYCARD), in Bauchspeicheldrüsen-Tumoren im Vergleich zum gesunden Pankreas durchgängig erhöht ist, über verschiedene molekulare Subtypen der Erkrankung hinweg. Hohe ASC-Spiegel sowie hohe Werte seines Partnerenzyms Caspase-1 und des Zytokins IL-18 korrelierten mit einer schlechteren Patient:innen-Prognose. Mittels fortgeschrittener Färbetechniken an Tumorbiopsien zeigte das Team, dass ASC und aktiviertes Caspase-1 hauptsächlich in den krebsartigen Gangzellen selbst zu finden sind und dort helle punktartige „Specks“ sowohl innerhalb der Zellen als auch im umliegenden Gewebe bilden—ein Hinweis auf aktive Inflammasom-Komplexe. 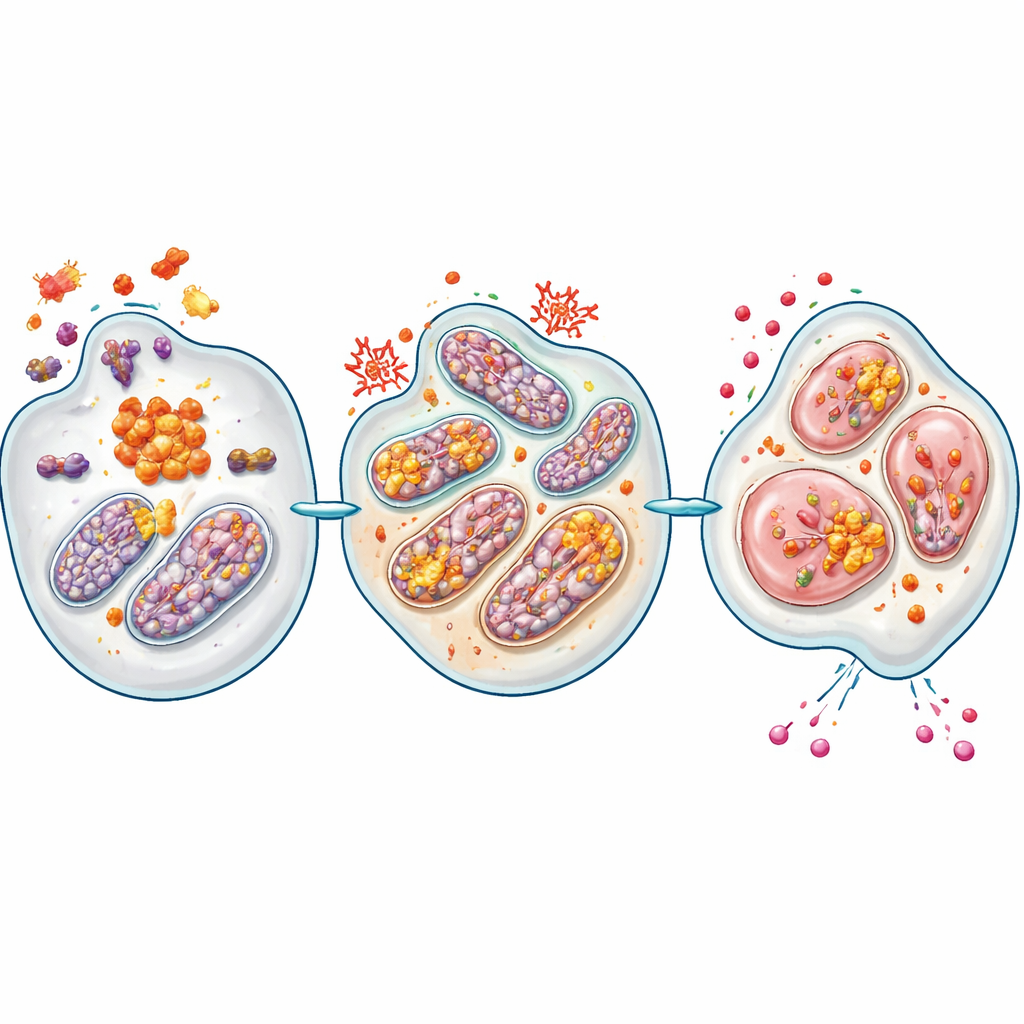
Das Abschalten von ASC verlangsamt das Tumorwachstum
Um zu prüfen, ob ASC tatsächlich zur Entstehung von Bauchspeicheldrüsenkrebs beiträgt und nicht nur dessen Begleiter ist, verwendeten die Forschenden ein etabliertes Mausmodell, das von mutierten Kras- und Trp53-Genen angetrieben wird und die menschliche Erkrankung gut nachbildet. In diesen Mäusen waren ASC, Caspase-1 und IL-18 im Pankreas erhöht, und zirkulierendes IL-18 nahm mit dem Fortschreiten der Läsionen zu. Wurde ASC im ganzen Körper entfernt, bildeten die Mäuse deutlich kleinere Pankreas aus, wiesen viel weniger und weniger aggressive Tumoren auf und zeigten keine Lebermetastasen. Die selektive Entfernung von ASC nur im duktalen Pankreasepithel erzeugte einen starken, wenn auch etwas abgeschwächten Schutzeffekt, was unterstreicht, dass ASC in Tumorzellen ein wesentlicher Treiber ist. Wichtig ist, dass das Blockieren der extrazellulären „Specks“ von ASC mit einem spezialisierten Nanobody-Medikament ebenfalls die Tumorlast und die Zellproliferation verringerte—ein Hinweis darauf, dass ASC sowohl innerhalb als auch außerhalb von Zellen krankheitsfördernd wirkt.
Umschaltung der Kraftwerke der Krebszelle
Vertiefende Analysen mittels ganzheitlichem Transkriptomprofiling verglichen die Genaktivität in normalem, tumortragendem und ASC-defizientem Pankreas. In tumortragenden Mäusen waren Gene, die mit Immunaktivierung verbunden sind, hochreguliert, während solche, die an mitochondrialer Atmung und oxidativer Phosphorylierung—dem zentralen energieproduzierenden Weg der Zelle—beteiligt sind, heruntergefahren waren. Der Verlust von ASC kehrte dieses Muster weitgehend um. Biochemische Tests bestätigten, dass zentrale Proteine der mitochondrialen Atmungskette in Tumoren reduziert, aber bei Fehlen von ASC wiederhergestellt waren. Tumortragende Mäuse hatten weniger Kopien mitochondrialer DNA, mehr oxidative Schäden und höhere Laktatwerte—alles Kennzeichen einer Verlagerung von sauerstoffbasierter Energiegewinnung hin zu einer „Warburg-ähnlichen“ aeroben Glykolyse. Das Entfernen von ASC erhöhte die Kopienzahl der mitochondrialen DNA und senkte sowohl oxidativen Stress als auch Laktatproduktion.
Von Mausmodellen zu menschlichen Krebszellen
Um zu prüfen, ob diese Befunde direkt auf menschliche Tumoren übertragbar sind, verringerten die Autoren ASC-Spiegel in zwei menschlichen Bauchspeicheldrüsenkrebs-Zelllinien mittels kleiner interferierender RNA. Zellen mit reduziertem ASC zeigten geringere Caspase-1-Aktivierung, wuchsen langsamer, bildeten weniger Kolonien und produzierten weniger Laktat und mitochondriales Superoxid. Ihre mitochondrialen Gene und die Kopienzahl der mitochondrialen DNA erholten sich, und ihr Sauerstoffverbrauch sowie die Reserveatmungskapazität stiegen—ein Hinweis auf eine Rückkehr zu gesünderer mitochondrialer Atmung. Bemerkenswerterweise wurden diese ASC-defizienten Zellen weniger empfindlich gegenüber Wirkstoffen, die die Glykolyse blockieren, was mit einer verringerten Abhängigkeit von diesem krebsfördernden Energiestoffwechsel übereinstimmt. Zusammengenommen zeigen diese Ergebnisse, dass ASC aktiv Bauchspeicheldrüsenzellen in einen Zustand mit hoher Glykolyse und erhöhtem oxidativem Stress lenkt, der schnelles Wachstum unterstützt.
Was das für zukünftige Behandlungen bedeutet
Die Studie identifiziert ASC als zentrale „Brücke“ zwischen angeborener Immunität, chronischer Entzündung und dem fehlgesteuerten Energiestoffwechsel, der Bauchspeicheldrüsenkrebs antreibt. Statt nur in klassischen Immunzellen zu wirken, hilft ASC innerhalb duktaler Tumorzellen beim Zusammenbau von Inflammasomen, fördert die Produktion von IL-18, stört die mitochondriale Biogenese und treibt Zellen in Richtung Glykolyse und aggressiven Wachstums. In Mäusen verlangsamt das genetische Entfernen von ASC oder die Neutralisierung seiner extrazellulären Specks den Krankheitsverlauf, was nahelegt, dass Wirkstoffe, die ASC oder seine Inflammasom-Komplexe angreifen, bestehende Therapien ergänzen könnten. Zwar bleiben Fragen offen—etwa welche upstream Sensoren ASC in diesem Krebs aktivieren und wie IL-18 sicher blockiert werden kann—doch die Arbeit liefert eine überzeugende Begründung, ASC als neues, mechanistisch begründetes Therapieziel beim duktalen Adenokarzinom der Bauchspeicheldrüse zu verfolgen.
Zitation: Chey, Y.C.J., Kashgari, B., McLeod, L. et al. Cancer cell-intrinsic inflammasome protein ASC links innate immunity with mitochondrial metabolism in driving pancreatic cancer. Nat Commun 17, 2477 (2026). https://doi.org/10.1038/s41467-026-69398-w
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Inflammasom, mitochondrialer Stoffwechsel, IL-18, Krebsimmunologie