Clear Sky Science · de
Laktat aus Makrophagen treibt die phänotypische Umprogrammierung dermaler Hautfibroblasten über MCT1-vermittelte Histon H3 Lysin 23 Laktylierung bei hypertrophen Narben
Warum manche Narben dick und erhöht werden
Die meisten Schnitte und Verbrennungen heilen schließlich zu dünnen, flachen Narben ab. Manche Wunden jedoch verheilen mit dicken, erhöhten Gewebebändern, sogenannten hypertrophen Narben, die jucken, schmerzen und die Beweglichkeit einschränken können. Diese Studie entdeckt einen unerwarteten Treiber dieser hartnäckigen Narben: ein verbreitetes Stoffwechselzwischenprodukt namens Laktat, das von Immunzellen in steifer, heilender Haut produziert wird und benachbarte Reparaturzellen so umprogrammiert, dass sie ein aggressiveres, narbenbildendes Verhalten zeigen.
Von normaler Reparatur zur problematischen Narbe
Bei gesunder Wundheilung arbeiten Hautzellen zusammen, um die Verletzung zu verschließen und das Gewebe wieder aufzubauen. Fibroblasten, die wichtigsten Reparaturzellen in der tiefen Hautschicht, wechseln vorübergehend in einen aktivierten Zustand, in dem sie vermehrt Kollagen produzieren, das Proteingerüst der Haut. Sobald die Wunde verschlossen ist, beruhigen sich diese Zellen wieder. Bei hypertrophen Narben hingegen bleiben Fibroblasten in diesem überaktiven Zustand und lagern zu viel Kollagen in dicken, ungeordneten Bündeln ein. Die Autor:innen begannen damit, normale Haut mit hypertropher Narbe zu vergleichen und fanden eine klare Stoffwechselverschiebung: das Narbenmilieu begünstigte eine schnelle, zuckerabbauende Chemie, die große Mengen Laktat erzeugt, sowie hohe Mengen eines Transportproteins namens MCT1, das Laktat in Zellen transportiert. 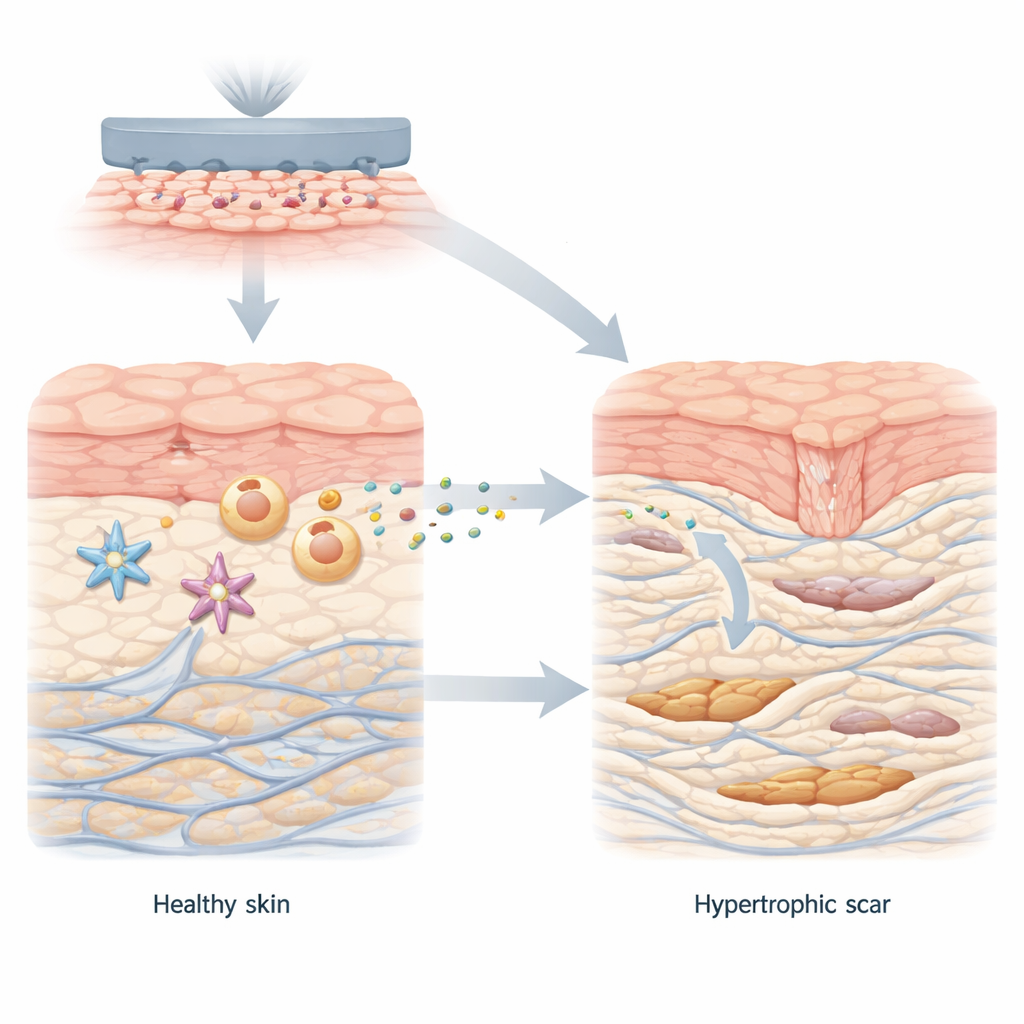
Immunzellen als unerwartete Laktatfabriken
Um herauszufinden, wo all dieses Laktat herkommt, untersuchte das Team verschiedene Zelltypen aus menschlicher Haut und Mausmodellen: Makrophagen (Immunzellen, die Trümmer beseitigen und die Heilung koordinieren), Blutgefäßzellen und Fibroblasten. Sie kultivierten diese Zellen auf weichen oder steifen Materialien, die normale bzw. vernarbte Haut nachahmen. Auf steifen Oberflächen schalteten nur Makrophagen in einen hochglykolytischen, also zuckerhungrigen Modus um und pumpten große Mengen Laktat aus – sowohl in Zellkulturen als auch im tatsächlichen Narbengewebe. Wurden Makrophagen aus heilenden Mauswunden entfernt, sanken die Gewebelaktatwerte und die Narbenbildung nahm ab. Diese Ergebnisse deuten darauf hin, dass besonders Makrophagen, die eine steife Umgebung wahrnehmen, die Hauptquellen des Laktats sind und das Narbenmikromilieu prägen.
Laktat als Signal, das Fibroblasten umprogrammiert
Als Nächstes fragten die Forscher:innen, wie dieses überschüssige Laktat die Fibroblasten beeinflusst. Wurden Fibroblasten in laktatreiche Flüssigkeit aus steif kultivierten Makrophagen gebadet, teilten sie sich schneller, bewegten sich mehr und produzierten mehr Kollagen – alles Kennzeichen des aggressiven Myofibroblasten-Zustands. Das Blockieren des MCT1-Transporters auf Fibroblasten oder das Reduzieren der Laktatproduktion in Makrophagen senkte diese Veränderungen deutlich. Innerhalb von Fibroblasten bewirkte einströmendes Laktat mehr als nur Energiebereitstellung: Es löste einen spezifischen chemischen Marker an Histonproteinen aus, die die DNA im Zellkern verpacken. Dieser Marker, genannt H3K23-Laktylierung, war in narbenbildenden Fibroblasten deutlich erhöht und fungierte wie ein Schalter, der zwei Schlüsselgene, HEY2 und COL11A1, aktivierte, die zusammen narbenverstärkende Signale verstärken.
Eine sich selbst verstärkende Narbenschleife
Die durch diesen Histonmarker gesteuerten Proteine bilden eine starke Rückkopplungsschleife. HEY2 steigert die Aktivität eines Signalwegs, an dem YAP1 und SMAD2 beteiligt sind und der bekannt dafür ist, Fibroblasten in einen kontraktileren, kollagenproduzierenden Zustand zu treiben. COL11A1, ein kollagenverwandtes Strukturprotein, interagiert physisch mit dem MCT1-Transporter auf Fibroblasten, stabilisiert ihn und macht die Laktataufnahme effizienter. Mit anderen Worten: Eintretendes Laktat verändert die Genregulation so, dass die Laktataufnahme und Kollagenproduktion weiter verstärkt werden und Fibroblasten in eine pro-narbenbildende Identität eingeschlossen werden. 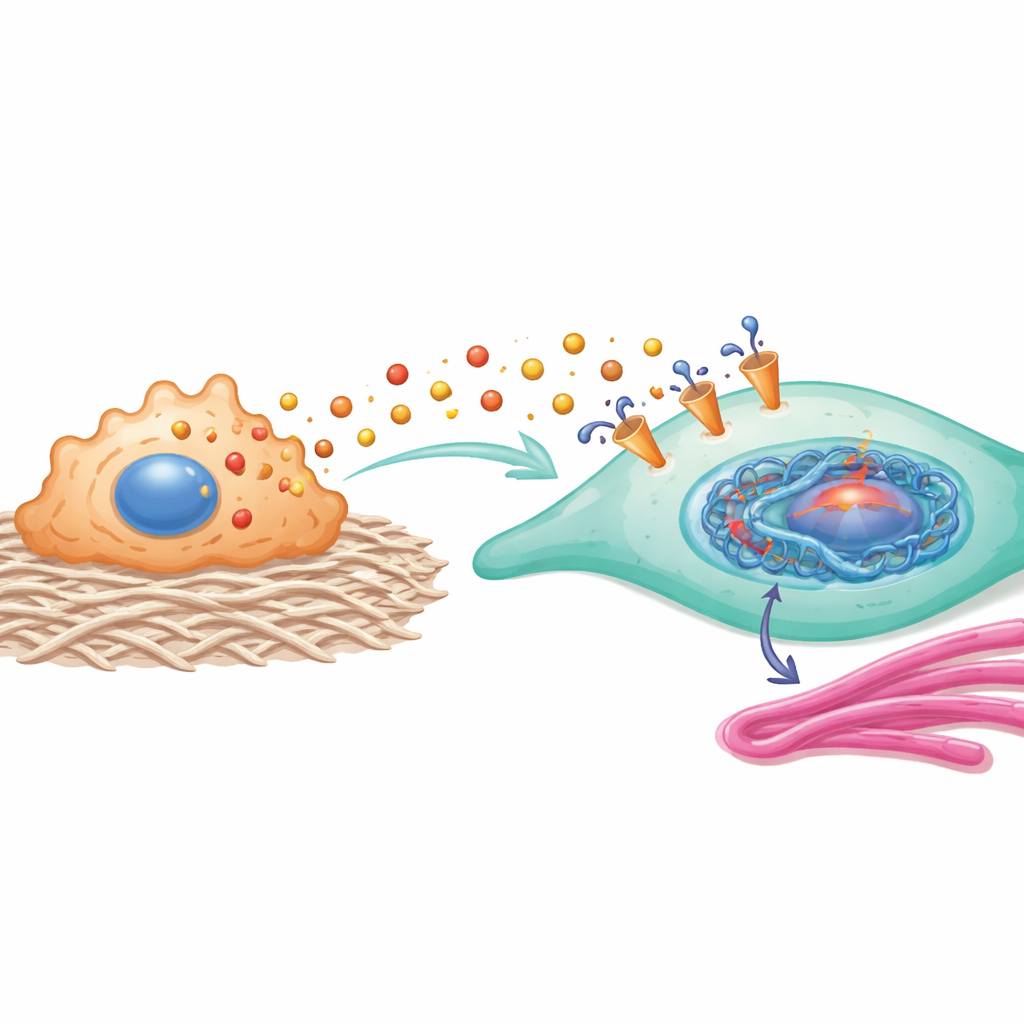
Die Schleife dämpfen, um die Heilung zu verbessern
Um zu testen, ob das Unterbrechen dieser Schleife die Heilung verbessert, verwendete das Team Mäuse, bei denen MCT1 selektiv aus Fibroblasten entfernt werden konnte, sowie ein Medikament, das MCT1 blockiert. In beiden Fällen schlossen sich Wunden schneller, die neu gebildete Haut wirkte organisierter und Kollagenfasern waren dünner und besser ausgerichtet, mit weniger Merkmalen hypertropher Narbenbildung. Der spezifische Histonmarker und seine nachgelagerten Gene gingen ebenfalls zurück. Das Entfernen der Makrophagen, der Hauptlaktatquelle, oder die chemische Senkung von Laktat hatte ähnliche Anti-Narbeneffekte. Diese Experimente zeigen, dass die Kette steife Wunde–Makrophage–Laktat–Fibroblast nicht nur eine Korrelation ist, sondern ein zentraler Treiber pathologischer Narbenbildung.
Was das für zukünftige Narbenbehandlungen bedeutet
Diese Arbeit rückt Laktat von einem einfachen Stoffwechselabfallprodukt zu einem kraftvollen Botenstoff, der Mechanik, Stoffwechsel und Genkontrolle in der Wundheilung verbindet. Indem gezeigt wird, wie von Makrophagen erzeugtes Laktat über MCT1 Histone verändert und ein sich selbst verstärkendes Narbenprogramm in Fibroblasten einschaltet, hebt die Studie mehrere vielversprechende therapeutische Zielpunkte hervor. Wirkstoffe, die die Laktatproduktion modulieren, MCT1 blockieren oder die spezifische Histonmodifikation stören, könnten eines Tages helfen, Wunden schneller und mit flacheren, weniger sichtbaren Narben heilen zu lassen.
Zitation: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Schlüsselwörter: hypertrophe Narbe, Laktat-Signalgebung, Makrophagen–Fibroblasten-Kommunikation, Histon-Laktylierung, Wundheilungstherapie