Clear Sky Science · de
Myoferlin ist Bestandteil von späten vRNP-Transportvesikeln bei behüllten RNA-Viren
Warum das für die Gesundheit im Alltag wichtig ist
Saisonale Grippe und andere Atemwegsinfektionen wirken vielleicht routinemäßig, sind aber zusammen für Millionen Todesfälle weltweit pro Jahr verantwortlich. Viele dieser Viren, darunter Influenza A und das respiratorische Synzytialvirus (RSV), umgehen bereits durch schnelle Mutationen Impfstoffe und antivirale Mittel. Diese Studie betrachtet stattdessen etwas, das Viren nicht so leicht verändern können: die zelluläre Maschinerie des Menschen, die sie kapern, um aus infizierten Zellen auszutreten. Indem die Arbeit eine gemeinsame Schwachstelle dieser Maschinerie aufdeckt, weist sie auf künftige Wirkstoffe hin, die eine ganze Bandbreite von Atemwegsviren gleichzeitig abschwächen könnten.
Eine zelluläre Lieferroute, die Viren ausnutzen
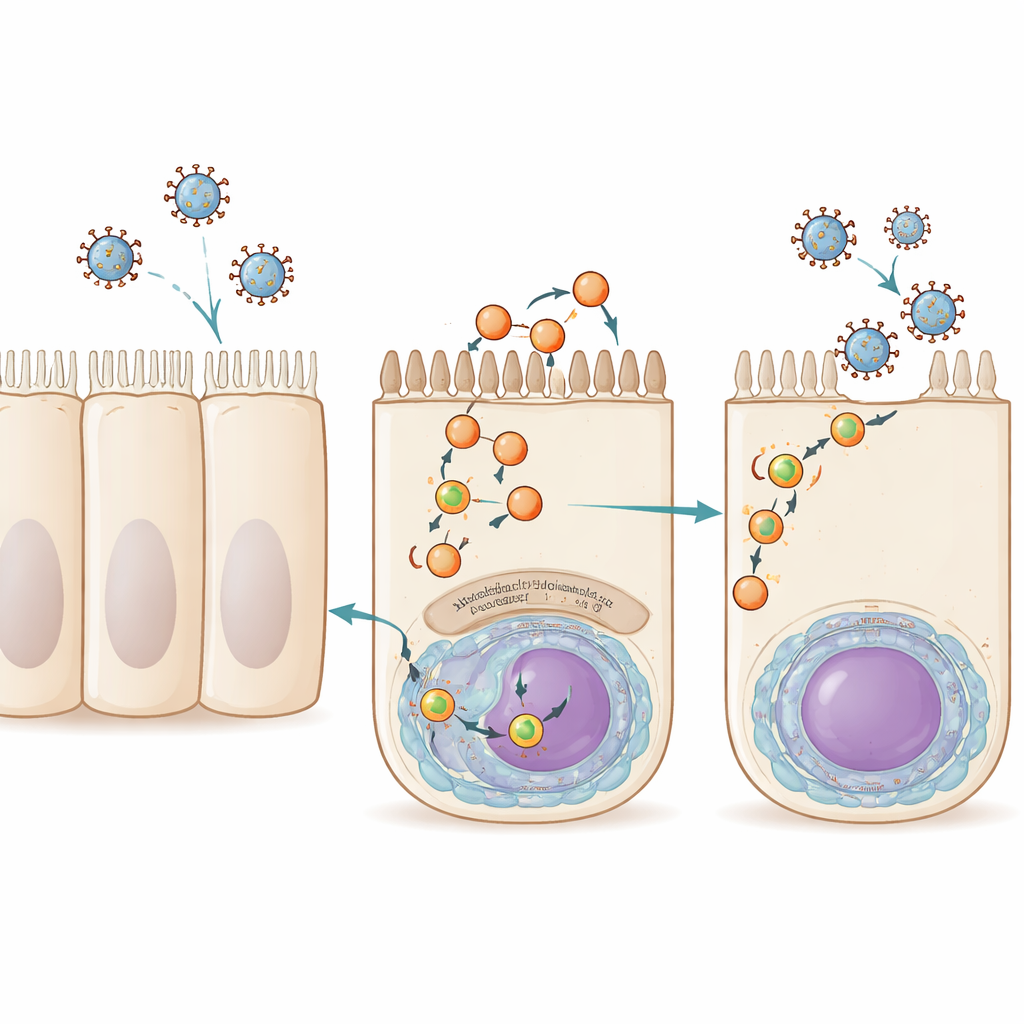
Unsere Atemwegszellen nutzen ständig Teile ihrer Außenmembran wieder, ein Prozess, der als Recycling bezeichnet wird. Kleine Membranblasen, sogenannte Vesikel, transportieren Fracht aus dem Zellinneren zurück an die Oberfläche und werden dabei von einer Proteinfamilie geleitet, die zusammen als Rab11 bekannt ist. Influenza-A-Virus, RSV und ein verwandtes Virus namens Sendai-Virus nutzen diese Route alle in späten Infektionsstadien. Sie laden ihre genetische Fracht, verpackt als Ribonukleoproteinkomplexe, auf Rab11-haltige Vesikel, die sie zur obersten (atemwegszugewandten) Seite der Zelle bringen, wo neue Viruspartikel abschnüren und sich verbreiten. Bislang war Rab11 der einzige Wirtsfaktor, der klar von diesen Transportvesikeln geteilt wurde, was ein großes Wissensloch darüber hinterließ, wie sie entstehen und funktionieren.
Entdeckung eines neuen Akteurs: Myoferlin
Die Forschenden begannen damit zu untersuchen, welche menschlichen Proteine zu verschiedenen Zeitpunkten der Infektion physisch mit dem Genom-Verpackungsapparat von Influenza assoziiert sind. Sie konstruierten ein Influenza-A-Virus, dessen Polymerase einen molekularen Markierer trug, und nutzten dann Massenspektrometrie, um menschliche Proteine zu katalogisieren, die früh und spät in der Infektion an diesen Komplex gebunden sind. Unter Hunderten von Kandidaten stach einer zu späten Zeitpunkten hervor: Myoferlin, ein großes membranassoziiertes Protein, das zuvor mit Muskelentwicklung, Endozytose und Membranreparatur in Verbindung gebracht worden war. Als das Team Myoferlin-Spiegel in aus der Lunge stammenden Zellen mittels kleiner interferierender RNAs verringerte oder es mit einem niedermolekularen Inhibitor blockierte, produzierten die Zellen weiterhin normal virale RNA und virale Proteine, setzten aber deutlich weniger infektiöse Influenzapartikel frei. Das deutet darauf hin, dass Myoferlin nicht für die Kopie des viralen Genoms benötigt wird, wohl aber für die späten Stadien, in denen neue Viren zusammengesetzt werden und die Zelle verlassen.
Myoferlin reist mit viraler Fracht
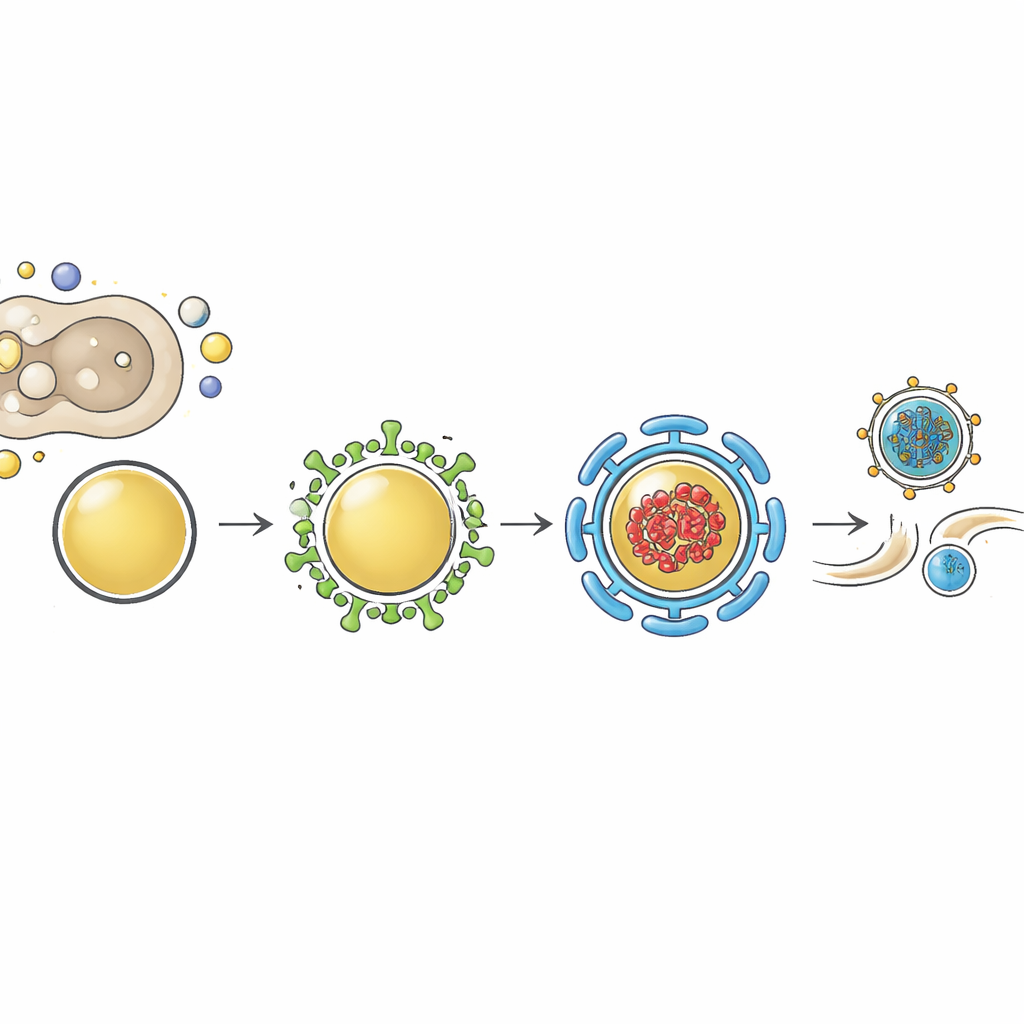
Hochauflösende Bildgebung zeigte, wo Myoferlin während der Infektion lokalisiert ist. In unveränderten Zellen überlappt Myoferlin weitgehend mit Rab11-positiven Recyclingvesikeln, sowohl in der Nähe des Zellkerns als auch in Richtung Zellrand, und der Verlust eines der beiden Proteine stört die normale Verteilung des jeweils anderen. Während einer Influenza-Infektion wird das Rab11-Netzwerk dramatisch umgestaltet zu vergrößerten, unregelmäßigen Vesikeln, die virale Ribonukleoproteine transportieren. Myoferlin bleibt in diesen umgestalteten Vesikeln erhalten und zeigt eine starke Kolokalisation mit dem viralen Genom und Rab11. Als das Team ein Medikament einsetzte, das virale Genomkomplexe und ihre Trägervesikel verklumpen lässt, wurde Myoferlin in dieselben Aggregate hineingezogen, was bestätigt, dass es ein fester Bestandteil dieser späten Transportstrukturen ist und nicht nur zufällig in der Nähe vorkommt.
Ein gemeinsamer Knotenpunkt für mehrere Atemwegsviren
Die Studie prüfte anschließend, ob diese Abhängigkeit von Myoferlin einzigartig für Influenza ist oder breiter geteilt wird. Das Herunterregulieren von Myoferlin in Lungenzellen, die mit RSV oder Sendai-Virus infiziert waren, führte erneut zu einem starken Rückgang an freigesetzten infektiösen Viren, ohne die Mengen an viraler RNA zu senken. Einzelmolekül-Bildgebung zeigte, dass die Genome beider Viren zusammen mit Myoferlin und Rab11 in zytoplasmatischen Punkten zusammenlaufen, die wahrscheinlich Transportknoten und nicht Replikationsfabriken darstellen. Dieses Muster stützt ein einheitliches Bild: Verschiedene behüllte respiratorische RNA-Viren, trotz unterschiedlicher Lebensweisen, konvergieren beim Transport ihrer fertigen Genome zur Zelloberfläche für Verpackung und Austritt auf dasselbe Rab11–Myoferlin-Vesikelsystem.
Wie Myoferlin virusbeladene Vesikel formt
Myoferlin besteht aus mehreren C2-Domänen, die Membranen und Partnerproteine binden können. Frühere Arbeiten zeigten, dass eine dieser Domänen eine Familie membranumformender Proteine namens EHDs anspricht. In dieser Studie wurden fluoreszenzmarkierte EHD1 und EHD2 in denselben umgestalteten Vesikeln gefunden, die Influenza-Genome und Rab11 transportieren, besonders wenn diese Vesikel experimentell verklumpt wurden. Eine Reduktion von EHD2-Niveaus verringerte, ähnlich wie die Reduktion von Myoferlin, die Influenza-Ausbeute, ohne die Genomreplikation zu beeinflussen. Darüber hinaus führte das Entfernen von Myoferlin zu einem Absinken der EHD2-Proteinmenge, was nahelegt, dass Myoferlin hilft, EHD2 auf Membranen zu stabilisieren oder korrekt zu positionieren. Die Autorinnen und Autoren schlagen vor, dass Myoferlin auf Rab11-positiven Vesikeln sitzt und EHD-Proteine rekrutiert, um deren Membranen zu formen, wodurch spezialisierte „unregelmäßig beschichtete Vesikel“ entstehen, die für den Transport viraler Fracht zu Abschnürungsstellen optimiert sind.
Was das für künftige antivirale Strategien bedeutet
In der Summe positionieren die Ergebnisse Myoferlin als zentralen Organisator einer Wirtsrecycling-Route, auf die sich viele behüllte Atemwegsviren in einem kritischen späten Schritt stützen. Da die alleinige Zielsetzung viraler Proteine oft schnell zu Resistenzen führt, sind Wirtsfaktoren, die von mehreren Viren wiederverwendet werden, attraktive Wirkstoffziele. Das Stören von Myoferlins Funktion oder seiner Partnerschaften mit Rab11 und EHD-Proteinen könnte prinzipiell die Ausbreitung verschiedener Erreger verlangsamen oder blockieren, von Influenza und RSV bis hin zu anderen Rab11-abhängigen Viren wie einigen Coronaviren. Es bleibt viel zu tun, um dieses Konzept in sichere Therapien zu überführen, aber die Studie liefert eine detaillierte Karte einer gemeinsamen Fluchtroute der Viren — und rückt Myoferlin als vielversprechenden Engpass auf diesem Pfad ins Blickfeld.
Zitation: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Schlüsselwörter: Influenza, Atemwegsviren, vesikulärer Transport, Wirtfaktoren, Myoferlin