Clear Sky Science · de
Ingenieurmäßig hergestellte Exosom-Nanovesikel zur Abgabe von Antikörpern zur Behandlung entzündlicher Darmerkrankungen
Neue Hoffnung für eine hartnäckige Darmerkrankung
Entzündliche Darmerkrankungen (IBD) können den Alltag in einen ständigen Kampf mit Schmerzen, Durchfall und Müdigkeit verwandeln und erhöhen langfristig das Risiko für Darmkrebs. Viele der heute eingesetzten Medikamente beruhigen zwar Schübe, setzen aber die fehlgeleiteten Immunreaktionen, die der Krankheit zugrunde liegen, nicht dauerhaft zurück, sodass die Symptome oft zurückkehren. Diese Studie stellt ein raffiniert konstruiertes „intelligentes“ Nanopartikel vor, das über den Blutkreislauf reist, entzündete Bereiche des Darms findet und eine zweigleisige Behandlung abliefert, die sowohl schädliche Entzündungen dämpft als auch ein nachhaltiges immunologisches Gleichgewicht wiederaufbaut.
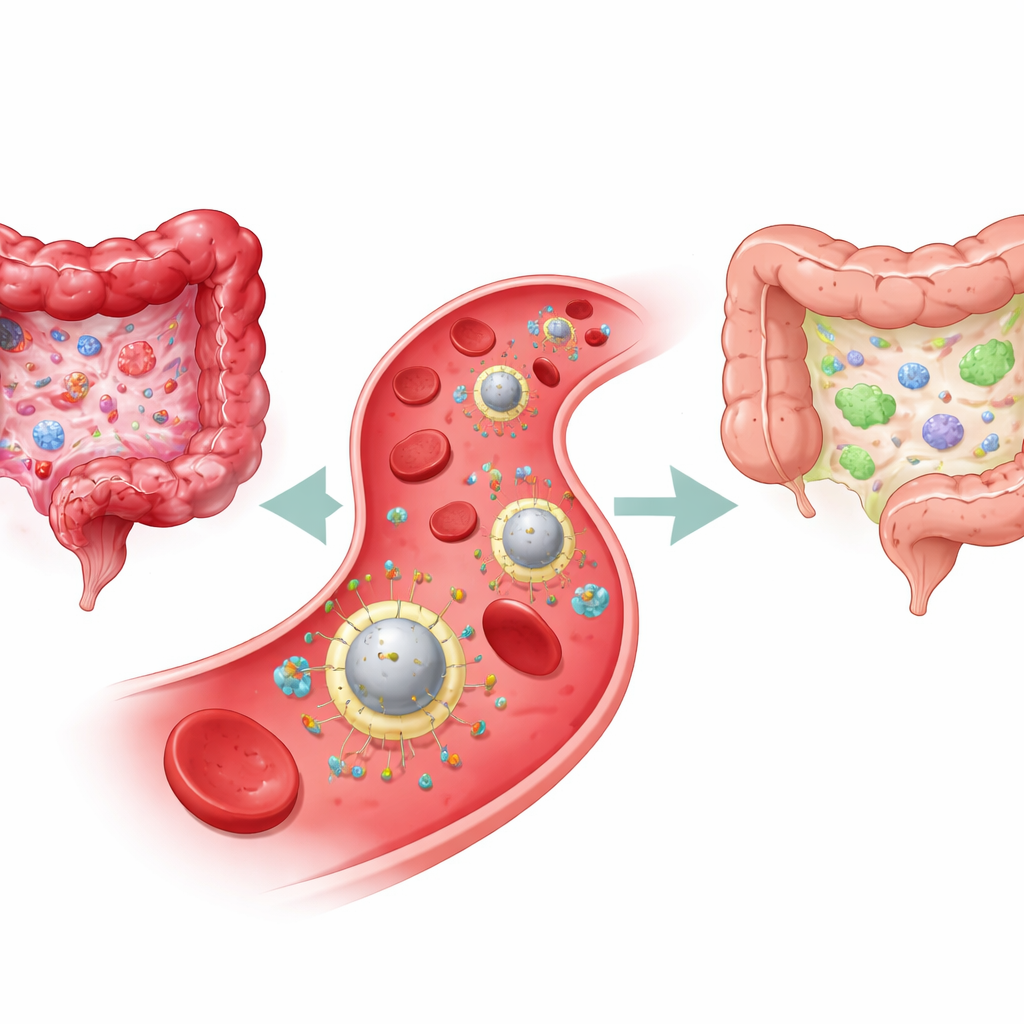
Warum aktuelle Behandlungen nicht ausreichen
IBD, zu der Morbus Crohn und Colitis ulcerosa zählen, entsteht aus einem chronischen Tauziehen im Immunsystem des Darms. Auf der einen Seite stehen aggressiven Immunzellen und entzündungsfördernde Moleküle, die die Darmschleimhaut schädigen; auf der anderen Seite regulierende Zellen, die diese Reaktion normalerweise im Zaum halten. Standardtherapien — wie Steroide, Immunsuppressiva und biologische Wirkstoffe — zielen hauptsächlich darauf ab, Entzündungen im ganzen Körper abzumildern. Sie können Symptome lindern, stellen aber häufig das zugrunde liegende immunologische Gleichgewicht nicht wieder her, und eine breite Immunsuppression erhöht das Infektionsrisiko. Selbst neuere Antikörpertherapien, die ein wichtiges Entzündungssignal namens Interleukin‑23 (IL‑23) blockieren, helfen nur einem Teil der Patientinnen und Patienten und zirkulieren weiterhin weitreichend, statt nur dort zu wirken, wo sie gebraucht werden.
Entwicklung einer zielgerichteten, formwandelnden Medizin
Die Forschenden wollten eine Behandlung entwickeln, die sich mehr wie eine lebende Zelle als wie ein simples Medikament verhält. Sie begannen mit winzigen Vesikeln, die natürlicherweise von regulatorischen T‑Zellen freigesetzt werden — Immunzellen, die Toleranz und Friedenssicherung fördern. Diese Vesikel, Exosomen genannt, tragen Proteine und genetisches Material, die andere Immunzellen in einen beruhigenden Zustand lenken können. Das Team verschmolz diese Exosomen mit Fragmenten von Thrombozytenmembran und nutzte so das Vermögen der Blutplättchen, an beschädigten Blutgefäßen in entzündetem Gewebe haften zu bleiben. An die Oberfläche dieser hybriden Hülle befestigten sie IL‑23‑blockierende Antikörper mithilfe einer molekularen „Schnur“, die von Enzymen (Matrix‑Metalloproteinasen) durchschnitten werden kann — Enzyme, die nur im entzündeten Darmgewebe vermehrt vorkommen. Das Ergebnis, PrEXO‑a23 genannt, ist eine Nanovesikel, die im Blut zirkuliert, an verletzte Darmgefäße andockt und ihre Antikörperfracht nur dort freisetzt, wo die Krankheit aktiv ist.
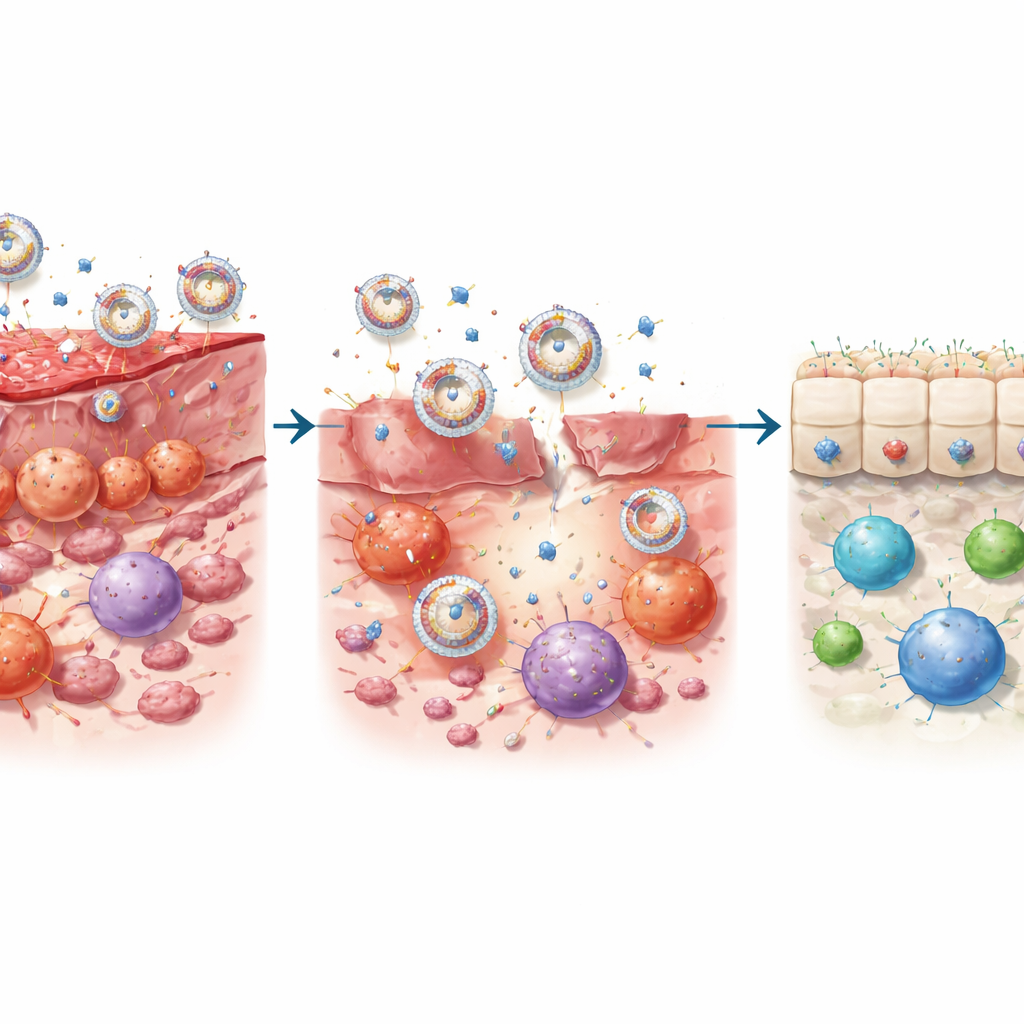
Umerziehung des immunologischen Umfelds im Darm
In Zellstudien übertraf PrEXO‑a23 sowohl den Antikörper allein als auch die Exosomen allein. Es reduzierte stark die Bildung entzündlicher T‑Helfer‑17‑(Th17‑)Zellen und die Freisetzung schädlicher Zytokine, die die Darmschleimhaut angreifen, und schützte gleichzeitig menschliche Darmepithelzellen vor dem Absterben. Gleichzeitig brachte es dendritische Zellen — die Torwächter, die T‑Zellen anleiten — von einem feindseligen, aktivierenden Zustand in einen „toleranten“ Zustand, der das Wachstum regulatorischer T‑Zellen fördert. In Mausmodellen der Kolitis suchten die Nanovesikel effizient entzündetes Darmgewebe auf, wurden von verschiedenen Immunzelltypen aufgenommen und setzten Antikörper als Reaktion auf lokale Enzymaktivität frei. Diese doppelte Wirkung — Blockade der IL‑23‑getriebenen Entzündung und Verstärkung toleranzfördernder Signale — brachte Entzündungsmarker nahe an normale Werte zurück und stellte ein gesünderes Verhältnis von T‑Zelltypen wieder her.
Gewebe reparieren und langfristige Schäden verhindern
Mäuse mit chemisch induzierter Kolitis, die PrEXO‑a23 erhielten, verloren weniger Gewicht, hatten längere, gesündere Därme und zeigten weniger Milzvergrößerung, ein Zeichen systemischer Entzündung. Die mikroskopische Untersuchung zeigte erhaltene Darmarchitektur und engere Verbindungen zwischen Epithelzellen, was auf eine reparierte Barriere hinweist. Die Behandlung trug außerdem zur Wiederherstellung eines ausgewogeneren Darmmikrobioms bei, indem Familien gefördert wurden, die mit Darmgesundheit assoziiert sind, und solche reduziert wurden, die mit Krankheit in Verbindung stehen. In einem schwereren Modell, das den Übergang von chronischer Kolitis zu Darmkrebs nachahmt, lindert PrEXO‑a23 nicht nur die anhaltende Entzündung, sondern verhinderte vollständig die Tumorentwicklung und bremste die Verdickung und Vernarbung der Darmwand, die für Fibrose typisch sind. Molekulare Analysen deuteten auf die Wiederherstellung schützender p53‑Signalwege hin — ein zentraler Wächter gegen Krebs — die für den anti‑tumorösen Effekt wichtig waren.
Auf dem Weg zu intelligenterer, dauerhafterer IBD‑Versorgung
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass diese Arbeit über ein bloßes „Herunterregeln“ von Entzündungen hinausgeht. Indem zielgerichtete Abgabe, vor Ort erfolgende Antikörperfreisetzung und immunberuhigende Exosomenfracht in einem winzigen Paket kombiniert werden, beruhigt PrEXO‑a23 sowohl aktive Erkrankung als auch hilft, das Immunsystem auf dauerhafte Toleranz umzuschulen. Bei Mäusen führte dies nicht nur zu einer Linderung der Symptome, sondern auch zu Schutz vor Vernarbung und Darmkrebs, zwei der gefürchtetsten Komplikationen langjähriger IBD. Obwohl noch umfangreiche Prüfungen nötig sind, bevor eine solche Therapie Patienten erreichen kann, zeigt die Studie, wie biologisch inspirierte Nanomedikamente eines Tages präzisere und langlebigere Kontrolle über komplexe Immunerkrankungen wie IBD ermöglichen könnten.
Zitation: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Schlüsselwörter: entzündliche Darmerkrankung, Nanotherapie, Immuntoleranz, Exosomen, Kolonkarzinom‑Prävention