Clear Sky Science · de
Strukturelle Defekte in Amyloid-β-Fibrillen treiben die sekundäre Nukleation an
Warum winzige Fehler in Hirnproteinen wichtig sind
Bei Alzheimer und verwandten Erkrankungen verklumpen bestimmte Proteine zu langen, fadenförmigen Strukturen, den Amyloid-Fibrillen. Diese Fibrillen sind nicht nur Marker der Krankheit; sie fördern auch die Entstehung neuer, hochtoxischer Proteinpartikel, die Nervenzellen schädigen können. Die Studie stellt eine einfache, aber entscheidende Frage: Wirken seltene strukturelle „Fehler“ innerhalb von Amyloid-Fibrillen als die Haupt-Hotspots, die neues schädliches Wachstum auslösen? Die Antwort könnte auf neue Wege hinweisen, diese Erkrankungen zu verlangsamen oder zu stoppen, indem nur wenige kritische Stellen statt der gesamten Proteinoberfläche gezielt angegangen werden. 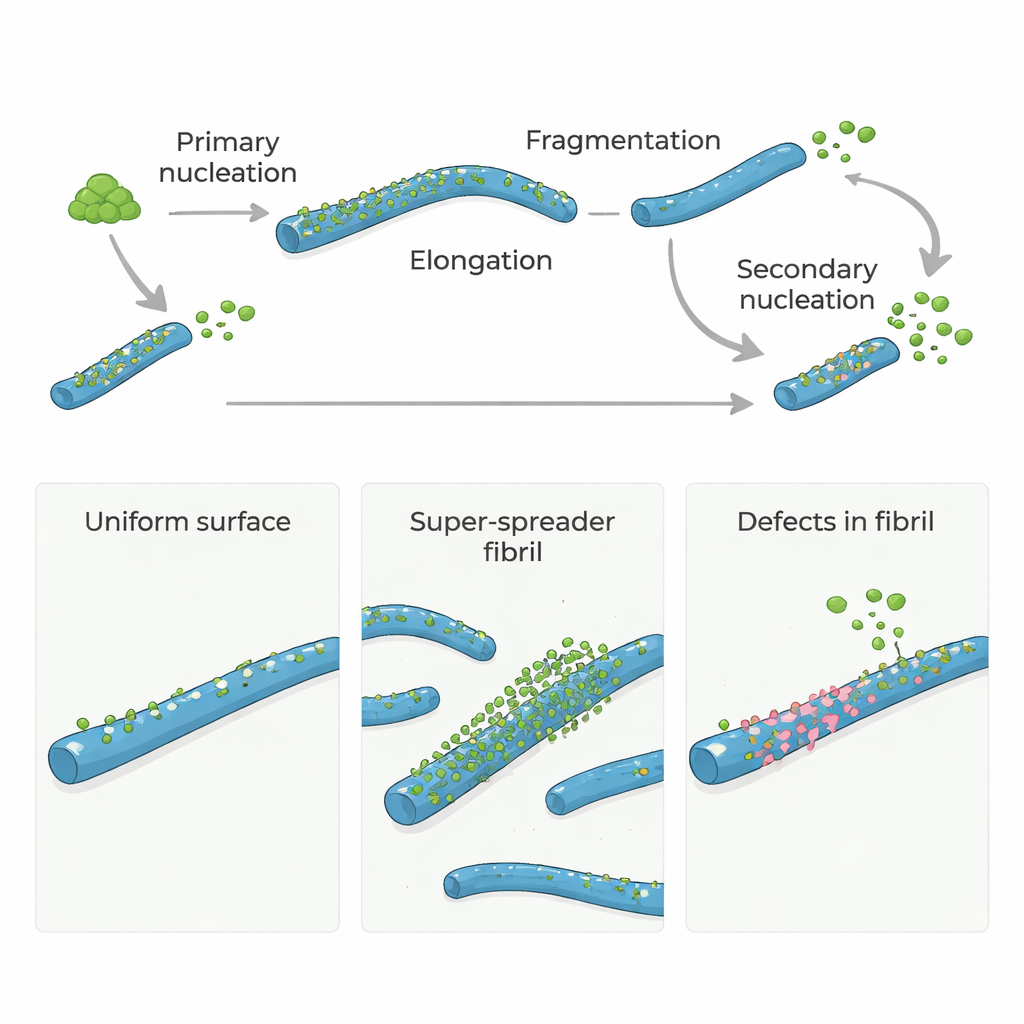
Vom ruhigen Protein zur außer Kontrolle geratenen Kettenreaktion
Amyloid-β (Aβ)-Proteine, die eine zentrale Rolle bei Alzheimer spielen, bilden normalerweise nicht schnell von selbst Aggregate. Damit es losgeht, müssen einige Monomere langsam die ersten winzigen Fibrillen bilden, ein Schritt, der als primäre Nukleation bezeichnet wird. Sobald diese anfänglichen Fibrillen existieren, wachsen sie schnell weiter, wenn weitere Monomere an ihren Enden anlagern. Noch wichtiger ist, dass bestehende Fibrillen auf ihren Oberflächen neue Fibrillen auslösen können — ein Prozess, der als sekundäre Nukleation bekannt ist. Dieser oberflächengetriebene Schritt kann das System mit neuen Fibrillen und kleinen, toxischen Oligomeren überschwemmen und aus einem langsamen Rinnsal eine unkontrollierbare Kettenreaktion machen.
Sind alle Fibrilloberflächen gleichermaßen gefährlich?
Viele Modelle gingen bisher davon aus, dass die gesamte Oberfläche einer Amyloid-Fibrille gleichermaßen gut in der Katalyse sekundärer Nukleation ist. Neuere Experimente deuteten jedoch an, dass nur ein kleiner Bruchteil der Oberfläche wirklich aktiv ist. Um dem nachzugehen, nutzten die Autoren ein natürliches molekulares „Chaperon“ namens Brichos, das dafür bekannt ist, die sekundäre Nukleation von Aβ40 und Aβ42 (zwei wichtige Formen von Amyloid-β) zu blockieren. Durch genaue Messungen, wie viel fluoreszenzmarkiertes Brichos an Fibrillen bindet, fanden sie heraus, dass es zwar stark bindet, aber nur in sehr geringer Zahl: etwa ein Brichos-Molekül pro 100–150 Aβ-Moleküle in einer Fibrille. Trotzdem reichte diese spärliche Besetzung aus, um mehr als 90 % der sekundären Nukleation zu unterdrücken, was bedeutet, dass nur seltene, lokalisierte Stellen — und nicht die gesamte Oberfläche — die Produktion neuer toxischer Aggregate dominieren.
Die Rolle verborgener Defekte untersuchen
Diese Ergebnisse legten nahe, dass die entscheidenden Nukleationsstellen strukturelle Defekte sein könnten — kleine Unregelmäßigkeiten, die beim Fibrillenwachstum entstehen, etwa fehlgelegte Schichten oder teilweise freigelegte innere Kerne. Um diese Idee direkt zu prüfen, züchteten die Forschenden Aβ40-Fibrillen unter zwei verschiedenen Bedingungen. Eine Gruppe, die „Kontroll“-Fibrillen, entstand unter typischen, stark übersättigten Bedingungen, die schnelles Wachstum und kinetisches Einfrieren von Defekten begünstigen. Die andere Gruppe wurde mit einem langsamen, temperaturkontrollierten Annealing-Protokoll erzeugt: Fibrillen wurden bei sehr geringer effektiver Triebkraft nahe ihrer Löslichkeitsgrenze gewachsen, wo inkorrekte Strukturen sich auflösen oder reparieren können, bevor sie dauerhaft werden. Hochauflösende Kryo-Elektronenmikroskopie zeigte, dass beide Fibrillgruppen in Form und Torsion im Wesentlichen identisch aussahen, was darauf hinweist, dass der Annealing-Prozess die grundlegende Morphologie nicht veränderte. 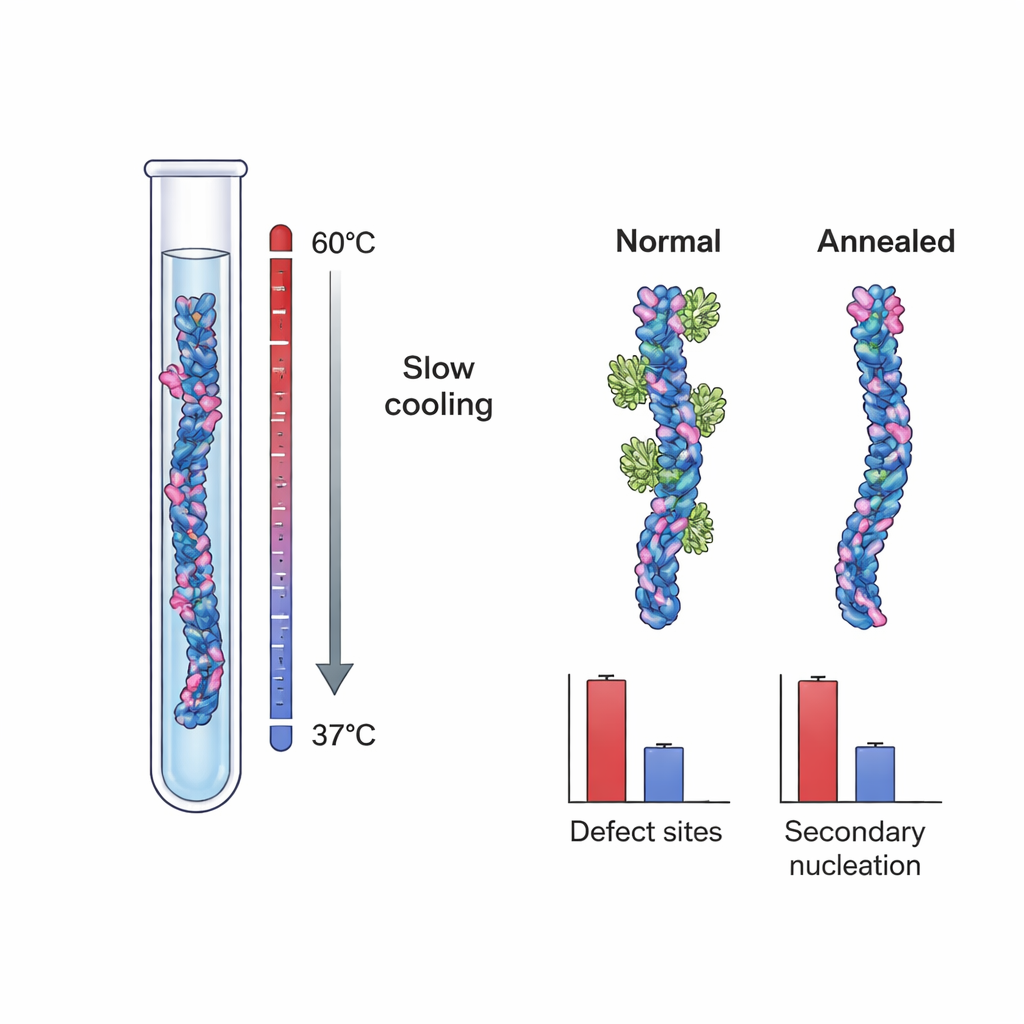
Weniger Mängel, weniger gefährliche Wachstumsstellen
Als das Team die Brichos-Bindung an diese beiden Fibriltypen maß, entdeckten sie einen auffälligen Unterschied. Kontroll-Aβ40-Fibrillen hatten etwa eine Brichos-Bindungsstelle pro ~100 Monomeren, was erneut seltene, aber wichtige Stellen anzeigt. Annealierte Fibrillen hingegen wiesen nur etwa eine Stelle pro ~800 Monomeren auf — eine Reduktion der Stellenhäufigkeit um nahezu 90 %. In separaten Tests, bei denen diese Fibrillen als „Seeds“ zu frischen Aβ40-Lösungen hinzugefügt wurden, waren die annealierten Fibrillen viel weniger effektiv darin, neue Aggregation auszulösen, selbst wenn ihre Gesamtmasse an die der Kontrollfibrillen angepasst war. Detaillierte kinetische Modellierung zeigte, dass dieser Rückgang der Seed-Wirksamkeit sich nicht allein durch Unterschiede in der Fibrillenlänge erklären ließ. Stattdessen stimmte er quantitativ mit der reduzierten Anzahl von Brichos-Bindungsstellen überein und stärkte damit die Idee, dass Wachstumsdefekte die Haupttriebkräfte der sekundären Nukleation sind.
Ein allgemeines Prinzip mit therapeutischem Potenzial
Durch die Kombination thermodynamischer Argumente, Neubewertung früherer Arbeiten und Vergleiche zwischen mehreren amyloidbildenden Proteinen argumentieren die Autoren, dass seltene Wachstumsdefekte wahrscheinlich in vielen Systemen zentral für die sekundäre Nukleation sind — nicht nur bei Alzheimer-assoziiertem Aβ. Diese Defekte legen teilweise den dicht gepackten inneren Kern der Fibrille frei und bieten eine vorgefertigte Schablone, auf der sich neue Oligomere und Fibrillen weit leichter bilden können als auf einer glatten Oberfläche. Die Anerkennung dieser Defekte als Schlüsseltäter eröffnet neue Wege für die Wirkstoffentwicklung. Statt zu versuchen, jede mögliche Wechselwirkung auf einer Fibrillenoberfläche zu blockieren, könnten Therapien darauf abzielen, genau diese knappen Defektstellen abzuschirmen oder zu reparieren oder die Bedingungen zu reduzieren, die sie überhaupt erst erzeugen. Praktisch könnte das bedeuten, die effektive Konzentration amyloidbildender Proteine im Gehirn zu senken oder Moleküle zu entwerfen, die von Brichos inspiriert sind und Defekt-getriebene Nukleations-Hotspots erkennen und neutralisieren. Gelingt dies, könnten solche Strategien die Hauptquelle toxischer Oligomere abschneiden und das Fortschreiten amyloid-verbundener Erkrankungen verlangsamen.
Zitation: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Schlüsselwörter: Amyloid-Fibrillen, Alzheimer-Krankheit, sekundäre Nukleation, Proteinaggregation, Brichos-Chaperon