Clear Sky Science · de
Sauerstoffverarmung in biomolekularen Kondensaten wird von der makromolekularen Dichte bestimmt
Unsichtbare Taschen innerhalb lebender Zellen
In unseren Zellen sind viele chemische Reaktionen auf eine konstante Sauerstoffzufuhr angewiesen. Zellen sind jedoch keine einfachen Flüssigkeitsbeutel: sie enthalten winzige, tröpfchenähnliche Kompartimente, sogenannte biomolekulare Kondensate, die sich ohne Membranen bilden. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Verändern diese Tröpfchen die Verfügbarkeit von Sauerstoff in verschiedenen Zellbereichen, und wenn ja, warum? Die Antwort stellt gängige Vorstellungen darüber in Frage, wie sich kleine Moleküle in diesen dichten Mikroumgebungen verhalten.

Tröpfchen ohne Wände
Biomolekulare Kondensate sind weiche, flüssigkeitsähnliche Ansammlungen von Proteinen und Nukleinsäuren, die nach Bedarf assembliert und aufgelöst werden. Sie strukturieren die Biochemie, indem sie bestimmte Moleküle konzentrieren und andere ausschließen, obwohl sie keine umgebende Membran besitzen. Frühere Arbeiten zeigten, dass viele kleine Metaboliten und verfahrlikende Verbindungen in diese Tröpfchen hineingezogen werden, typischerweise weil das Innere im Vergleich zur wässrigen Zellflüssigkeit etwas wie ein öliges Lösungsmittel wirkt. Sauerstoff ist jedoch ein Sonderfall: er ist ein kleines Gasmolekül, das die Zellatmung antreibt, aber auch schädliche Nebenreaktionen fördert. Ob Kondensate Sauerstoff anreichern oder verdrängen, könnte daher beeinflussen, wie effizient Enzyme arbeiten und wie viel oxidative Schäden in der Nähe oder innerhalb dieser Tröpfchen auftreten.
Sauerstoffmessung in winzigen Kompartimenten
Um die Sauerstoffwerte innerhalb von Kondensaten zu untersuchen, bauten die Forscher ein einfaches, aber einstellbares Modellsystem aus künstlich entworfenen, flexiblen Proteinen, die in Salzlösungen leicht Tröpfchen bilden. Zunächst erzeugten sie großflächige, makroskopische Phasen durch Zentrifugation der Proben und führten dann haarfeine elektrochemische Mikroelektroden ein, um die Sauerstoffkonzentration direkt über die Grenze zwischen proteinreichen und proteinarmen Schichten hinweg abzulesen. Diese Messungen zeigten, dass die Sauerstoffwerte fallen, wenn die Sonde in die proteinreiche Phase eindringt: die Tröpfchen schließen Sauerstoff teilweise aus, anstatt ihn aufzusaugen.
Sauerstoff sichtbar machen mit speziellen Farbstoffen
Weil Elektroden kleine Tröpfchen stören, griff das Team zur phosphoreszenzlebensdauer-basierten Bildgebung, einer optischen Methode, die spezielle Farbstoffmoleküle verwendet, deren Leuchten kürzer anhält, wenn mehr Sauerstoff vorhanden ist. Durch Verfolgen der Leuchtdauer innerhalb und außerhalb einzelner Tröpfchen und sorgfältige Korrektur dafür, wie die Tröpfchenumgebung das Grundverhalten des Farbstoffs verändert, konnten sie Sauerstoffkonzentrationen ableiten, ohne die Kondensate physikalisch zu stören. Unter verschiedenen Bedingungen stimmten die optischen Daten mit den Elektrodenmessungen überein: Der Sauerstoffgehalt ist innerhalb der Kondensate durchweg niedriger als in der umgebenden Lösung. Computersimulationen mit einem grob modellierten molekularen Modell unterstützten dieses Bild und zeigten, dass sich Sauerstoff relativ wenig Zeit in den dichten Proteinregionen aufhält.
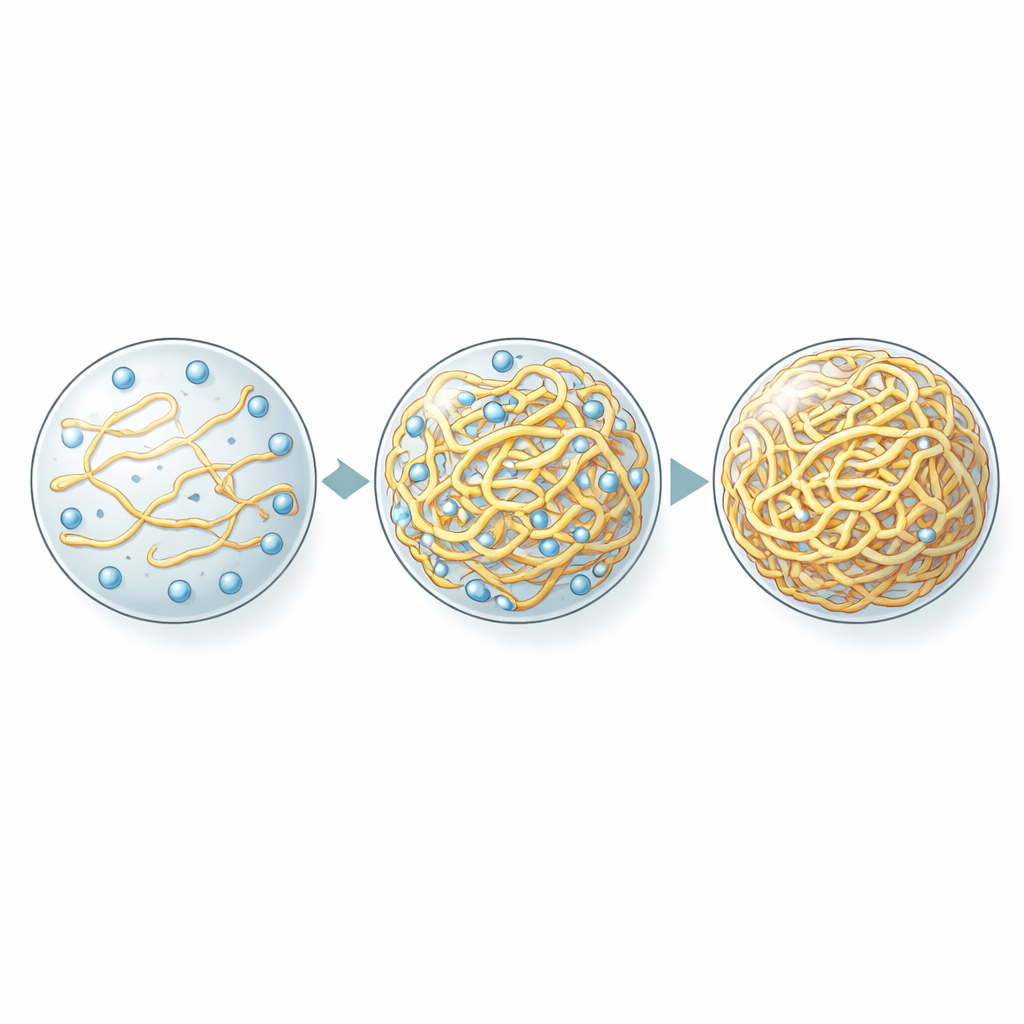
Dichte, nicht Fettigkeit, bestimmt den Sauerstoffgehalt
Der naheliegende Verdächtige für die Steuerung der Sauerstoffaufnahme ist die Hydrophobizität — die „Fettigkeit" des Tröpfcheninneren — die zuvor als entscheidender Faktor dafür identifiziert worden war, wie viele andere kleine Moleküle in Kondensate partitionieren. Um das zu prüfen, veränderten die Autoren systematisch die Proteinsequenzen, sowohl in der Anzahl der Wiederholungseinheiten als auch in ihrem hydrophoben Charakter, und maßen dann den Sauerstoffgehalt in den entstehenden Tröpfchen. Überraschenderweise korrelierte der Sauerstoffgehalt nicht mit der ölig- oder wasserähnlichen Natur der Tröpfchen. Stattdessen hing er stark und umgekehrt mit der Menge an Protein zusammen, die in der dichten Phase gepackt war. Varianten, die dichtere Kondensate bildeten, enthielten weniger Sauerstoff, selbst wenn sie insgesamt weniger hydrophob waren. Andere kleine, ölige Farbstoffe verhielten sich anders: sie bevorzugten weiterhin hydrophobere Tröpfchen, was bestätigte, dass Sauerstoff die üblichen Regeln durchbricht.
Neue Sicht auf nanoskalige Sauerstoffgradienten
Diese Ergebnisse führen zu einer überarbeiteten Sicht darauf, wie Kondensate ihre chemische Umgebung formen. Für kleine Moleküle, die nicht stark an die Gerüstproteine binden, wird die schiere Dichte der Makromoleküle zum dominierenden Faktor: je mehr Volumen die Proteine einnehmen, desto weniger Raum bleibt für gelösten Sauerstoff. Das bedeutet, dass Zellen Sauerstoffgradienten über Nanometer- bis Mikrometerdistanzen erzeugen können, allein durch die Bildung oder Auflösung von Kondensaten oder durch Veränderung der Packungsdichte dieser Tröpfchen. Praktisch gesehen legt die Arbeit nahe, dass membranlose Organellen die Verfügbarkeit von Sauerstoff für nahegelegene Reaktionen subtil einstellen können — möglicherweise indem sie einige beschleunigen, andere verlangsamen oder empfindliche Komponenten schützen — durch einen physikalischen Crowding-Effekt und nicht durch spezifische chemische Bindung.
Zitation: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
Schlüsselwörter: biomolekulare Kondensate, Sauerstoffpartitionierung, makromolekulare Crowding, Phasentrennung, zelluläre Mikroenvironmente