Clear Sky Science · de
Ultraschneller lösungsmittelgesteuerter Roaming‑Mechanismus in Bromoform aufgedeckt durch Femtosekunden‑Röntgenstreuung in Lösung
Warum winzige Moleküle in Wasser und Luft wichtig sind
Bromoform ist ein kleines, natürlich vorkommendes Molekül mit großen ökologischen Auswirkungen. Wenn Sonnenlicht dieses Molekül in der Atmosphäre oder in Meeresspray trifft, kann es Bromatome freisetzen, die zur Zerstörung von Ozon beitragen – jener Schutzschicht, die uns vor den schädlichen ultravioletten Strahlen der Sonne bewahrt. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Verändert die flüssige Umgebung um Bromoform herum das, was in den ersten Billionsteln einer Sekunde nach Lichteinfall geschieht, und beeinflusst damit, wie viel ozonabbauendes Brom letztlich entsteht?
Licht, das ein Molekül auseinanderreißt
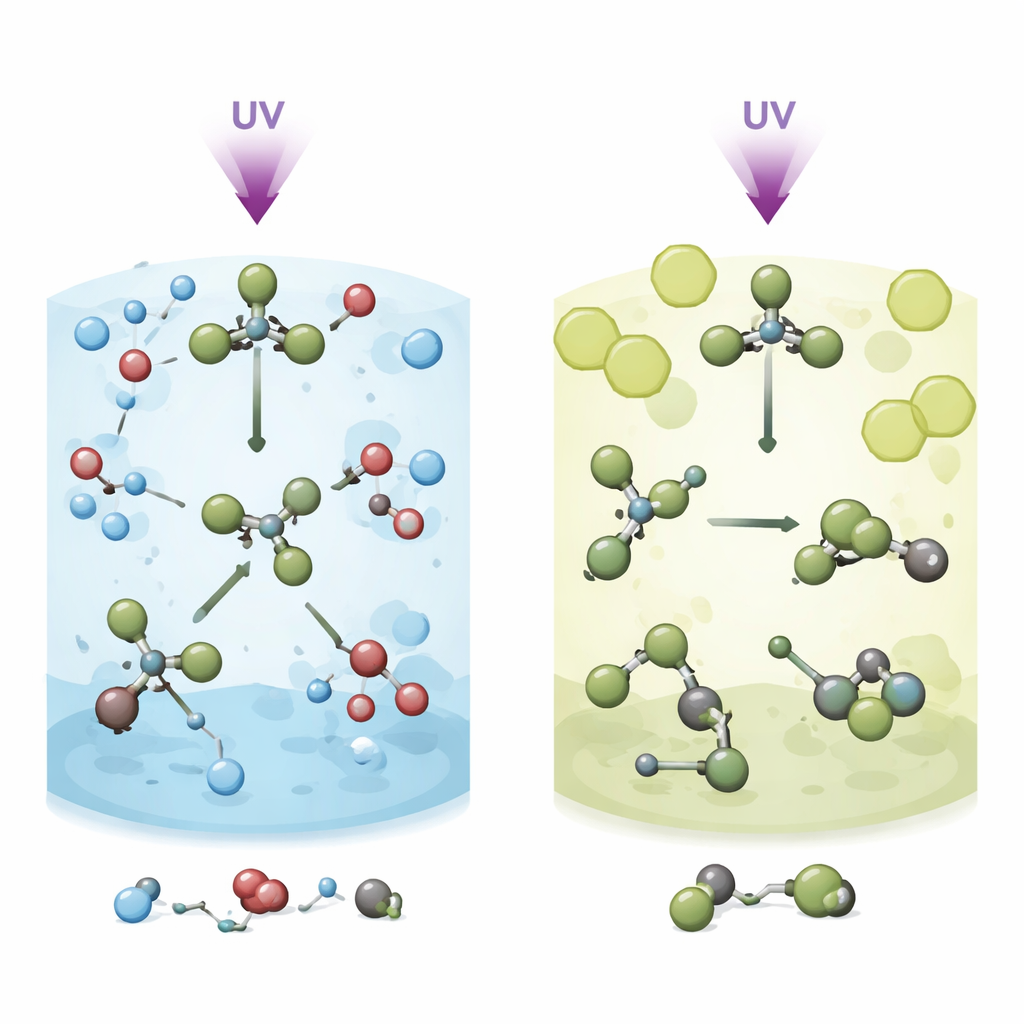
Die Forschenden beginnen damit, extrem kurze Ultraviolett‑Blitze auf in zwei verschiedenen Flüssigkeiten gelöstes Bromoform zu richten: Methanol, das polar und chemisch reaktiv ist, und Methylcyclohexan, das unpolar und vergleichsweise inert ist. Das Licht schwächt rasch eine der Kohlenstoff‑Brom‑Bindungen und veranlasst das Molekül, auseinanderzufallen. Anstatt jedoch einfach wegzufliegen, verharrt ein Bromatom und „streift“ um das verbleibende Fragment CHBr₂ herum. Diese Roaming‑Bewegung erzeugt eine flüchtige, umgestaltete Form, ein Isomer. Das zentrale Rätsel ist, was mit diesem roamingartigen Zwischenzustand in verschiedenen Flüssigkeiten geschieht und wie diese Entscheidung steuert, ob Bromoform freie Bromatome freisetzt oder in andere Produkte abgelenkt wird.
Molekulare Filme mit Röntgenstrahlen aufnehmen
Um diese Vorgänge zu beobachten, nutzt das Team femtosekundenaufgelöste Röntgenstreuung in Lösung am Europäischen Röntgen‑Frei‑Elektronen‑Laser. Im Grunde nehmen sie einen Stroboskop‑Film auf, der zeigt, wie sich Zwischenatomdistanzen in Echtzeit verändern, mit sowohl Pikosekunden‑ als auch Sub‑Pikosekunden‑Auflösung. Durch den Vergleich der gemessenen Streumuster mit computergenerierten Mustern vieler möglicher Strukturen rekonstruieren sie, wie sich Bindungslängen und Winkel innerhalb von Bromoform nach der Anregung entwickeln. Fortgeschrittene Analysetechniken und maschinell‑lern‑beschleunigte Simulationen helfen dabei, sich überschneidende Reaktionswege zu trennen und präzise Lebensdauern kurzlebiger Spezies zuzuweisen.
Zwei Flüssigkeiten, zwei sehr verschiedene Schicksale
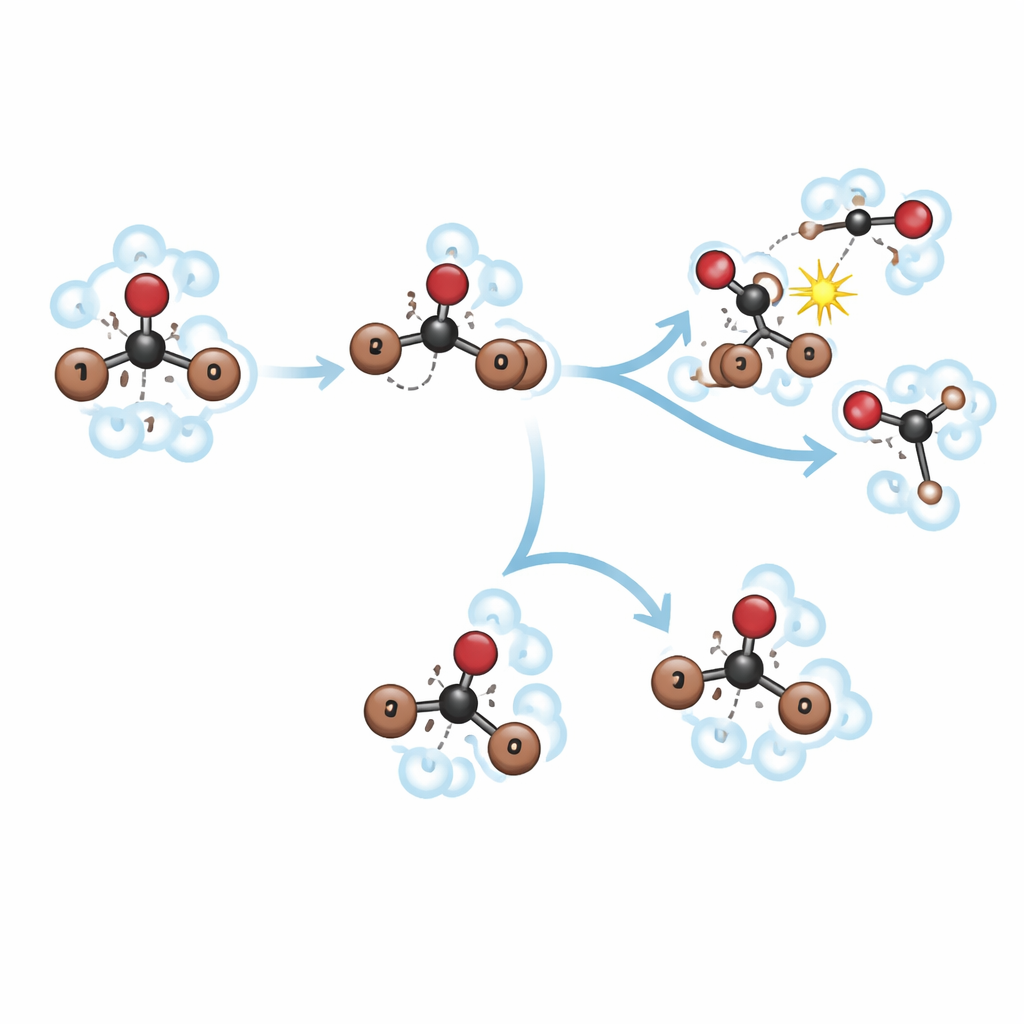
In Methanol ist der roamingartige Zwischenzustand zwar vorhanden, aber kurzlebig. Innerhalb von etwa 150 Femtosekunden bricht die anfängliche C–Br‑Bindung, es bildet sich CHBr₂ und ein roamingartiges Brom. In den folgenden ~400 Femtosekunden dehnt und biegt sich dieses heiße, vibrierende Isomer wiederholt, wodurch die Fragmente häufigen Kontakt mit benachbarten Methanol‑Molekülen haben. Statt in eine stabile, umgeformte Struktur zu entspannen, wird der Roaming‑Zustand schnell durch Methanol in einer „Methanolyse“‑Reaktion abgefangen. Dies erzeugt neue Moleküle, CH₃OCHBr₂ und HBr, während freie CHBr₂‑ und Br‑Fragmente aus einem parallelen, direkteren Spaltweg langsamer über mehrere Pikosekunden weiterreagieren. Der enge molekulare „Käfig“ des Lösungsmittels und seine reaktiven Hydroxylgruppen wirken zusammen, um Bromoform eher diesen chemischen Reaktionsweg hinzuführen als zu einem langlebigen Isomer.
Wenn die Flüssigkeit zurücktritt und Roaming zulässt
In Methylcyclohexan verändert sich die Lage dramatisch. Der gleiche UV‑Impuls erzeugt ebenfalls innerhalb von etwa 150 Femtosekunden Roaming‑Bewegung, doch die unpolare Flüssigkeit umgibt Bromoform lockerer und reagiert nicht so leicht damit. Hier haben das roamingartige Brom und das CHBr₂‑Fragment Raum, sich neu zu orientieren und in eine stabile isomere Struktur einzusinken, statt sofort mit Lösungsmittelmolekülen zu interagieren. Ein direkter Zerfall in getrennte CHBr₂‑ und Br‑Fragmente tritt weiterhin auf und konkurriert mit der Isomerbildung, doch nun überdauert das umgestellte Isomer deutlich länger. Simulationen zeigen, dass der größere, weichere Lösungsmittelkäfig in Methylcyclohexan dieses gasähnliche Roaming‑Verhalten begünstigt, während der enge, stark wechselwirkende Käfig in Methanol denselben Zwischenzustand direkt in chemische Reaktionen lenkt.
Was das für Ozon und darüber hinaus bedeutet
Die Experimente und Rechnungen zusammen zeigen, dass Roaming ein universeller früher Schritt ist, wenn Bromoform in flüssiger Umgebung ultraviolettes Licht absorbiert, aber das umgebende Lösungsmittel entscheidet, wie es weitergeht. In methanolähnlichen Umgebungen dient Roaming hauptsächlich dazu, sehr schnelle Reaktionen mit der Flüssigkeit zu treiben, was die Bildung langlebiger Isomere begrenzt und beeinflusst, wie und wann bromhaltige Produkte auftreten. In methylcyclohexanähnlichen Umgebungen fördert Roaming stattdessen ein langlebiges umgestelltes Isomer, das später Brom über andere Zeitskalen freisetzen kann. Durch das direkte Filmen dieser ultraschnellen Bewegungen zeigt die Arbeit, dass der mikroskopische Charakter von Tröpfchen, Aerosolen und anderen kondensierten Phasen die chemischen Reaktionswege ozonrelevanter Moleküle stark kontrollieren kann und so Forschenden hilft, genauere Modelle der atmosphärischen und lösungsphasigen Photochemie zu entwickeln.
Zitation: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Schlüsselwörter: Bromoform, Roaming‑Mechanismus, ultraschnelle Photochemie, Lösungsmittel‑Effekte, Ozonabbau