Clear Sky Science · de
Wettbewerbende Wasserstoffbrückenordnungen treiben Wassers anomale Oberflächenspannung
Warum die Wasseroberfläche seltsamer ist, als sie scheint
Die Wasseroberfläche erlaubt Insekten, über Teiche zu laufen, formt Regentropfen und bestimmt, wie Blasen entstehen und platzen. Wenn Forscher jedoch messen, wie „straff“ diese Oberfläche ist – also die Oberflächenspannung – stellen sie fest, dass sich Wasser beim Abkühlen überraschend eigenartig verhält, besonders wenn es unter seinen normalen Gefrierpunkt gekühlt wird. Dieser Artikel nutzt fortgeschrittene Computersimulationen, um zu zeigen, wie die verborgene Organisation der Wassermoleküle an der Oberfläche dieses lange ungelöste Rätsel erklärt.
Zwei verborgene Typen flüssigen Wassers
Obwohl wir Wasser als eine einfache, einheitliche Flüssigkeit erleben, können sich seine Moleküle lokal in zwei gegensätzlichen Mustern anordnen. Eine Anordnung ist dichter und ungeordneter; die Autorinnen und Autoren bezeichnen diesen Zustand als ρ-Zustand. Die andere ist weiter und symmetrischer, wobei jedes Molekül grob in einer vierfachen, tetraedrischen Anordnung umgeben ist; das nennt sich S-Zustand. Frühere Arbeiten legten nahe, dass das Gleichgewicht zwischen diesen beiden lokalen Mustern viele der ungewöhnlichen Volumeneigenschaften von Wasser erklärt. Hier fragen die Autorinnen und Autoren, wie dieses Zwei-Zustände-Bild an der Luft–Wasser-Grenzfläche wirkt, wo die Oberflächenspannung entsteht.
Wie die Oberfläche Moleküle ausrichtet
An der Grenze zwischen Luft und Wasser wirken die Moleküle nicht mehr gleichmäßig in alle Richtungen. Diese gebrochene Symmetrie begünstigt ρ-Zustand-Moleküle, deren Wasserstoffatome und molekulare Dipole sich leicht in eine bevorzugte Richtung neigen können. Simulationen zeigen, dass sich bei Zimmertemperatur und etwas darunter die oberste Schicht des Wassers mit diesen ausgerichteten ρ-Zustand-Molekülen füllt, während S-Zustand-Moleküle etwas unterhalb der Oberfläche und im Volumen häufiger vorkommen. Weil ρ-Zustand-Moleküle stark ausgerichtet sind, erzeugen sie ein Ungleichgewicht der Kräfte – eine Spannungsanisotropie –, die eine relativ hohe Oberflächenspannung im Vergleich zu gewöhnlichen Flüssigkeiten wie Benzol verursacht.
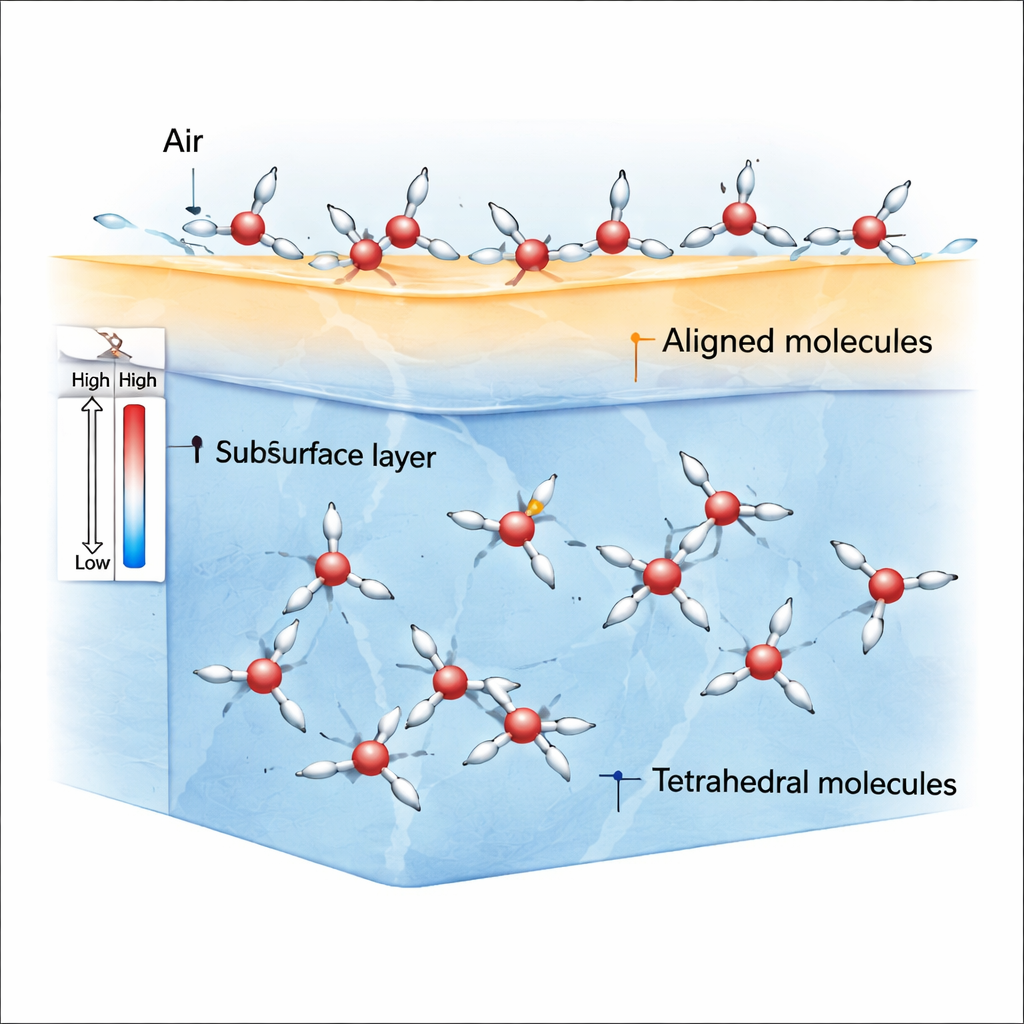
Warum Abkühlung zuerst das Oberflächenspannen verlangsamt, dann beschleunigt
Bei den meisten einfachen Flüssigkeiten führt Abkühlung zu einer stetigen Straffung der Oberfläche, sodass die Oberflächenspannung nahezu linear ansteigt. Wasser macht das nur bei höheren Temperaturen. Beim Abkühlen bis etwa –0,15 °C (275 K) beginnt der Anstieg der Oberflächenspannung zu verlangsamen. Die Simulationen zeigen, dass diese Verlangsamung daher kommt, dass die ρ-Zustand-Moleküle an der Oberfläche bereits so weit ausgerichtet sind, wie sie es können; weiteres Abkühlen ändert ihren Beitrag kaum. Gleichzeitig bleiben die S-Zustand-Moleküle in der Unterschicht überwiegend zufällig orientiert und tragen wenig zur Erhöhung der Oberflächenspannung bei. Das Nettoergebnis ist eine Art Plateau: Die Temperatur sinkt weiter, aber die Oberflächenspannung wächst nur noch schleppend.
Tiefes Überkühlen löst eine zweite Straffung aus
Wird Wasser deutlich weiter abgekühlt, weit unter seinen normalen Gefrierpunkt in das tief überkühlte Regime (etwa 250 K und darunter), ändert sich sein Verhalten erneut. Der Anteil an S-Zustand-, tetraedrischen Strukturen steigt stark an, sogar nahe der Oberfläche. Entscheidenderweise zeigen diese S-Zustand-Moleküle dann keine zufällige Ausrichtung mehr. Ihre Dipole beginnen sich entlang der Richtung senkrecht zur Oberfläche zu orientieren, angetrieben durch Wechselwirkungen zwischen benachbarten Moleküldipolen und durch einen Bereich negativer Spannung direkt unter der Oberfläche. Sobald das passiert, stärkt das S-Zustand-Wasser, das zuvor die Oberflächenspannung abgemildert hatte, diese nun. Dieser zusätzliche, geordnete Beitrag bewirkt einen erneuten, schnelleren Anstieg – die „reentrante“ Zunahme der Oberflächenspannung bei niedrigen Temperaturen.
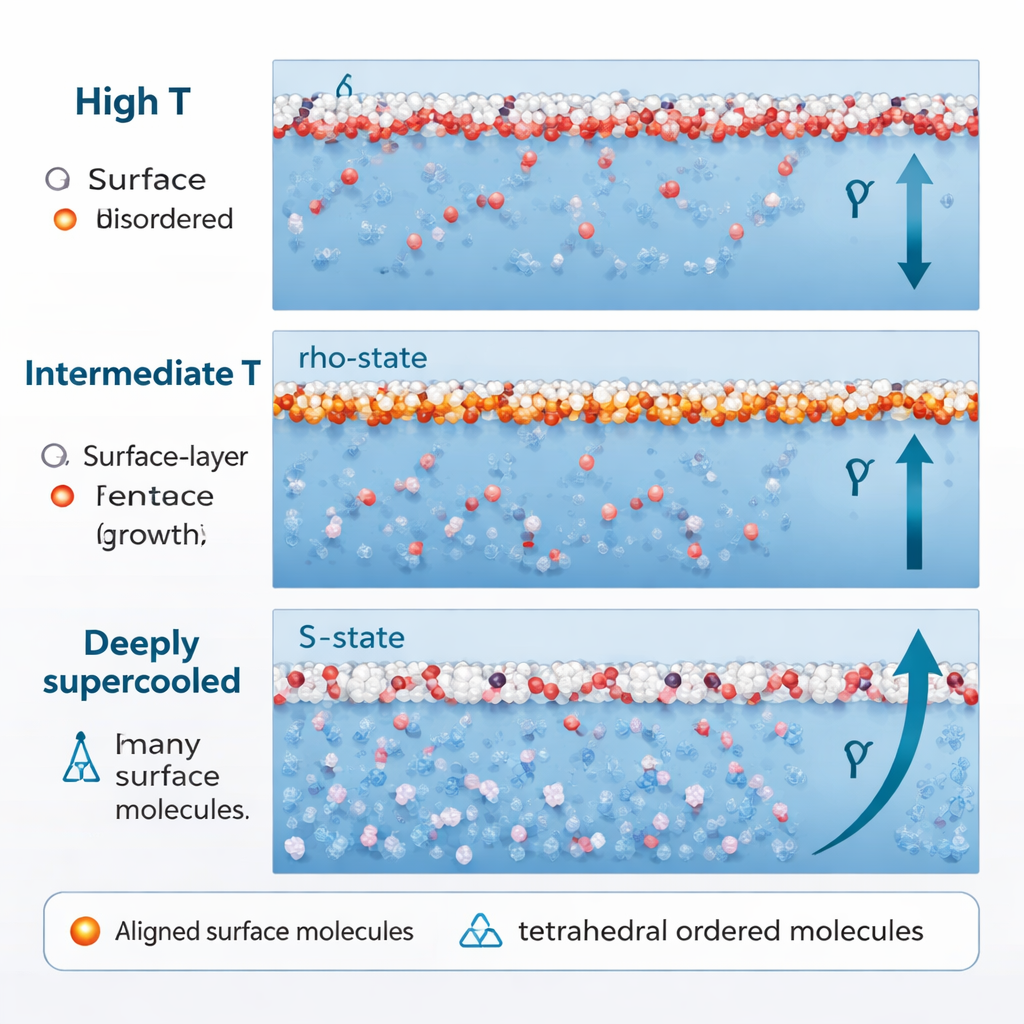
Von Oberflächenrätseln zu Eis und darüber hinaus
Die gleichen tetraedrischen S-Zustand-Cluster, die die Oberfläche bei niedrigen Temperaturen versteifen, ähneln auch frühen Bausteinen bestimmter Eisformen, und die Simulationen finden sie in erhöhter Konzentration nahe der Grenzfläche. Das bedeutet, dass die Luft–Wasser-Grenze als Wiege für Eisbildung wirken kann, was hilft zu erklären, warum Gefrieren oft an Oberflächen beginnt. Allgemeiner liefert die Arbeit eine konkrete, molekulare Verbindung zwischen der Anordnung und Orientierung von Wassermolekülen und der Stärke des nach innen wirkenden Oberflächenzugs. Dieses Struktur–Mechanik-Bild löst nicht nur die ungewöhnliche Temperaturkurve der Oberflächenspannung von Wasser, sondern bietet auch eine Straßenkarte, um interfaciale Phänomene in anderen netzwerkbildenden Flüssigkeiten zu verstehen und zu steuern – vom überkühlten Wasser in Wolken bis zu Materialien, die in Technik und Biologie verwendet werden.
Zitation: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Schlüsselwörter: Oberflächenspannung von Wasser, Wasserstoffbrücken, überkühltes Wasser, Flüssigkeitsstruktur, Eiskeimbildung