Clear Sky Science · de
STING wirkt mit TOX zusammen und unterdrückt die HO-1-Expression, um Ferroptose in tumorinfiltrierenden CD8+-T-Zellen auszulösen und die Immuntherapie zu schwächen
Warum diese Forschung für die Krebsbehandlung wichtig ist
Moderne Krebsimmuntherapien wirken, indem sie die körpereigenen Killer-T‑Zellen freisetzen, doch viele Tumore finden weiterhin Wege, diese Zellen auszuschalten. Diese Studie deckt einen versteckten Selbstzerstörungsschalter in CD8+-"Killer"-T‑Zellen auf, den Tumore ausnutzen, und zeigt, wie das Abschalten dieses Schalters die Wirksamkeit der Immuntherapie deutlich steigern kann.
Ein verborgener Todesweg in tumorkämpfenden T‑Zellen
Innerhalb eines Tumors sollen CD8+-T‑Zellen Krebszellen aufspüren und zerstören. Stattdessen sind sie oft selten, träge und kurzlebig. Die Autoren konzentrierten sich auf zwei Moleküle in T‑Zellen—STING, einen Sensor für DNA-Schäden, und TOX, ein Protein, das mit T‑Zell-Erschöpfung in Verbindung steht. Sie erzeugten Mäuse, in denen CD8+-T‑Zellen entweder STING, TOX oder beides nicht hatten, und setzten verschiedene Tumorarten ein. Überraschenderweise räumten Mäuse, deren T‑Zellen entweder STING oder TOX fehlten, die Tumore deutlich besser ab. Diese Tumore wuchsen langsamer, enthielten viel mehr CD8+-T‑Zellen, und diese Zellen produzierten größere Mengen an krebsbekämpfenden Molekülen wie Interferon‑gamma und Granzyme B. Das deutete auf ein internes Programm hin, das T‑Zellen innerhalb von Tumoren still sabotiert.
Wie eisengetriebener Zelltod die Immunität schwächt
Durch die Untersuchung der Genaktivität in tumorinfiltrierenden T‑Zellen fanden die Forschenden heraus, dass normale T‑Zellen innerhalb von Tumoren für eine spezielle Form des Zelltods namens Ferroptose prädisponiert waren. Im Gegensatz zur Apoptose wird Ferroptose durch Eisenüberladung und die Ansammlung beschädigter Lipide in Zellmembranen ausgelöst. In gewöhnlichen CD8+-T‑Zellen, die Tumorzellen ausgesetzt waren, wurden Gene hochreguliert, die Eisenansammlung und Lipidschäden fördern, während schützende Gene heruntergefahren wurden. Im Gegensatz dazu zeigten STING‑ oder TOX‑defiziente T‑Zellen das entgegengesetzte Muster: Sie exprimierten mehr der schützenden Enzyme HO‑1 und GPX4, hatten niedrigere Eisenwerte, weniger Lipidperoxidation, gesündere Mitochondrien und widerstanden dem ferroptotischen Tod. In vitro-Tests bestätigten, dass das chemische Blockieren der Ferroptose normale T‑Zellen am Leben erhält, während das Entfernen von STING oder TOX sie von Natur aus resistent machte.
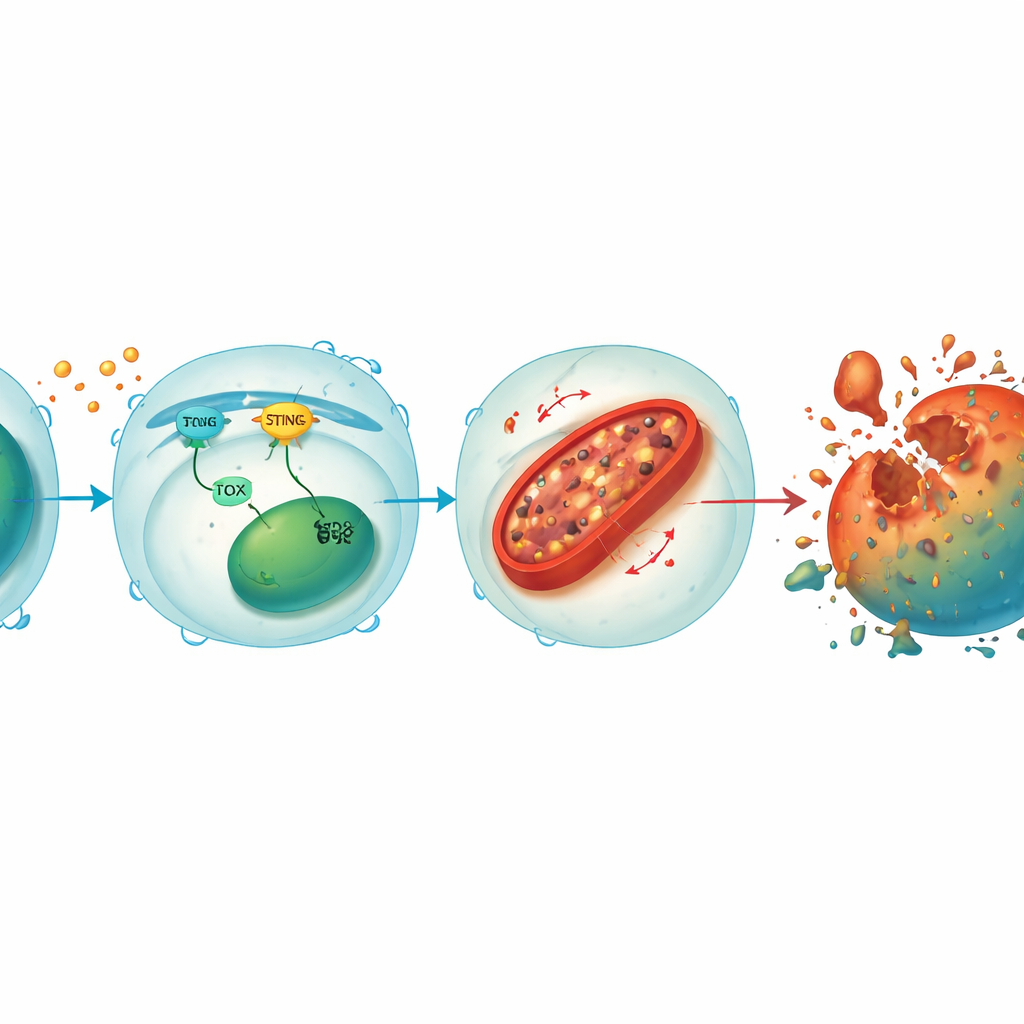
Eine Schleife, die Stresssignale mit mitochondrialen Schäden verbindet
Bei genauerer Betrachtung entdeckte das Team, dass STING und TOX eine sich verstärkende Schleife innerhalb von CD8+-T‑Zellen bilden. Wenn Tumor‑ oder Virussignale STING aktivieren, löst das nachgeschaltete Faktoren aus, die TOX erhöhen, und TOX wiederum trägt zur Aufrechterhaltung der STING-Aktivität bei. Zusammen unterdrücken sie HO‑1, ein Enzym, das normalerweise hilft, zelluläres Eisen zu kontrollieren. Wird HO‑1 heruntergedrückt, sammelt sich Eisen in den Mitochondrien—den Kraftwerken der Zelle—an, was zu hohen Mengen reaktiver Sauerstoffmoleküle und zur Oxidation von Membranlipiden führt. Diese mitochondriale Schädigung entleert die Energieproduktion und drängt die T‑Zelle schließlich in die Ferroptose. Die Wiederherstellung von STING oder TOX in Knockout‑T‑Zellen brachte Eisenüberladung und Zelltod zurück, während eine weitere Absenkung von HO‑1 selbst die geschützten T‑Zellen wieder verwundbar machte, was HO‑1 als zentrales Bremselement dieses zerstörerischen Weges hervorhebt.
Wie tumoreigenes Laktat den Auslöser betätigt
Das tumoröse Mikroenvironment ist reich an Laktat, einem Nebenprodukt des veränderten Stoffwechsels von Krebs. Die Studie zeigt, dass dieses Laktat nicht nur metabolischer Abfall ist—es hilft aktiv mit, den Ferroptose-Schalter in T‑Zellen umzulegen. Im Vergleich zu anderen Zellen waren CD8+-T‑Zellen besonders empfindlich gegenüber Laktat. Wenn Laktat über spezifische Transporter in die Zellen gelangte, verursachte es Eisenansammlung, Schrumpfung der Mitochondrien, Verlust mitochondrialer DNA und mehr oxidative Schäden. Gleichzeitig steigerte Laktat die Aktivität von STING und TOX und unterdrückte HO‑1 weiter. T‑Zellen ohne STING oder TOX waren wesentlich widerstandsfähiger gegen laktatinduzierte Schäden. Die Blockade eines wichtigen Laktattransporters mit einem Wirkstoff (AZD3965) schützte CD8+-T‑Zellen in Mäusen vor Ferroptose, erhöhte ihre Präsenz in Tumoren und verlangsamte das Tumorwachstum—ein Effekt, der dem Vorteil durch genetisches Entfernen von STING in T‑Zellen ähnelt.
Eine Verwundbarkeit in einen therapeutischen Vorteil verwandeln
Diese mechanistischen Einsichten haben praktische Konsequenzen. Als die Forschenden adoptive Zelltherapie anwandten—indem sie Mäusen im Labor aktivierte T‑Zellen infundierten—stellten sie fest, dass T‑Zellen, die so verändert waren, dass sie kein STING oder TOX hatten, eine deutlich stärkere Tumorkontrolle erzielten als normale T‑Zellen. Darüber hinaus führte die Kombination dieser „ferroptose-resistenten“ T‑Zellen mit bestehenden Therapien wie PD‑1‑ oder TIM‑3‑Checkpoint‑Inhibitoren, Cisplatin‑Chemotherapie oder einem STING-aktivierenden Wirkstoff zu deutlich besserer Tumorverkleinerung als irgendeine Einzeltherapie. Schließlich waren in Tumorproben von Patientinnen mit Zervixkarzinom höhere TOX‑ und niedrigere HO‑1‑Werte in tumorinfiltrierenden Lymphozyten mit schlechterem Überleben verbunden, was nahelegt, dass dieser Signalweg auch klinische Ergebnisse beim Menschen beeinflusst.
Was das für die zukünftige Krebsversorgung bedeutet
Kurz gesagt zeigt die Studie, dass Tumore unsere wirksamsten Krebsbekämpfer–T‑Zellen von innen heraus „rosten“ lassen können, indem sie eine eisengetriebene Form des Zelltods forcieren. Ein Laktat–STING–TOX‑Kreislauf reduziert den Schutz durch HO‑1, schädigt Mitochondrien und führt zur Ferroptose, wodurch die Reihen effektiver CD8+-T‑Zellen gelichtet werden. Das Unterbrechen dieses Kreislaufs—etwa durch das Engineering von T‑Zellen ohne STING oder TOX, die Stärkung von HO‑1 oder die Blockade des Laktateintritts—hält T‑Zellen am Leben, energiegeladen und einsatzbereit. Diese Arbeit weist den Weg zu nächsten Generationen von Immuntherapien, die metabolische und genetische Anpassungen von T‑Zellen mit bestehenden Medikamenten kombinieren, um Resistenz zu überwinden und dauerhaftere Krebskontrolle zu ermöglichen.
Zitation: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Schlüsselwörter: Krebsimmuntherapie, CD8-T-Zellen, Ferroptose, tumoröses Mikroenvironment, STING-TOX-HO-1-Signalweg