Clear Sky Science · de
Seq-Scope-eXpanded: räumliche Omics jenseits der optischen Auflösung
Zellen schärfer sehen
Unser Körper besteht aus einer Vielzahl winziger Zellen, jede erfüllt zahlreiche Aktivitäten, die wir selbst mit leistungsfähigen Mikroskopen oft nicht vollständig erfassen können. Dieser Artikel stellt Seq-Scope-X vor, eine Technologie, die Forschenden erlaubt, die inneren Abläufe von Geweben mit beispielloser Klarheit zu untersuchen und zu kartieren, welche Gene und Proteine an welchen präzisen Orten innerhalb und zwischen Zellen aktiv sind. Ein solches Detailniveau könnte unsere Studien zur Entwicklung, zum Immunsystem und zu Erkrankungen wie Krebs oder Leberschädigung verändern.
Warum Moleküle an ihrem Ort abbilden?
Zellen funktionieren nicht isoliert: sie leben in Nachbarschaften, bilden Schichten und spezialisieren sich je nach Lage. Traditionelle Gen-Sequenzierverfahren zerstückeln Gewebe und verlieren so diesen räumlichen Kontext. Neuere „räumliche Omics“-Werkzeuge behalten Moleküle am Ort, doch bisher gab es einen Kompromiss. Bildgebungsbasierte Methoden liefern sehr feine Details, erfassen aber meist nur eine begrenzte Anzahl von Genen. Sequenzierbasierte Ansätze lesen nahezu jedes Gen gleichzeitig, verwischen dabei aber feine Merkmale und verteilen Signale oft über mehrere Mikrometer — mehr als viele subzelluläre Strukturen groß sind. Die Autorinnen und Autoren wollten diese Lücke schließen: die umfassende, unvoreingenommene Erfassung durch Sequenzierung bewahren und gleichzeitig die Schärfe moderner Mikroskope erreichen oder übertreffen.
Gewebe dehnen, um optische Grenzen zu überwinden
Die Kernidee von Seq-Scope-X ist verblüffend einfach: man vergrößert das Gewebe selbst so, dass ursprünglich winzige Strukturen leichter auflösbar werden. Das Team verankert zunächst RNA-Moleküle — oder spezielle DNA-Tags, die an Antikörper gekoppelt sind — in ein weiches Hydrogel, das um den Gewebeschnitt herum aufgebaut wird. Anschließend wird das ursprüngliche Gewebe abgebaut und das Gel in einer salzhaltigen Lösung aufgequollen, wodurch alles etwa dreifach physisch gestreckt wird, während die relativen Positionen weitgehend erhalten bleiben. Dieses expandierte Gel wird auf einen ultradichten Sequenzierchip gelegt, der mit Fangsonden beschichtet ist. Durch kontrolliertes Erhitzen werden die verankerten Moleküle aus dem Gel freigesetzt und auf dem Chip zurückgebunden, der anschließend sequenziert werden kann, um zu zeigen, welche Gene oder Proteine an jedem winzigen Koordinatenpunkt vorhanden waren. 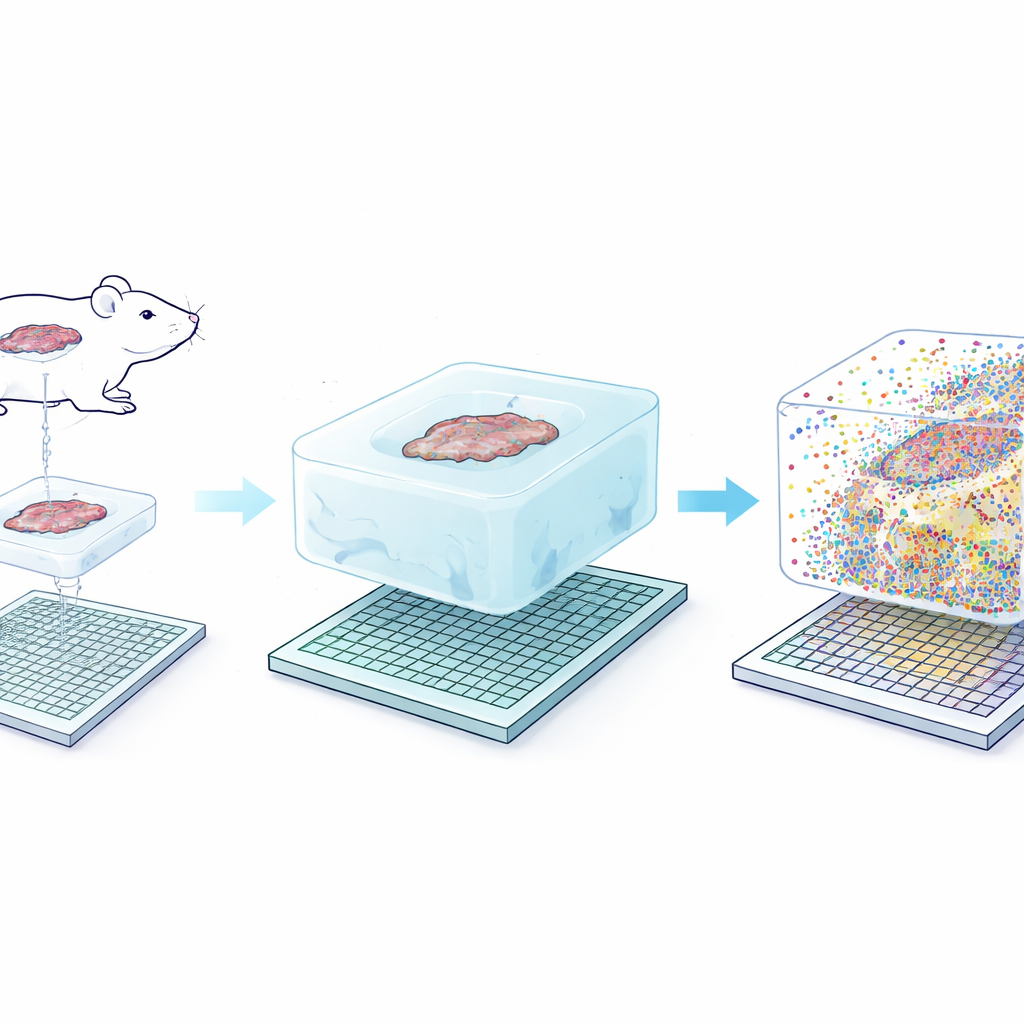
Von verschwommenen Signalen zu subzellulären Karten
Als die Forschenden Seq-Scope-X auf Mäuseleber anwendeten, stellten sie fest, dass die Methode die räumliche Auflösung von etwa 0,6 Mikrometern auf rund 0,2 Mikrometer verbesserte und die Zahl messbarer Positionen pro Quadratmillimeter nahezu verzehnfachte. Praktisch bedeutete das: Was zuvor wie unscharfe Signalwolken aussah, löste sich nun in klare Umrisse einzelner Zellen auf. Noch auffälliger war, dass sich RNA-Cluster, die noch nicht vollständig verarbeitet waren (unspliced), eng mit den Zellkernzentren deckten, während reife RNA (spliced) das umgebende Zytoplasma nachzeichnete. Dadurch konnten die Autorinnen und Autoren Zellgrenzen allein anhand von RNA definieren und für nahezu jeden Hepatozyten des Gewebes nukleäre und zytoplasmatische Genprofile getrennt auslesen — etwas, das frühere sequenzierbasierte Methoden nur angedeutet hatten.
Zellen mit geteilter Identität
Mit dieser neuen Klarheit entdeckte das Team eine unerwartete Form molekularer „Doppelleben“ innerhalb von Leberzellen. Entlang des bekannten Gradienten von den Blutgefäßen an der Portalseite des Leberläppchens zu denen an der Zentralseite spezialisieren sich Hepatozyten auf unterschiedliche Stoffwechselaufgaben. Seq-Scope-X zeigte, dass in vielen Zellen das Muster der Gene im Zellkern nicht mit dem Muster im umgebenden Zytoplasma übereinstimmte. Ungefähr ein Drittel der Hepatozyten schien ein nukleäres Profil zu besitzen, das zu einer Zone passte, während das zytoplasmatische Profil einer benachbarten Zone entsprach. Unabhängige bildgebende Verfahren, darunter MERFISH und Einzelmolekül-RNA-Fluoreszenztests, bestätigten, dass einzelne Transkripte entweder im Kern oder im Zytoplasma konzentriert sein können. Zusammen deuten diese Befunde darauf hin, dass Hepatozyten ihre metabolischen Rollen dynamisch über die Zeit verschieben können, wobei der Zellkern auf einen zukünftigen Zustand vorbereitet, das Zytoplasma jedoch den aktuellen widerspiegelt. 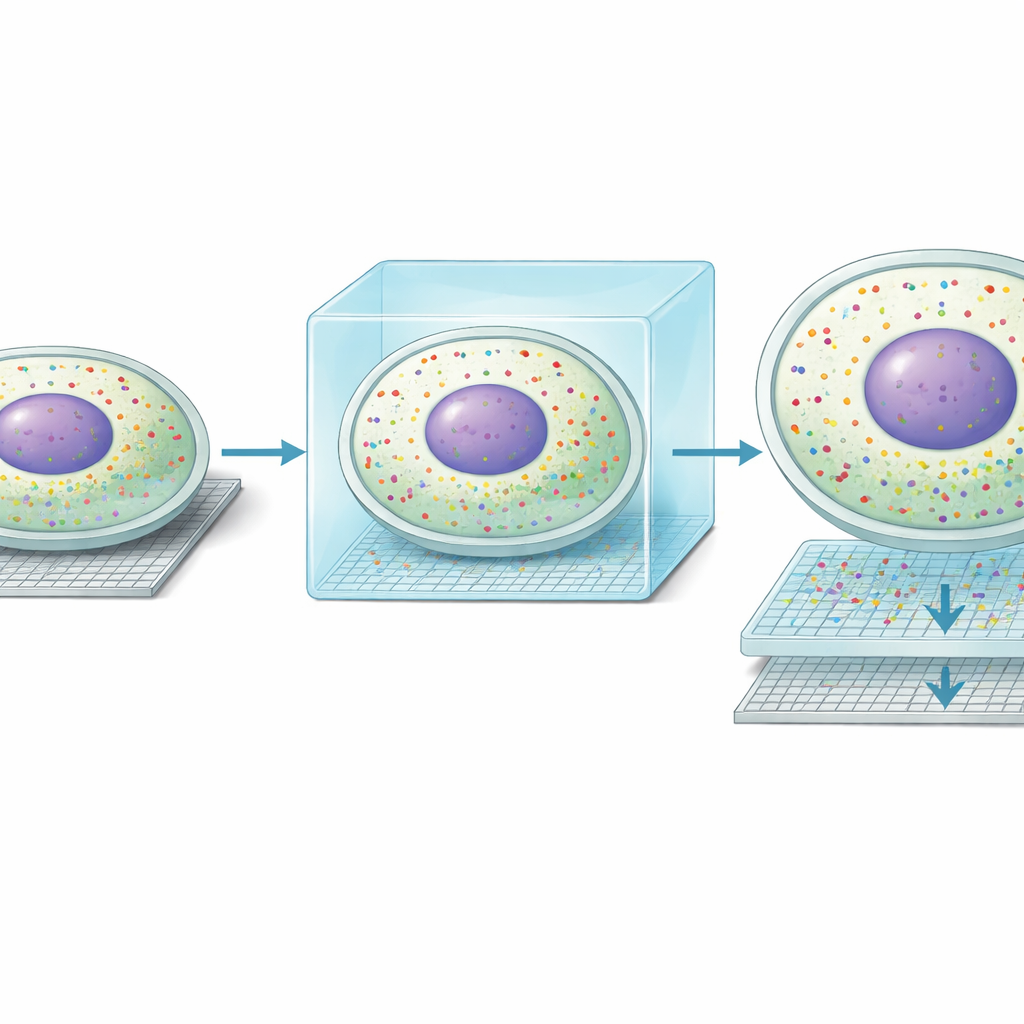
Über die Leber hinaus: Gehirn, Darm und Immungewebe
Die Autorinnen und Autoren prüften anschließend, ob Seq-Scope-X auch in anderen Organen funktioniert. Im Gehirn unterschied es sauber verschiedene Neuronentypen und Stützzellen und zeigte subzelluläre RNA-Muster um Zellkerne. Im Kolon löste es unterschiedliche Becherzellsubtypen und Schichten von Kolonozyten entlang der Krypten-zu-Oberfläche-Achse auf und erfasste erneut nukleäre Signaturen. Vielleicht am eindrücklichsten passte das Team die Methode auf Proteine an, indem es DNA-barcode-tragende Antikörper in Mäusesplen und menschlicher Tonsille einsetzte. Seq-Scope-X konnte gleichzeitig über hundert verschiedene zelloberflächenmarker in Einzelzellauflösung kartieren und eng gepackte T- und B-Zell-Subsets sowie myeloide Zellen unterscheiden. Durch den Wechsel zu einer stärker expandierbaren Gelchemie trieben sie die effektive Auflösung in Richtung echten Nanomaßstabs, während die Gewebearchitektur ausreichend gut erhalten blieb, um detaillierte Karten zu erlauben.
Was das für die Zukunft bedeutet
Seq-Scope-X zeigt, dass das physische Vergrößern von Geweben vor der Sequenzierung langjährige Auflösungsgrenzen überwinden kann und nahezu mikroskopische Details liefert, während gleichzeitig Tausende Gene oder Protein-Tags auf einmal ausgelesen werden. Für Laien bedeutet das: Forschende können jetzt „molekulare Atlanten“ erstellen, die nicht nur sagen, welche Zellen wo sind, sondern auch zeigen, was in verschiedenen Teilen jeder Zelle vor sich geht. Solche Karten könnten erklären helfen, wie Gewebe auf Verletzungen reagieren, wie Immunzellen in lymphatischen Organen und Tumoren organisiert sind oder wie subtile Verschiebungen innerhalb von Zellen auf bevorstehende Erkrankungen hinweisen. Zwar sind noch Verbesserungen nötig, um die Abdeckung zu skalieren und einige Färbepanels zu optimieren, doch Seq-Scope-X eröffnet ein mächtiges neues Fenster auf die mikroskopischen Landschaften, die Gesundheit und Krankheit zugrunde liegen.
Zitation: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Schlüsselwörter: räumliche Transkriptomik, Gewebeerweiterung, Single-Cell-Omics, räumliche Proteomik, Leberzonierung