Clear Sky Science · de
Vom Mikrobiom abgeleitetes IPA schützt vor Kolitis, indem es die intestinale HMGCS2-vermittelte Ketogenese reguliert, um die Schleimhautheilung zu erleichtern
Warum Darmbakterien für einen geschädigten Darm wichtig sind
Wenn die Darmschleimhaut beschädigt ist, wie bei entzündlichen Darmerkrankungen (IBD) oder nach harten medizinischen Eingriffen, muss der Körper diese innere „Haut“ schnell reparieren, damit schädliche Stoffe nicht ins Blut gelangen. Diese Studie zeigt, wie ein einzelnes Molekül, das von nützlichen Darmbakterien gebildet wird, dem Darm dabei helfen kann, sich selbst zu heilen, und weist auf neue Behandlungsansätze für chronische Darmerkrankungen hin, ohne das Immunsystem breit zu unterdrücken.
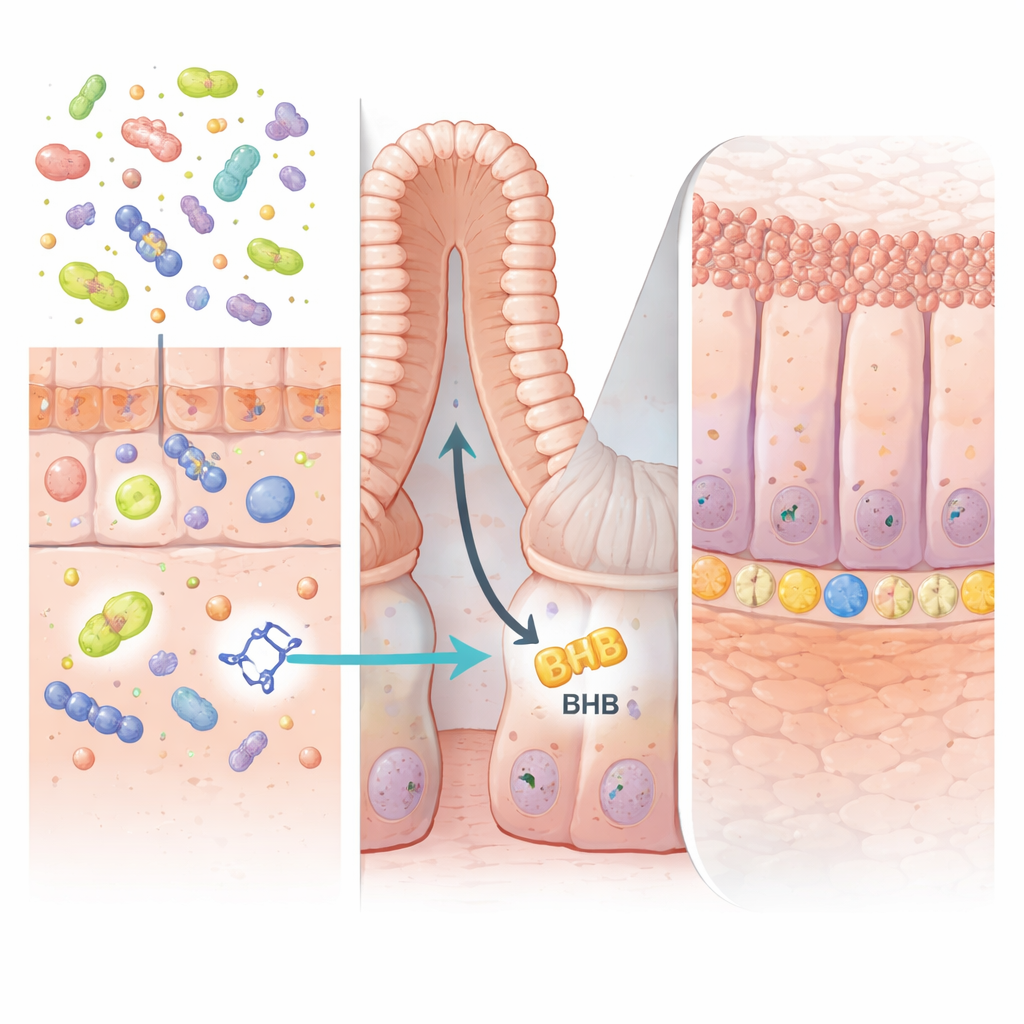
Ein hilfreiches Signal freundlicher Mikroben
Die Forschenden begannen damit, chemische Fingerabdrücke aus Stuhlproben von Menschen mit IBD und gesunden Freiwilligen sowie aus mehreren Mausmodellen der Kolitis zu vergleichen. Unter Hunderten von Molekülen stach eines hervor: Indol-3-propionsäure (IPA), ein Abbauprodukt der diätischen Aminosäure Tryptophan, das von bestimmten Darmbakterien produziert wird. Die IPA-Spiegel waren bei Menschen mit Morbus Crohn und bei Mäusen mit Kolitis konsistent niedriger als bei gesunden Vergleichspersonen. Das deutete darauf hin, dass der Verlust von IPA Teil dessen sein könnte, was schiefgeht, wenn die Darmschleimhaut entzündet ist und nicht richtig repariert wird.
Stärkung der schützenden Darmbarriere
Um zu prüfen, ob IPA nur ein Begleitmarker der Krankheit ist oder tatsächlich schützt, verabreichte das Team Mäusen IPA, bevor verschiedene Arten von Darmverletzungen ausgelöst wurden, darunter chemische Kolitis und strahlenbedingte Schäden. Mäuse, die angemessene Dosen IPA erhielten, hatten längere, gesündere Kolons, weniger entzündliche Veränderungen im Mikroskop und eine dickere Schleimschicht mit dichteren Zellverbindungen. Sie wiesen weniger ausgetretene Entzündungsmarker auf und mehr Becherzellen, die den schützenden Schleim produzieren. Wichtig ist, dass diese Vorteile auch bei keimfreien Mäusen ohne residenten Mikrobiom beobachtet wurden, was zeigt, dass IPA, sobald es vorhanden ist, direkt auf die Darmschleimhaut wirken kann, ohne andere Mikroben zu benötigen.
Stammzellen mit einer speziellen Energieart versorgen
Der Schlüssel zur Wirkung von IPA lag tief in den intestinalen „Krypten“, den winzigen Taschen, in denen die Stammzellen sitzen und die Schleimhaut ständig erneuern. Die Autoren zeigten, dass IPA ein Protein namens PPARα in intestinalen Epithelzellen aktiviert. Dies steigert wiederum die Produktion eines Enzyms namens HMGCS2, das die Ketogenese antreibt — den Prozess der Herstellung des energiereichen Moleküls β‑Hydroxybutyrat (BHB). Erhöhte BHB-Werte in der Darmwand stimulierten LGR5-positive Stammzellen zur Expansion und zur schnelleren Regeneration von geschädigtem Gewebe. Wenn das HMGCS2-Enzym oder PPARα selektiv aus intestinalen Zellen von Mäusen entfernt wurde, konnte IPA die Stammzellaktivität oder den Schutz vor Kolitis nicht mehr steigern, was bestätigt, dass dieser ketonproduzierende Weg essenziell ist.
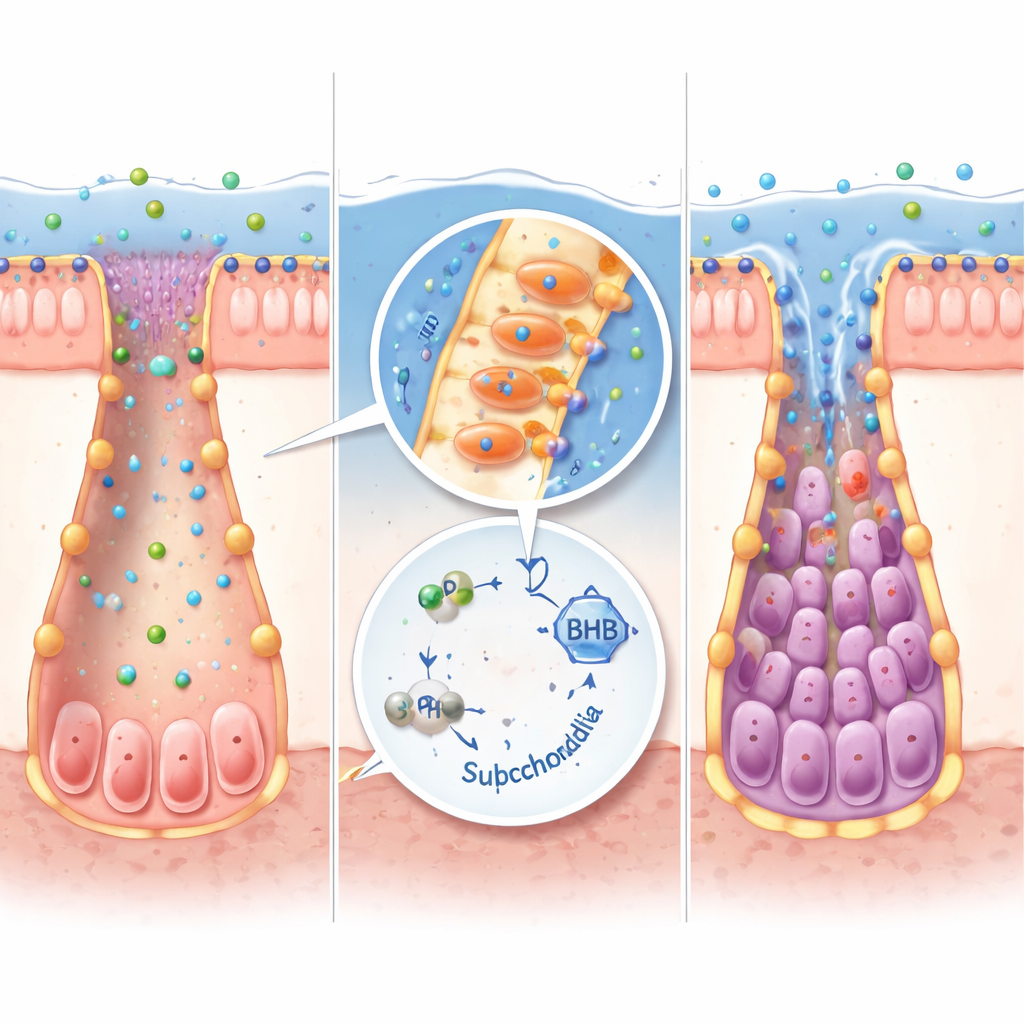
Von bakteriellen Fabriken zu menschlichem Gewebe
Nicht alle Darmbakterien können IPA herstellen. Durch die Reanalyse großer Mikrobiom-Datensätze identifizierten die Forschenden Peptostreptococcus russellii als einen wichtigen IPA-Produzenten, der in mehreren IBD-Kohorten vermindert ist. In Laboransätzen wandelte dieses Bakterium Tryptophan effizient in IPA um. Als keimfreie Mäuse mit P. russellii kolonisiert wurden, stiegen ihre IPA-Spiegel, ketonproduzierende Gene wurden hochreguliert, Stammzellmarker nahmen zu und die Schwere der Kolitis nahm im Vergleich zu Mäusen, die eine generische mikrobielle Transplantation erhielten, ab. Derselbe IPA–Keton-Weg funktionierte in Miniatur-Darmorganoiden, die aus Maus- und menschlichem Gewebe gezüchtet wurden: Die Zugabe von IPA oder BHB half den Stammzellen, sich nach entzündlichen Schäden zu erholen, während proinflammatorische Signale gedämpft wurden.
Was das für künftige Behandlungen bedeuten könnte
Zusammengefasst skizziert die Arbeit eine einfache, aber kraftvolle Abfolge: Bestimmte Darmbakterien wandeln diätisches Tryptophan in IPA um; IPA aktiviert einen Stoffwechselschalter in intestinalen Zellen; dieser Schalter fördert die Produktion von BHB; und BHB belebt wiederum Stammzellen, die die Darmschleimhaut wiederaufbauen. Für Menschen mit IBD oder anderen Zuständen, die die intestinale Barriere schädigen, könnten Therapien, die IPA wiederherstellen oder seine Effekte sicher nachahmen — durch Ernährung, gezielte Probiotika oder designte Wirkstoffe — eine echte Schleimhautheilung fördern, ohne das Immunsystem breit zu unterdrücken. Während weitere Studien an Patienten erforderlich sind, bietet diese Achse aus Mikrobe, Metabolit und Stammzelle einen vielversprechenden neuen Ansatz, den Darm von innen heraus zu reparieren.
Zitation: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Schlüsselwörter: Darmmikrobiom, intestinale Stammzellen, entzündliche Darmerkrankung, mikrobielle Metaboliten, Schleimhautheilung