Clear Sky Science · de
Benchmarking der EGF-Signalweg-Inferenz mit Phosphoproteomik und Kinasen-Substrat-Interaktionen
Warum das über das Labor hinaus wichtig ist
Unsere Zellen hören ständig auf Signale aus ihrer Umgebung und reagieren darauf. Eines der wichtigsten dieser Signale ist der epidermale Wachstumsfaktor (EGF), der hilft zu steuern, wie Zellen wachsen, sich teilen und überleben. Gerät dieses Kommunikationssystem aus dem Gleichgewicht, kann es Krebs und andere Krankheiten antreiben. Die Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wenn wir heutige leistungsfähige Messtechnologien und Computermodelle einsetzen, wie viel besser können wir den EGF-Signalweg wirklich verstehen als in den Lehrbuchdiagrammen?
Von geraden Strichen zu realen Schaltplänen
Traditionelle „Signalwege“ werden oft als ordentliche, fast lineare Ketten von Proteinen gezeichnet, die eine Botschaft von der Zelloberfläche zum Zellkern weitergeben. Diese Karten entstanden über Jahrzehnte mit langsamen, zielgerichteten Experimenten, die jeweils nur wenige Proteine betrachteten. Die Autoren argumentieren, dass uns das eine eingeschränkte, vom Straßenlaternen-Effekt geprägte Sicht hinterlassen hat: Wir wissen viel über die wenigen Proteine, die leicht zu untersuchen waren, und deutlich weniger über das größere Netz von Verbindungen, das in echten Zellen wahrscheinlich existiert.
Beim Lauschen an tausenden molekularer Schalter zugleich
Um über diese begrenzte Sicht hinauszukommen, nutzte das Team Phosphoproteomik, eine Massenspektrometrie-Technik, die in einem einzigen Experiment Zehntausende winziger chemischer Markierungen, sogenannter Phosphatgruppen auf Proteinen, verfolgen kann. Diese Markierungen werden von Enzymen namens Kinasen angebracht und wirken als schnelle Ein-/Aus-Schalter für die Signalübertragung. Die Forschenden stellten zunächst die umfassendsten Karten „wer-kann-wen-phosphorylieren“ zusammen, indem sie drei Informationsquellen zusammenführten: kuratierte Befunde aus der Literatur, Vorhersagen eines KI-Modells, das Proteinsequenzen liest, und groß angelegte experimentelle Screens zu Kinasepräferenzen. Dadurch wurde die Abdeckung bekannter oder vermuteter Kinase–Substrat-Beziehungen von etwa 5 % der messbaren Stellen auf bis zu 70–80 % ausgeweitet.
Stresstest der EGF-Signalgebung über viele Experimente
Als Nächstes konzentrierten sie sich auf die EGF-Antwort, einen klassischen Signalweg und wichtigen Faktor bei Lungen-, Brust-, Haut- und Hirntumoren. Die Gruppe kombinierte drei hochmoderne veröffentlichte Datensätze mit drei neuen, sehr tiefgehenden zeitaufgelösten Messungen in nierenabgeleiteten Zellen sowie zwei Kontrollstudien mit anderen Stimuli. Zusammen maßen diese Experimente über 40.000 Phosphorylierungsstellen pro Datensatz und verfolgten, wie diese Minuten nach EGF-Stimulation anstiegen oder abfielen. Während die allgemeinen Muster zwischen Zelltypen und Technologien etwas variierten, wurden Schlüsselpunkte der Phosphorylierung im EGF-Weg wiederholt aktiviert, was bestätigt, dass das Kernsignal selbst über verschiedene Experimente hinweg robust ist.
Wiederaufbau der verborgenen Kommunikation zwischen Kinasen
Nachdem sie abgeschätzt hatten, welche Kinasen aktiver oder weniger aktiv wurden, versuchten die Autoren, die zugrundeliegende „Unterhaltung“ zwischen ihnen nachzubilden: Welche Kinasen aktivieren oder beeinflussen wahrscheinlich welche anderen? Sie wandelten ihre Kinase–Substrat-Karten in Kinase–Kinase-Netzwerke um und wendeten drei rechnerische Strategien an, von einfachen Rangfolgenschemata bis zu einem komplexeren Ansatz, der das Ergebnis dazu zwingt, wie ein gerichteter Baum mit der EGF-Rezeptorwurzel auszusehen. Die abgeleiteten Wege verglichen sie mit mehreren Arten von „Ground Truth“: einer sorgfältig kuratierten EGF-Karte aus einer Datenbank, groß angelegten Experimenten mit Überexpression einzelner Kinasen und Paaren von Kinase-Stellen, deren Verhalten über die Zeit stark korreliert war.
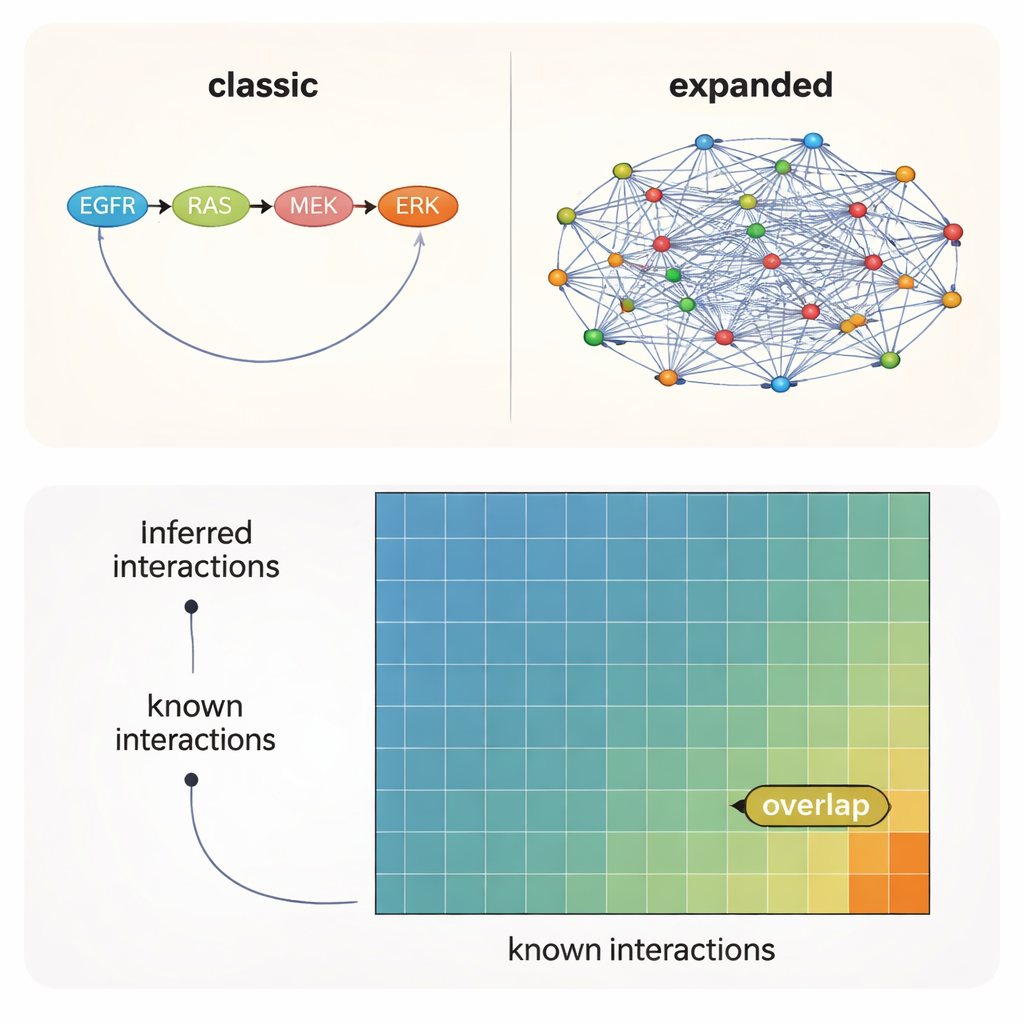
Die plausibelsten Verbindungen fehlen größtenteils auf der offiziellen Karte
Über alle Tests hinweg war eine Botschaft klar: Die Wahl des Vorwissens — welches Ausgangsnetzwerk man dem Algorithmus gibt — war wichtiger als die konkrete Methode oder sogar der experimentelle Kontext. Aus der Literatur abgeleitete Netzwerke fanden die größte Zahl bekannter Interaktionen, während breiter angelegte Vorhersagequellen auf viele zusätzliche, plausible Verbindungen hinwiesen, die noch nicht formell dokumentiert sind. Selbst unter besten Bedingungen waren jedoch nur etwa 10–12 % der durch Daten und Modelle vorgeschlagenen Interaktionen in irgendeinem Referenzsatz enthalten. Anders gesagt: Rund 90 % der unterstützten Kinase–Kinase-Verbindungen liegen in unbekanntem Terrain.
Was das für zukünftige Therapien bedeutet
Für Nichtfachleute lautet die Schlussfolgerung, dass das bekannte EGF-Diagramm in Lehrbüchern wohl nur die Spitze des Eisbergs ist. Moderne Phosphoproteomik in Kombination mit fortgeschrittenen Rechenmethoden enthüllt ein deutlich reichhaltigeres und verschachtelteres Signalinternet. Viele der neu vorgeschlagenen Verbindungen könnten übersehene Wege darstellen, mit denen Krebszellen Signale umleiten, um Medikamenten zu entkommen, oder neue Chancen für die Entwicklung intelligenterer Wirkstoffkombinationen bieten. Die Studie beweist nicht, dass jede neue Verbindung real ist, liefert aber eine Landkarte und offene Werkzeuge, mit denen Forschende diese Hypothesen testen können, mit dem Ziel genauerer und wirksamerer Therapien in Krankheiten, in denen die EGF-Signalgebung eine zentrale Rolle spielt.
Zitation: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Schlüsselwörter: EGF-Signalgebung, Phosphoproteomik, Proteinkinasen, zelluläre Signalnetzwerke, Krebsbiologie