Clear Sky Science · de
Mycobacterium tuberculosis moduliert die Phosphorylierung der Wirts-ATP6V1E1, um intrazelluläres Überleben zu fördern
Warum das für den Kampf gegen Tuberkulose wichtig ist
Tuberkulose bleibt eine der tödlichsten Infektionskrankheiten weltweit und tötet jährlich über eine Million Menschen. Unsere Immunzellen besitzen leistungsfähige „saure Recyclingbehälter“, die normalerweise eingedrungene Mikroben verdauen. Diese Arbeit deckt auf, wie das Tuberkulose-Bakterium Mycobacterium tuberculosis (Mtb) dieses Versauerungssystem in unseren Zellen sabotiert, und zeigt, dass ein Medikament, das diese Täuschung adressiert, infizierten Tieren helfen kann, die Infektion effektiver zu beseitigen.
Das zelluläre Säurebad für Krankheitserreger
Wenn Tuberkulose-Bakterien in die Lunge eingeatmet werden, werden sie schnell von Immunzellen, den Makrophagen, aufgenommen. Die Bakterien gelangen in Membranblasen, die eigentlich mit Lysosomen verschmelzen sollen — kleinen Säcken voller Verdauungsenzyme, die am besten in einer stark sauren Umgebung funktionieren. Diese Säure wird von einer molekularen Pumpe, der vakuolären ATPase (V-ATPase), erzeugt, die zellliche Energie nutzt, um Protonen in Lysosomen zu pumpen und so den internen pH zu senken. Eine ordnungsgemäße Versauerung ist entscheidend für den Abbau von Mtb, doch jahrzehntelange Forschung hat gezeigt, dass dieser Erreger seine Kompartimente weniger sauer hält und so überlebt.
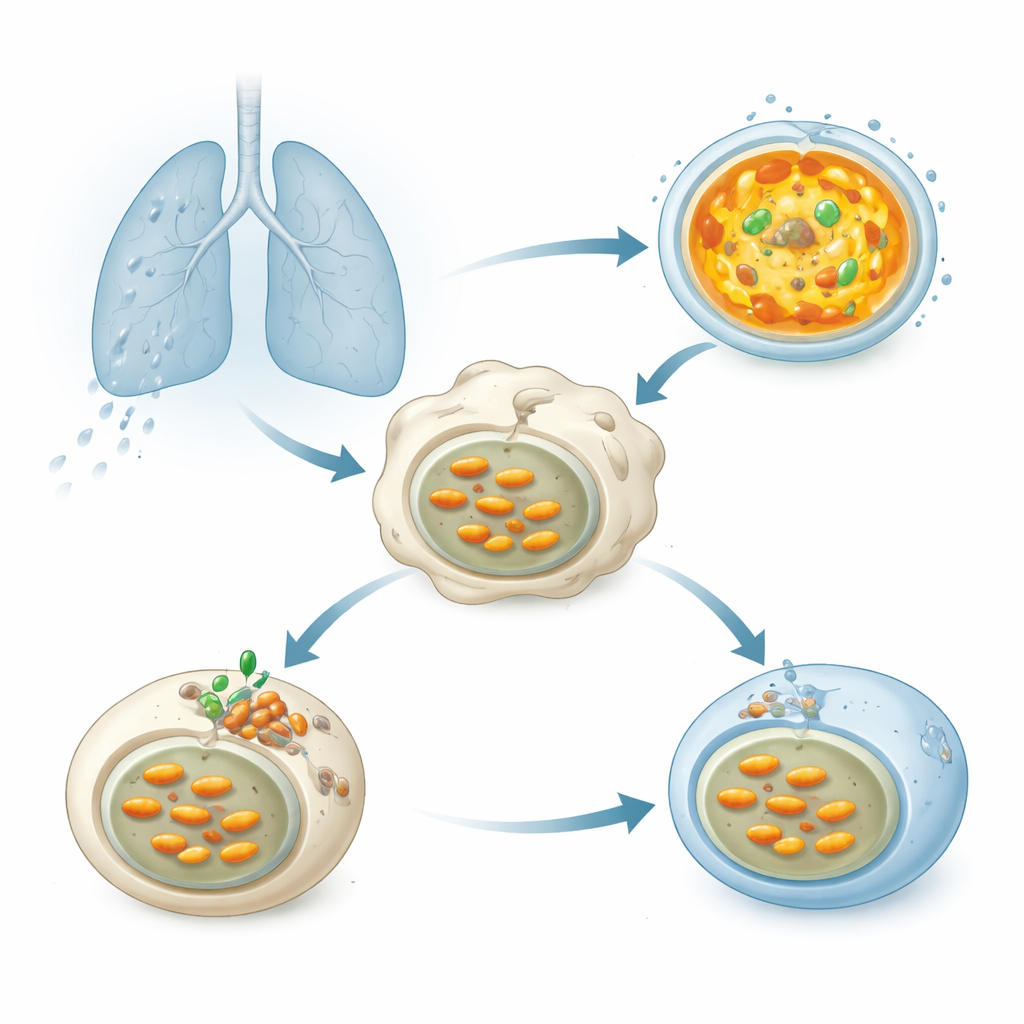
Ein bakterieller Helfer, der die Versauerung blockiert
Die Forscher untersuchten mehr als 200 Proteine, die Mtb freisetzen kann, um zu sehen, welche die lysosomale Versauerung in menschlichen Zellen abschwächen. Ein Protein stach hervor: ein Enzym namens Chp2 (auch bekannt als Rv1184). Wenn Zellen Chp2 produzierten, zeigten ihre Lysosomen mit säureempfindlichen Farbstoffen eine schwächere Signalstärke, was auf einen höheren, weniger feindlichen pH-Wert hindeutet. Mtb-Stämme, denen Chp2 fehlte, unterdrückten die Versauerung nicht mehr; in infizierten Makrophagen und Mäusen wurden diese Mutanten effizienter beseitigt und verursachten weniger schwere Lungenschäden. Die Wiederherstellung von Chp2 im Mutantenstamm brachte sowohl die Blockade der Versauerung als auch die erhöhte Bakterienlast zurück und identifizierte Chp2 damit als Virulenzfaktor, der Mtb hilft, in Wirtszellen zu persistieren.
Die Wirts-Pumpenuntereinheit als Kontrollschalter
Um zu verstehen, wie Chp2 die Versauerung stört, suchte das Team nach Wirtskomponenten, an die es binden könnte. Sie fanden, dass Chp2 direkt an einen bestimmten Teil der V-ATPase bindet: eine Untereinheit namens ATP6V1E1 (kurz E1), die hilft, die Struktur der Pumpe zu stabilisieren. Eine Erhöhung der E1-Menge in Zellen verstärkte die lysosomale Versauerung und erschwerte das Überleben von Mtb, während eine Verringerung von E1 den gegenteiligen Effekt hatte. Mäuse mit nur einer funktionierenden Kopie des E1-Gens zeigten weniger saure Lysosomen, höhere bakterielle Belastungen in der Lunge und stärkere Gewebeschäden nach Infektion, was zeigt, dass E1 ein wichtiger Wirtsfaktor zur Abwehr von Tuberkulose ist.
Ein Kinase-Anhängsel an der Pumpe, das die Säure herunterregelt
Die Autoren fragten dann, ob chemische „Marken“ auf E1 die Aktivität der Pumpe feinjustieren könnten. Sie entdeckten, dass das Anfügen von Phosphatgruppen an zwei spezifischen Tyrosinen (Tyr56 und Tyr57) von E1 wie eine Bremse wirkt: das Nachahmen der Phosphorylierung reduzierte die Versauerung und verhinderte die vollständige Assemblierung der V-ATPase, während das Verhindern der Phosphorylierung den gegenteiligen Effekt hatte. Durch Tests einer Enzympanel identifizierten sie eine Kinase namens BMX als das Wirtsprotein, das diese Markierung anbringt. Wurde BMX genetisch oder mit einem kleinen Molekül-Inhibitor blockiert, sank die E1-Phosphorylierung, die Pumpe setzte sich effizienter an lysosomalen Membranen zusammen, Lysosomen wurden saurer und das Überleben von Mtb in Makrophagen nahm ab.
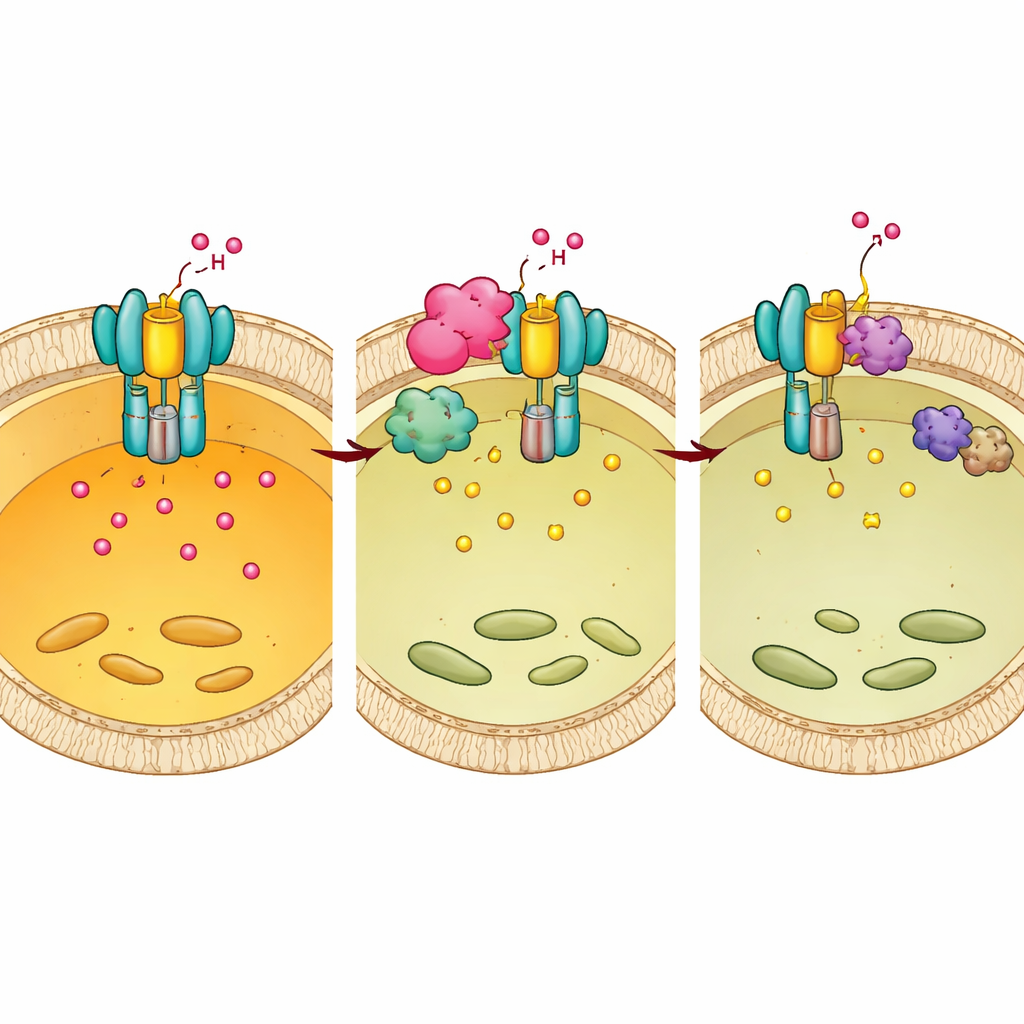
Wie Mtb den Wirts-Schalter zu seinen Gunsten umgeht
Chp2 und BMX arbeiten zusammen. Strukturelle und biochemische Experimente zeigten, dass Chp2 als Gerüst fungiert, das E1 und BMX an der Lysosomenoberfläche in Nähe zueinander bringt und so die Phosphorylierung von E1 an Tyr56/57 verstärkt. Diese zusätzliche Markierung stört die vollständige Pumpenassemblierung, erhöht den lysosomalen pH-Wert und schafft eine mildere Umgebung, in der Mtb persistieren kann. Wurde BMX gehemmt, verschwand der Überlebensvorteil, den Chp2 verschaffte, sowohl in kultivierten Zellen als auch in infizierten Mäusen. Wichtig ist, dass die Behandlung von Mäusen mit dem BMX-Inhibitor nach Infektion die bakterielle Belastung und Lungenschädigung bei normalen Tieren verringerte, jedoch nicht bei Mäusen mit geschwächtem E1 — was darauf hinweist, dass das Medikament durch Wiederherstellung einer effektiven E1-geführten Versauerung wirkt.
Die Täuschung des Erregers als therapeutische Idee
Alltagssprachlich zeigt diese Studie, dass Tuberkelbakterien ein Helferprotein in unsere Zellen einschleusen, das die „Säurepumpe“ des Abfallsystems so beeinflusst, dass sie gerade genug heruntergeregelt wird, damit die Mikroben der Vernichtung entgehen. Indem die Autoren die Pumpenuntereinheit identifizieren, die als Stellknopf dient (E1), und das Wirtsenzym, das diesen Knopf umlegt (BMX), legen sie einen präzisen Ansatzpunkt offen, an dem ein Medikament eingreifen kann. Die Hemmung von BMX bei Mäusen reaktiviert effektiv das zelluläre Säurebad und verbessert die bakterielle Beseitigung. Diese Erkenntnisse ebnen den Weg für wirtsgerichtete Therapien, die unsere eigenen Zellen gegenüber Mtb feindlicher machen können, möglicherweise in Kombination mit Antibiotika und zur Bekämpfung von medikamentenresistenter Tuberkulose.
Zitation: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Schlüsselwörter: Tuberkulose, Lysosomen, wirtsgerichtete Therapie, Mycobacterium tuberculosis, V-ATPase