Clear Sky Science · de
Entwicklung eines potenten monoklonalen Antikörpers zur Behandlung von Infektionen mit humanem Metapneumovirus
Warum ein verborgenes Wintervirus wichtig ist
Jede Erkältungs- und Grippesaison schickt ein wenig bekanntes Virus, das humane Metapneumovirus (HMPV), stillschweigend Millionen von Kleinkindern, älteren Erwachsenen und immungeschwächten Menschen in Kliniken und Krankenhäuser. Im Gegensatz zu seinem viralen Verwandten, dem respiratorischen Synzytialvirus (RSV), gibt es gegen HMPV weder Impfstoffe noch gezielte Therapien. Diese Studie berichtet die Entdeckung eines starken laborgefertigten Antikörpers, genannt 4F11, der HMPV in Zellen stoppen und infizierte Tiere schützen kann und damit auf ein dringend benötigtes neues Medikament für einige der verwundbarsten Patientengruppen hindeutet.
Das Virus, das unter dem Radar bleibt
HMPV ist ein weltweit verbreitetes Atemwegsvirus und verantwortlich für schätzungsweise 14 Millionen Infektionen der unteren Atemwege bei Kindern unter fünf Jahren pro Jahr; auch bei Erwachsenen über 60 fordert es erhebliche Opfer. Bei Patienten mit stark geschwächter Immunabwehr – etwa Empfängern von Stammzelltransplantationen – kann die Sterblichkeit durch HMPV-Lungeninfektionen alarmierend hoch sein. Für verwandte Viren wie RSV entstehen gerade erst Impfstoffe, und selbst wenn es einen HMPV-Impfstoff gäbe, würden viele stark immunsupprimierte Patienten kaum darauf ansprechen. Wegen dieser Lücke wenden sich Forschende monoklonalen Antikörpern zu – präzise zielgerichteten Immunproteinen, die als Arzneimittel verabreicht werden können, um schwere Infektionen zu verhindern oder zu behandeln.
Auf der Suche nach einem besonders schützenden Antikörper
Das Team machte sich daran, einen Antikörper mit drei Schlüsselmerkmalen zu finden: er musste extrem potent sein, gegen viele verschiedene HMPV-Stämme wirken und dem Virus nur wenig Raum zur Entwicklung von Resistenz lassen. Sie konzentrierten sich auf das Fusionsprotein des Virus, eine federbelastete Struktur auf der Virushülle, die ihre Form ändern muss, damit das Virus mit Lungenzellen verschmelzen und eindringen kann. Mithilfe einer „Köder-und-Tausch“-Strategie fischten sie seltene menschliche B‑Zellen aus Blut- und Milzproben, die einen Stamm von HMPV erkennen konnten, aber einen anderen neutralisierten, wodurch breit wirkende Antikörper angereichert wurden. Aus mehr als tausend Kandidatenzellen isolierten sie drei vielversprechende Antikörper und stellten fest, dass einer – 4F11 – außerordentlich stark war, Infektionen von Zellen in Konzentrationen zu blockieren, die fast 50‑mal niedriger lagen als bei einem zuvor führenden Antikörper, und gegen alle vier großen globalen HMPV‑Subtypen wirkte.
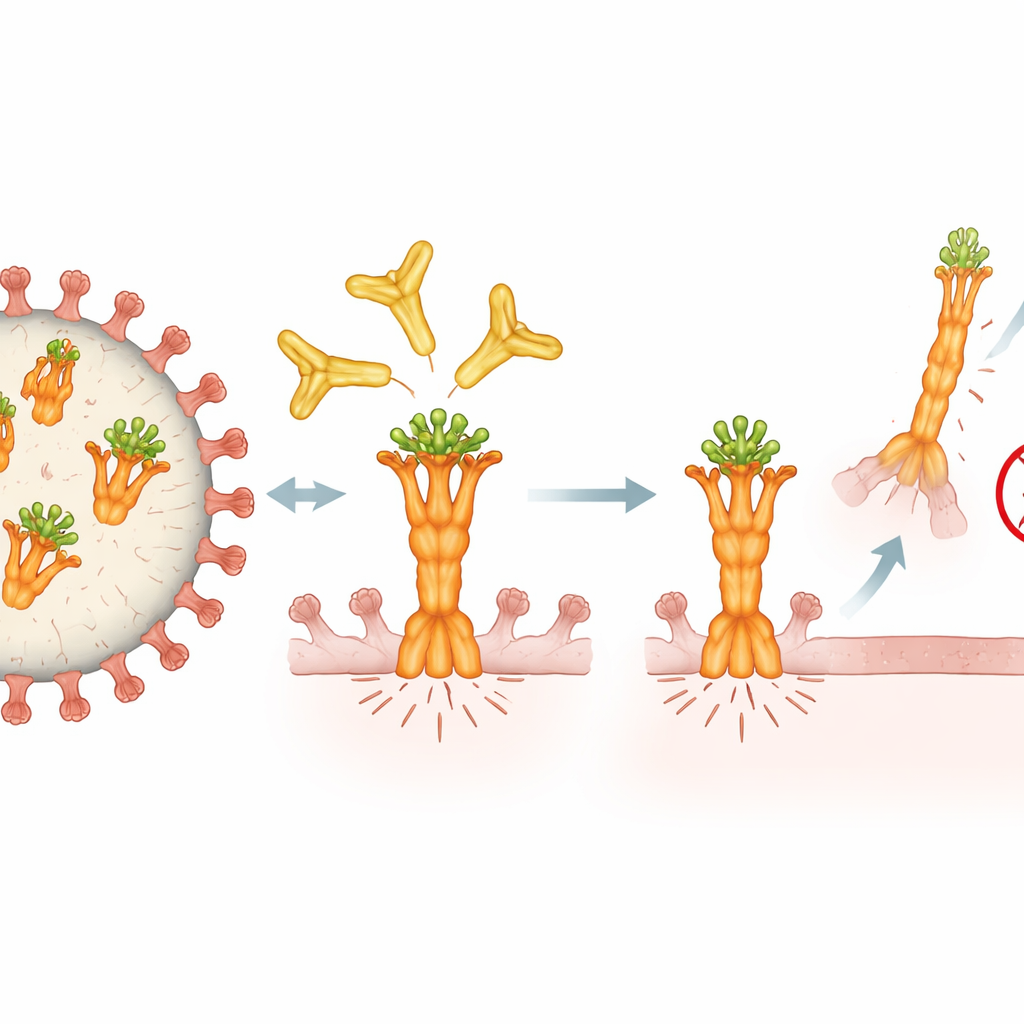
Wie 4F11 die Schwachstelle des Virus umgreift
Um zu verstehen, warum 4F11 so wirkungsvoll ist, nutzten die Forschenden hochauflösende Kryo‑Elektronenmikroskopie, um zu visualisieren, wie er am Fusionsprotein anliegt. Sie entdeckten, dass 4F11 eine winzige, konservierte Stelle ganz oben an der präfusionellen Form des Proteins – der Feder, bevor sie auslöst – anvisiert. Anders als andere Antikörper, die dreifach pro Fusionsprotein binden, sitzt 4F11 allein an der Spitze in einer Eins‑zu‑Eins‑Anordnung, reicht gerade nach unten und umfasst sogar eine Zuckerdekoration, die die Oberfläche schützt. Dieser ungewöhnliche Bindungswinkel und die Abhängigkeit von diesem Zucker machen 4F11 zu einem einzigartigen Antikörpertyp. Er erkennt nur die Prä‑Fusionsform, die auf infektiösem Virus vorhanden ist, und verhindert wahrscheinlich, dass das Protein sich in die Form umfaltet, die nötig ist, um in eine Wirtszelle einzudringen und mit ihr zu verschmelzen.
Kann das Virus entkommen – und zu welchem Preis?
Das Team setzte das Virus dann in Zellkultur der ständigen Präsenz von 4F11 aus, um zu sehen, wie leicht es Entkommungsvarianten entwickeln kann. Im Vergleich zu einem anderen Antikörperkontrollpräparat, das rasch mehrere Escape‑Mutationen hervorbrachte, hatte HMPV deutlich größere Schwierigkeiten, an 4F11 vorbeizuschlüpfen. Nur eine einzige Änderung im Fusionsprotein, die eine Aminosäure an Position 179 veränderte, störte 4F11‑Bindung vollständig. Viren mit dieser Mutation wuchsen jedoch deutlich schlechter als das normale Virus, was auf einen schweren Fitnessverlust hinweist. Datenbankrecherchen in Hunderten von HMPV‑Sequenzen zeigten, dass diese schädigende Veränderung in der Natur noch nie beobachtet wurde, was nahelegt, dass das Virus zwar im Labor prinzipiell an 4F11 vorbeikommen kann, dafür aber einen so hohen Preis in Form von Wachstumsnachteilen zahlt, dass eine weite Ausbreitung in der realen Welt unwahrscheinlich ist.
Schutzprüfung in einem Tiermodell
Laborwirksamkeit muss sich noch in echtem Schutz niederschlagen. Um dies zu testen, infizierten die Forschenden goldene Syrische Hamster mit HMPV und behandelten sie einen Tag später mit 4F11 – was eher einer frühen Therapie als einer Prophylaxe entspricht. Eine einzelne Niedrigdosisinjektion von 4F11 reduzierte die Virustiter in Lunge und Nasengängen deutlich, und bei höherer Dosis beseitigte sie in den meisten Tieren das nachweisbare Virus in der Lunge vollständig. Bemerkenswert sind die niedrigeren Dosen im Vergleich zu denen mehrerer monoklonaler Antikörper, die bereits für RSV beim Menschen zugelassen sind. Im Gegensatz dazu bot ein zuvor beschriebener Antikörper mit Kreuzreaktivität gegenüber mehreren Viren bei gleicher Dosis nur geringen Schutz, was die besondere Stärke von 4F11 als fokussierte HMPV‑Therapie hervorhebt.
Was das für Patientinnen und Patienten bedeuten könnte
Zusammen positionieren diese Befunde 4F11 als starken Kandidaten für die klinische Entwicklung. Er vereint hohe Potenz, breite Abdeckung zirkulierender HMPV‑Stämme, eine charakteristische Art, eine verwundbare Region des Fusionsproteins zu umgreifen, und ein Resistenzprofil, bei dem die offensichtliche Fluchtmöglichkeit des Virus mit einem erheblichen selbst zugefügten Nachteil einhergeht. Für Säuglinge, ältere Erwachsene und immungeschwächte Patientinnen und Patienten mit hohem Risiko für einen schweren HMPV‑Verlauf könnte ein auf 4F11 basierendes Arzneimittel eines Tages sowohl eine Notfallbehandlung nach Infektion als auch zusätzlichen Schutz neben oder statt Impfstoffen bieten.
Zitation: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
Schlüsselwörter: humanes Metapneumovirus, monoklonaler Antikörper, Atemwegsinfektion, Fusionsprotein, antivirale Therapie