Clear Sky Science · de
Eine Fehlpaar-Variante in ASCL5 führt zu Lobodontie
Wenn Zähne wie die eines Raubtiers aussehen
Lobodontie ist ein extrem seltener Zustand, bei dem menschliche Zähne ein auffälliges, nahezu carnivorenähnliches Aussehen annehmen, mit zusätzlich scharfen Kuppen und ungewöhnlichen Wurzeln. Bislang vermuteten Forscher, dass ein Calciumkanal‑Gen namens CACNA1S verantwortlich sei, doch die Belege waren dünn. Diese Studie beleuchtet die Frage mit modernen genomischen Methoden und Tierexperimenten neu und zeigt, dass ein anderes Gen, ASCL5, der eigentliche Treiber ist — und offenbart, wie eine winzige Veränderung in unserer DNA die Architektur von Zähnen und Kiefer umgestalten kann.
Seltsame Zähne in ansonsten gesunden Familien
Die Forscher untersuchten 17 Personen aus sechs thailändischen und kroatischen Familien, die dasselbe ungewöhnliche Gebissmuster teilten. Ihre Eckzähne waren verlängert und fangähnlich, die Prämolaren wiesen scharfe, spitze Kanten auf und die Molaren trugen mehrere zusätzliche Höcker, die an fleischfressende Tiere erinnerten. Röntgenaufnahmen zeigten weitere Besonderheiten: Schichten von Zahnschmelz, die in den Zahn hineinreichen, vergrößerte Pulpenkammern und untere Molaren mit einer einzelnen, dicken, pyramidenförmigen Wurzel statt der üblichen verzweigten Wurzeln. Trotz dieser dramatischen Veränderungen im Mund waren alle Betroffenen sonst gesund und wiesen normale Entwicklung und Intelligenz auf. Die Erkrankung trat in jeder Generation und bei beiden Geschlechtern auf, was auf eine einzelne dominante genetische Veränderung hinweist.
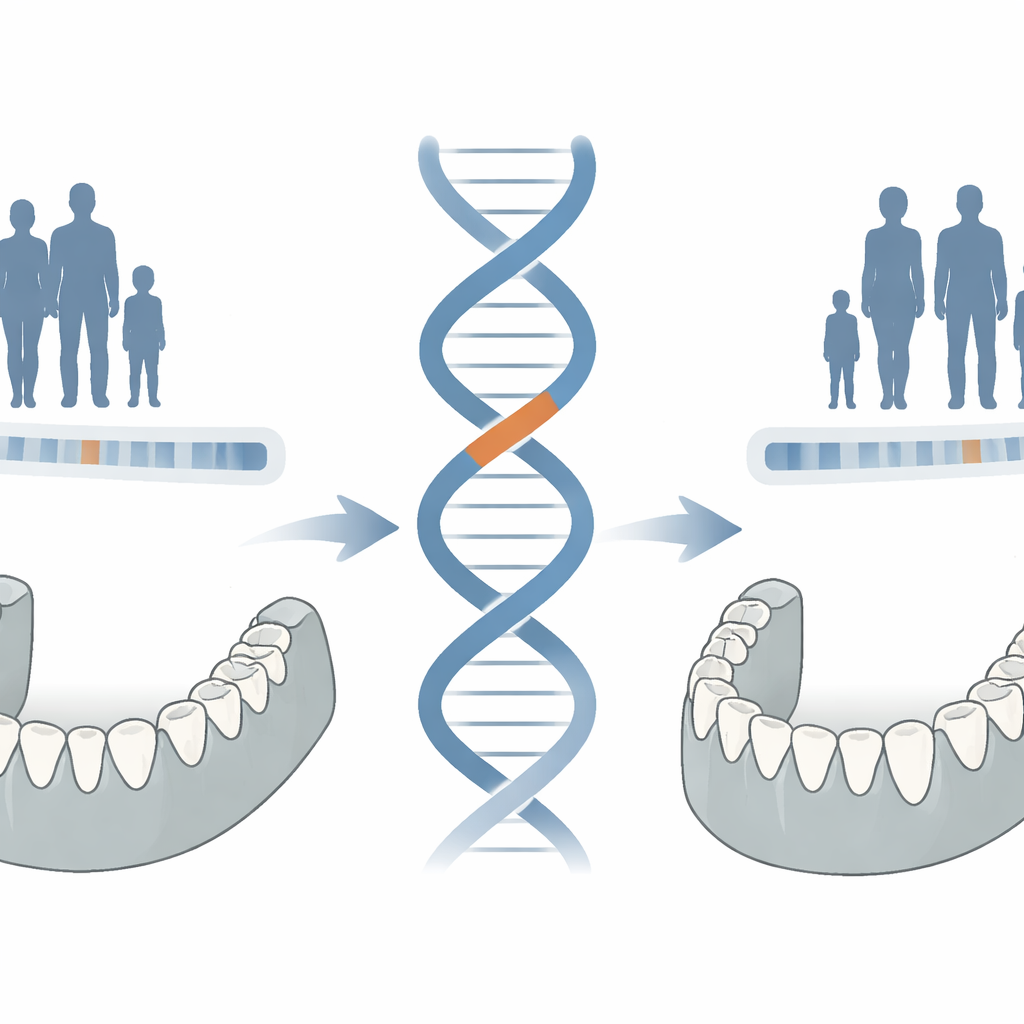
Vom Verdächtigen zum eigentlichen Schuldigen
Frühere Berichte hatten Lobodontie mit einer Variante in CACNA1S in Verbindung gebracht, einem Gen, das eher für seine Rolle in der Muskelarbeit bekannt ist. In der neuen Studie fanden die Autoren heraus, dass alle thailändischen Patienten diese CACNA1S‑Veränderung trugen, die kroatischen Patienten mit demselben Zahnphänotyp jedoch nicht. Noch aufschlussreicher war, dass eine gesunde thailändische Person mit normalen Zähnen ebenfalls die CACNA1S‑Variante besaß. Das war ein Warnsignal: Vielleicht reiste diese Veränderung nur zusammen mit der wahren Ursache auf demselben Chromosomenabschnitt, anstatt die Erkrankung selbst zu verursachen. Durch die Kombination von Ganzgenomsequenzierung mit feiner genetischer Kartierung in den thailändischen Familien schränkten die Forscher die Suche auf eine 15,4 Millionen Basen lange Region auf Chromosom 1 ein, die sowohl CACNA1S als auch ein wenig untersuchtes Gen, ASCL5, enthielt.
Ein einzelner Buchstabenwechsel in einem zahnspezifischen Gen
Innerhalb dieser Region deckte die Genomsequenzierung einen auffälligen Befund auf: Alle betroffenen Familienmitglieder, sowohl thailändische als auch kroatische, trugen dieselbe Veränderung in ASCL5 — ein einziger DNA‑Buchstabe, der eine Aminosäure im kodierten Protein verändert. Keiner der nicht betroffenen Verwandten trug diese Veränderung, und sie fehlte in großen Bevölkerungsdatenbanken, was ihre Seltenheit unterstreicht. ASCL5 ist ein Transkriptionsfaktor, ein Protein, das andere Gene an- oder ausschaltet; sein naher Verwandter bei der Maus, AmeloD genannt, ist dafür bekannt, in der Entwicklung des Zahnschmelzes aktiv zu sein. Computermodelle deuteten darauf hin, dass die neue Aminosäure die Bindung von ASCL5 an DNA schwächen und damit seine Kontrolle über wichtige Entwicklungsgene verändern könnte.
Mausbefunde: Wenn Kiefer‑ und Zahnpläne aus dem Ruder laufen
Um zu prüfen, ob diese DNA‑Änderung die Entwicklung tatsächlich stört, setzten die Forscher CRISPR‑Genbearbeitung ein, um die äquivalente Mutation in Mäuse einzuführen. Tiere mit einer veränderten Kopie des Gens — entsprechend der menschlichen Situation — entwickelten zusätzliche Höcker an den Molaren und zeigten Wurzelanomalien, was der Lobodontie sehr ähnelt. Mäuse mit zwei veränderten Kopien schnitten weit schlechter ab: Sie hatten verkürzte Unterkiefer, fehlende oder stark missgestaltete Molaren und überlange Vorderzähne, was zeigt, dass ASCL5 für eine normale Kiefer‑ und Zahnbildung entscheidend ist. Bei der Untersuchung der Genaktivität in den sich entwickelnden Unterkiefern stellten die Forscher fest, dass mehrere Gene, die bereits für die Formung von Gesichtsknochen und Zähnen bekannt sind, darunter Mitglieder der DLX‑Familie und das Signalmolekül Shh, in mutierten Embryonen heruntergeregelt waren.
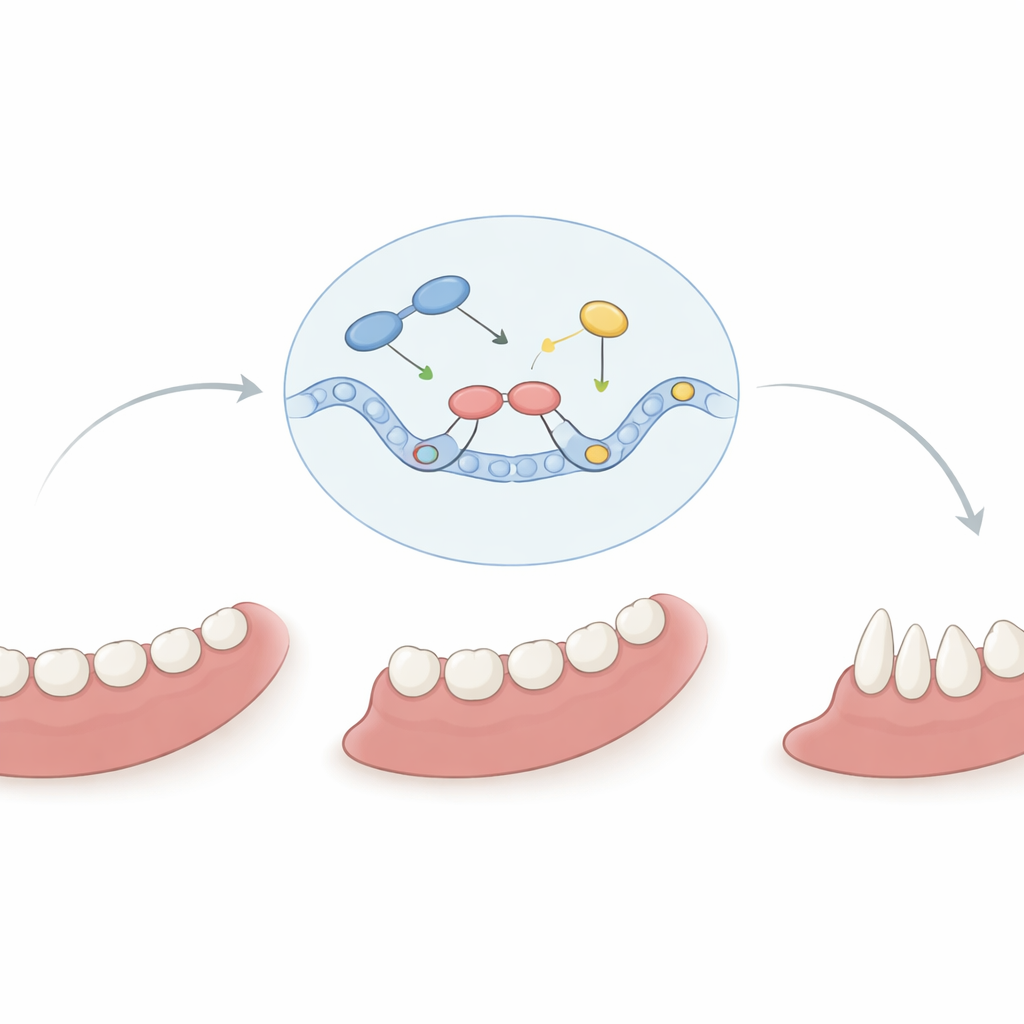
Wie ein fehlerhafter Schalter den Zahnbau fehlleitet
Da ASCL5 andere Gene steuert, fragten die Wissenschaftler, ob die lobodontie‑assoziierte Variante ihre normalen Aufgaben noch erfüllen kann. In zellbasierten Experimenten erhöhte das gesunde ASCL5‑Protein die Aktivität des DLX2‑Gens, eines Schlüsselfaktors in der kraniofazialen Entwicklung, während die mutierte Variante dies deutlich weniger wirksam erledigte. Gleichzeitig konnten sowohl das normale als auch das mutierte Protein ein Zelladhäsionsgen namens E‑Cadherin weiterhin unterdrücken, was darauf hindeutet, dass die Mutation einige Zielgene selektiv stört, andere jedoch nicht. In jungen Molaren mutierter Mäuse waren zusätzliche Gene, die mit der Bildung harter Gewebe verbunden sind, ungewöhnlich aktiviert, was nahelegt, dass die Variante auch die Mineralisation der Zähne fehlleiten könnte. Zusammengenommen zeichnen diese Ergebnisse das Bild von ASCL5 als fein abgestimmtem Hauptregler: Wenn eine kritische Aminosäure verändert ist, verschiebt sich das Timing und die Balance der Signale, die Zähne und Kiefer formen, was zu raubtierähnlichen Kronen, seltsamen Wurzeln und in schweren Fällen zu fehlenden Zähnen führt.
Was das für seltene Zahnfehler bedeutet
Indem diese Arbeit Lobodontie eindeutig mit einer spezifischen ASCL5‑Mutation verbindet und ihre Effekte in Mäusen reproduziert, widerlegt sie die frühere Fokussierung auf CACNA1S und etabliert ASCL5 als wichtigen Regulator dafür, wie Säugetierzähne und Kiefer Gestalt annehmen. Für Familien mit Lobodontie liefert sie eine klare genetische Erklärung und eine Grundlage für künftige Diagnosen. Allgemeiner zeigt sie, wie eine subtile Veränderung an einem entwicklungsbiologischen „Regelknopf“ die Form unserer Zähne neu ordnen kann, ohne den Rest des Körpers zu beeinträchtigen, und liefert neue Einblicke in seltene Zahnkrankheiten und die evolutionäre Anpassungsfähigkeit unseres Lächelns.
Zitation: Theerapanon, T., Intarak, N., Rattanapornsompong, K. et al. A missense variant in ASCL5 leads to lobodontia. Nat Commun 17, 2643 (2026). https://doi.org/10.1038/s41467-026-69323-1
Schlüsselwörter: lobodontie, ASCL5-Gen, Zahnentwicklung, kraniofaziale Genetik, dentale Anomalien