Clear Sky Science · de
Präoptisches Kisspeptin-nNOS-GnRH (KiNG) Neuronalnetzwerk reguliert LH-Rhythmik durch Aktivierung und Hemmung bei Mäusen
Warum diese Gehirngeschichte für die Fruchtbarkeit wichtig ist
Ovulation und Fruchtbarkeit hängen von einer winzigen Gruppe von Gehirnzellen ab, die ein Steuerhormon in Pulsen und gelegentlichen Spitzen freisetzen. Wenn dieses Timing gestört ist, kann die Fortpflanzung scheitern. Diese Studie zeigt, wie zwei Arten von Botenstoffen im Mausgehirn – einer, der Aktivität einschaltet, und ein anderer, der sie leise wieder abschaltet – zusammenwirken, um diese Hormonrhythmen zu gestalten. Das Verständnis dieses verborgenen Zeitgebers könnte helfen, bestimmte Formen von Unfruchtbarkeit zu erklären und neue Wege zur Behandlung von Fortpflanzungsstörungen aufzuzeigen.
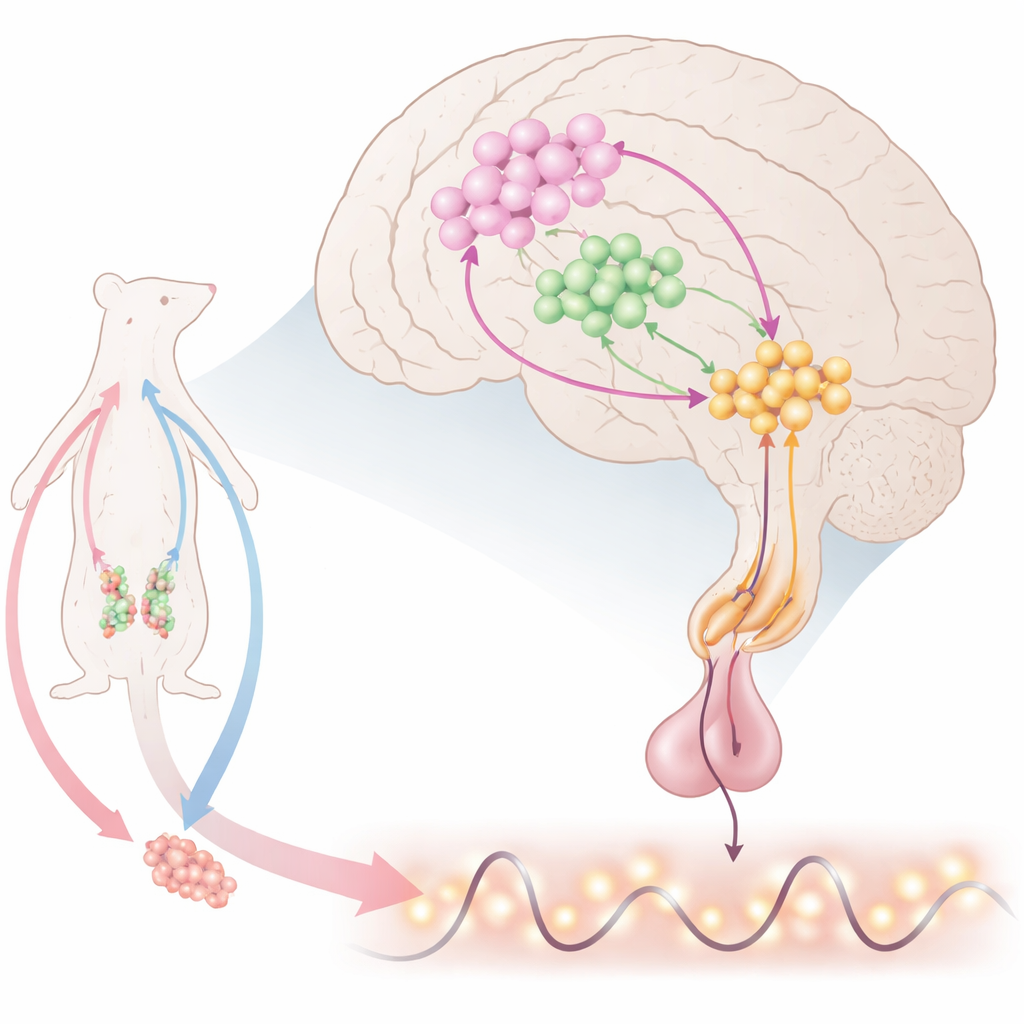
Der Zeitgeber des Gehirns für die Fortpflanzung
Tief im Gehirn setzen spezielle Nervenzellen das Gonadotropin-Releasing-Hormon (GnRH) frei, das die Hypophyse veranlasst, Luteinisierendes Hormon (LH) und Follikelstimulierendes Hormon auszuschütten. Diese steuern wiederum Eierstöcke und Hoden. GnRH fließt nicht gleichmäßig, sondern erscheint in regelmäßigen Pulsen und – bei Weibchen – in einer großen präovulatorischen Spitze. Forschende wissen, dass viele Signale auf GnRH-Zellen einwirken, doch die genaue Kombination, die sowohl Pulse als auch Spitzen erzeugt, war bislang unklar. Diese Arbeit konzentriert sich auf eine kleine Region vorne im Hypothalamus, wo GnRH-Zellen mit zwei weiteren wichtigen Akteuren zusammentreffen: kisspeptinproduzierenden Neuronen, die GnRH erregen, und Neuronen, die Stickstoffmonoxid (NO) herstellen, ein gasförmiges Signal, das sich über kurze Distanzen ausbreiten kann.
Eine Ein–Aus-Partnerschaft zwischen zwei Signalen
Die Forschenden schlagen ein dreiteiliges „KiNG“-Netzwerk vor, bestehend aus Kisspeptin-, NO-produzierenden (nNOS-) Neuronen und GnRH-Zellen. Kisspeptin ist ein starker Aktivator, der GnRH- und LH-Freisetzung antreiben kann, aber dauerhafte Stimulation fährt das System herunter, was nahelegt, dass eine interne Bremse nötig ist. Mit hochsensitiven molekularen Sonden, genetischen Werkzeugen und Aufzeichnungen aus Gehirnschnitten bei Mäusen zeigen die Autorinnen und Autoren, dass Kisspeptin mehr tut als nur GnRH-Neurone direkt zu erregen. Es aktiviert auch nahegelegene nNOS-Neurone im präoptischen Bereich, insbesondere in einer Region namens OV/MePO. Wenn Kisspeptin ansteigt, produzieren diese nNOS-Zellen NO in Bursts, was die Produktion des Botenstoffs cGMP in umliegenden Zellen, einschließlich der GnRH-Neurone selbst, auslöst. Dieses NO–cGMP-Signal dämpft das Feuern von GnRH und fungiert damit als eingebauter Abschalter für den Kisspeptin-Antrieb.
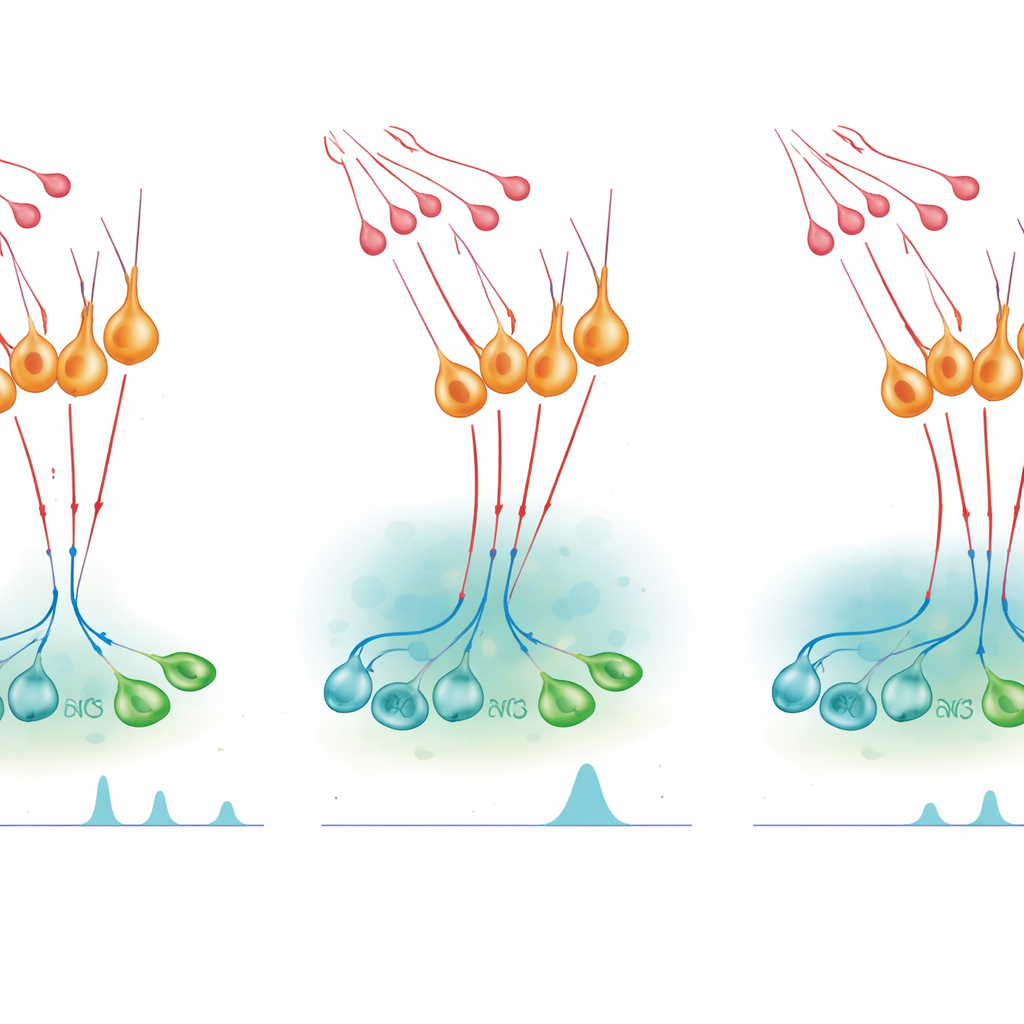
Spitzen der Hormone anschalten und wieder zurückschneiden
Um zu prüfen, wie dieser Mikroschaltkreis die Hormonfreisetzung beeinflusst, setzten die Forschenden chemogenetische Schalter ein – gentechnisch veränderte Rezeptoren, die von einem ansonsten inaktiven Wirkstoff aktiviert werden –, um nNOS-Neurone in lebenden Mäusen ein- oder auszuschalten. Künstliche Aktivierung der nNOS-Zellen während einer normalerweise ruhigen Phase des weiblichen Zyklus reichte aus, um einen spurähnlichen Anstieg des LH im Blut zu erzeugen; Gleiches galt für Männchen. Die Blockade der NO-Produktion beseitigte diesen Effekt, was zeigt, dass NO aus diesen Neuronen für die Spitze notwendig ist. Wenn jedoch die nNOS-Neurone gehemmt oder ihre Kisspeptin-Empfindlichkeit verringert wurden, führte eine Kisspeptin-Gabe zu einem übermäßigen und verlängerten LH-Anstieg. Pharmakologische Substanzen, die die NO-Synthese blockieren, hatten einen ähnlichen verstärkenden Effekt, während ein Wirkstoff, der das cGMP-Signal verlängert, die Kisspeptin-Antwort verkürzte und die spätere LH-Freisetzung reduzierte. Zusammengenommen deuten diese Experimente darauf hin, dass NO sowohl hilft, GnRH-Neurone zu synchronisieren, um Spitzen zu erzeugen, als auch begrenzt, wie lange Kisspeptin sie aktiv halten kann.
Ein flexibler Rhythmus über den Ovarialzyklus
Die Studie zeigt außerdem, dass dieses Ein–Aus-Gleichgewicht im Verlauf des weiblichen Zyklus variiert. Mithilfe einer sensiblen RNA-Nachweismethode fanden die Autorinnen und Autoren heraus, dass am Tag vor der Ovulation, wenn die Östrogenspiegel hoch sind und die LH-Spitze auftritt, mehr nNOS-Neurone den Kisspeptin-Rezeptor exprimieren. In den ruhigeren Phasen reagieren weniger nNOS-Neurone auf Kisspeptin und produzieren nur kleine, lokale Mengen NO, die GnRH-Pulse sanft dämpfen, ohne sie zu stoppen. Am Tag der Spitze führen stärkere Kisspeptin-Eingänge und erhöhte Rezeptorexpression zu einer massiven Steigerung der NO-Produktion, sodass NO weiter verbreitet wird und viele GnRH-Neurone gleichzeitig kurzzeitig stilllegt. Wenn das NO-Signal abklingt, erholen sich diese Zellen gemeinsam und erzeugen die große, koordinierte LH-Spitze, die für die Ovulation nötig ist.
Was das für die menschliche Gesundheit bedeutet
Einfach gesagt zeigt diese Arbeit, dass dasselbe Signal, das GnRH-Neurone startet – Kisspeptin – auch ein verzögertes Bremssystem über NO rekrutiert, wodurch hormonelle Ausbrüche stark, aber nicht unkontrolliert bleiben. Das KiNG-Netzwerk fungiert somit sowohl als Gaspedal als auch als Bremse der reproduktiven Zeitgebung, passt GnRH-Pulse während des Großteils des Zyklus an und formt die Spitze, die die Ovulation auslöst. Da genetische Veränderungen in Kisspeptin- und NO-Pfaden bei Menschen mit Fortpflanzungsstörungen gefunden wurden, könnte das Verständnis dieses fein ausbalancierten Schaltkreises neue Ansätze zur Diagnose und Behandlung von Unfruchtbarkeit und verwandten Erkrankungen ermöglichen.
Zitation: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Schlüsselwörter: reproduktive Hormone, Hypothalamus, Kisspeptin, Stickstoffmonoxid, Ovulations-Timing