Clear Sky Science · de
Histon-Lactylierung erhöht CXCL1-Expression für Neutrophileninfiltration und Immunflucht bei Bauchspeicheldrüsenkrebs
Warum diese Krebsstudie wichtig ist
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebsarten, teilweise weil er häufig modernen Immuntherapien widersteht, die bei anderen Tumoren wirken. Diese Studie zeigt, wie Bauchspeicheldrüsentumoren ihren eigenen Zuckerstoffwechsel umprogrammieren, um das Immunsystem stillschweigend zu schwächen, und wie das Blockieren dieses Prozesses einen Weg öffnen könnte, damit die körpereigenen Abwehrkräfte — und vorhandene Medikamente — wieder wirksam werden.
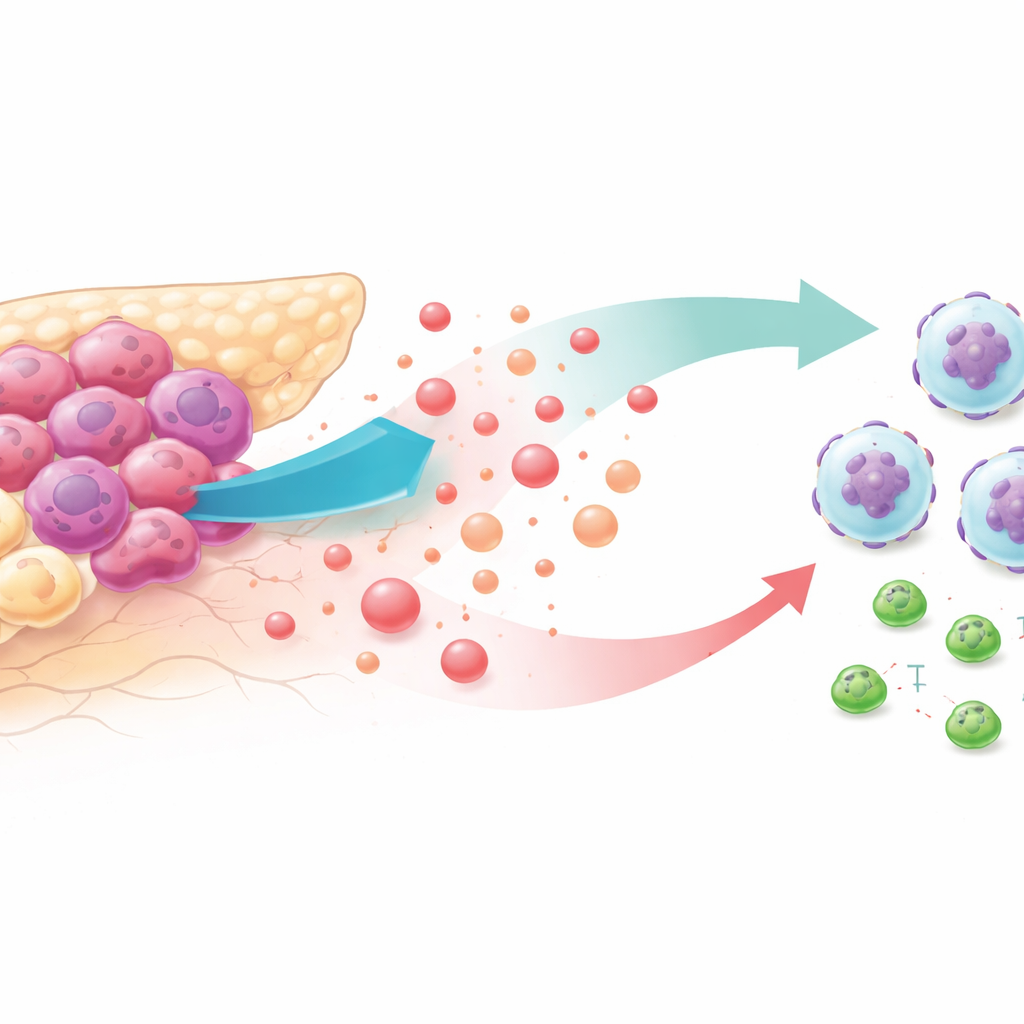
Zuckerhungrige Tumoren und eine feindliche Nachbarschaft
Krebszellen sind dafür bekannt, Glukose in rasanter Geschwindigkeit zu verbrennen, selbst wenn genügend Sauerstoff vorhanden ist. Dieser "hohe Glykolyse"-Stoffwechsel überschwemmt das Tumorumfeld mit Lactat, einem Nebenprodukt, das lange als bloßer Stoffwechselmüll abgetan wurde. Anhand von Patientendatenbanken und Mausmodellen fanden die Forschenden heraus, dass Bauchspeicheldrüsentumoren mit besonders intensiver Glykolyse reichlich Neutrophile enthielten — weiße Blutkörperchen, die in diesem Kontext das Tumorwachstum unterstützen — und gleichzeitig weniger krebsabtötende CD8-T-Zellen aufwiesen. Patienten mit diesem Profil in ihren Tumoren hatten tendenziell eine kürzere Überlebenszeit, was darauf hindeutet, dass veränderter Stoffwechsel und Immunflucht eng miteinander verknüpft sind.
Wie Tumoren Lactat nutzen, um die falsche Hilfe herbeizurufen
Um zu verstehen, wie Glykolyse Neutrophile anlockt, senkte das Team die Tumorglykolyse mit Medikamenten oder genetischen Eingriffen in Bauchspeicheldrüsenkrebs-Zelllinien und in Mäusen. Wurde der Zuckerabbau blockiert, setzten die Tumorzellen deutlich weniger eines chemischen Signals namens CXCL1 frei, und die zirkulierenden Werte dieses Signals sanken sowohl in Mäusen als auch in Patientenproben. In Labortests zur Migration wanderten Neutrophile eifrig auf Nährmedien von hochglykolytischen Krebszellen zu, nicht aber auf Medien von glykolyseblockierten Zellen — es sei denn, die Forschenden gaben gereinigtes CXCL1 wieder hinzu. In lebenden Mäusen führte das Wiederherstellen von CXCL1 in Tumoren mit reduzierter Glykolyse zu einer Rückkehr der Neutrophilenzahlen und schwächte den antitumoralen Effekt der Glykolysehemmung.
Ein neuer epigenetischer Schalter, angetrieben von Lactat
Die Studie ging dann auf die Ebene der DNA-Verpackung. Unsere Gene sind um spoolähnliche Proteine, sogenannte Histone, gewickelt; deren chemische Anhänge wirken als Ein-/Ausschalter für die Genaktivität. Die Autoren zeigen, dass in Bauchspeicheldrüsenkrebs Lactat aus der Glykolyse eine spezifische "Lactyl"-Markierung an einer Histonposition hinzufügt, bekannt als H3K18. Diese Modifikation, Histon H3K18-Lactylierung, war in Tumorgeweben deutlich höher als in normaler Bauchspeicheldrüse. Wenn die Glykolyse blockiert wurde, fiel die Lactylierung an H3K18, insbesondere in der Nähe der Kontrollregion des CXCL1-Gens, und die CXCL1-Produktion sank. Die Zugabe von Lactat stellte sowohl die Histonmarke als auch die CXCL1-Expression wieder her. Über Patientenproben hinweg zeigten Tumoren mit mehr H3K18-Lactylierung auch höhere CXCL1-Werte, was diesen molekularen Marker mit einer pro‑tumoralen Immunlandschaft verbindet.
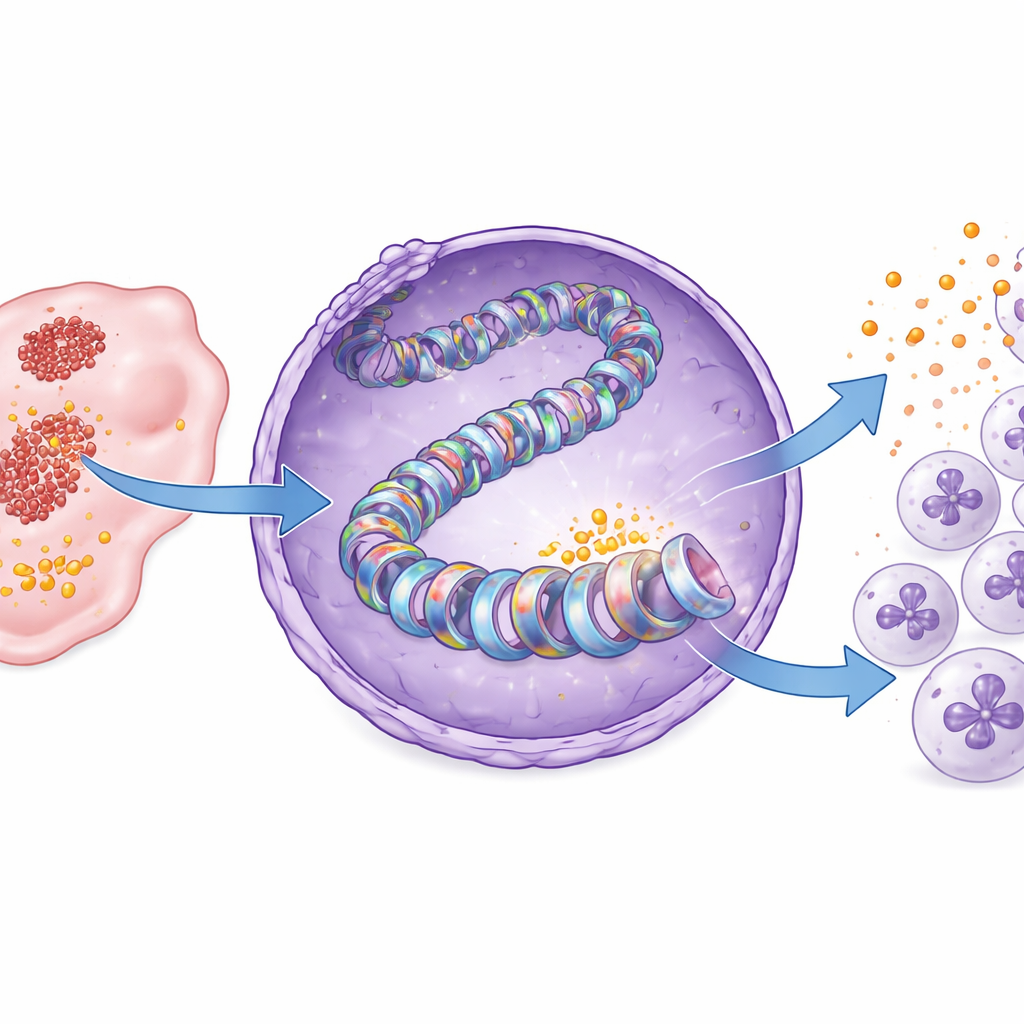
Identifizierung des Enzyms und einer medikablen Schwachstelle
Histonmarken werden von spezialisierten Enzymen gesetzt. Durch das Screening von Inhibitoren bekannter histonmodifizierender Proteine identifizierten die Forschenden ein Enzym namens PCAF als wichtigen Writer der H3K18-Lactylierung im Bauchspeicheldrüsenkrebs. Strukturelle Modellierung deutete darauf hin, dass PCAF an Lactyl‑CoA binden kann, die aktivierte Form von Lactat, die für das Anbringen der Markierung verwendet wird, und biochemische Tests bestätigten, dass gereinigtes PCAF direkt Lactylgruppen an Histon H3 anfügen kann. Die Hemmung von PCAF mit einem kleinen Molekül, Bromosporin, senkte die H3K18-Lactylierung und die CXCL1-Produktion in Krebszellen und in Maustumoren. Infolgedessen drangen weniger Neutrophile in die Tumoren ein, mehr CD8-T-Zellen sammelten sich an und das Tumorwachstum verlangsamte sich, ohne dass bei den Mäusen offensichtlicher Gewichtsverlust oder Toxizität auftrat.
Ein kalten Tumor mit Kombinationstherapie erwärmen
Da Standard-Checkpoint-Inhibitoren wie Anti‑PD‑1-Antikörper bei Bauchspeicheldrüsenkrebs nur begrenzt wirksam waren, prüfte das Team, ob das Zerstören des Lactat–PCAF–CXCL1‑Pfads diese Tumoren empfänglicher machen könnte. In subkutanen und orthotopen Pankreas‑Mausmodellen schrumpften Tumoren unter der Kombination von Bromosporin und Anti‑PD‑1 stärker als unter einer der Einzelbehandlungen, die Neutrophileninfiltration nahm ab, aktive CD8-T-Zellen wurden verstärkt, und das Überleben verlängerte sich deutlich. Dies legt nahe, dass das Unterbrechen der metabolischen "Sirene" für Neutrophile im Tumor dazu beiträgt, einen immunologisch "kalten" Tumor in einen "wärmeren" zu verwandeln, mit dem Checkpoint‑Therapie besser arbeiten kann.
Was das für zukünftige Behandlungen bedeutet
Vereinfacht gesagt offenbart die Studie eine Kettenreaktion: Bauchspeicheldrüsentumoren verbrennen Zucker, setzen Lactat frei, nutzen dieses Lactat, um einen epigenetischen Schalter an ihren DNA‑verpackenden Proteinen umzulegen, steigern CXCL1 und rufen so Neutrophile herbei, die ihnen helfen, sich vor Killer‑T‑Zellen zu verbergen. Das Unterbrechen dieser Kette am PCAF‑Schritt mit einem Wirkstoff verlangsamt nicht nur Tumoren, sondern macht bestehende Immuntherapien bei Mäusen auch wirksamer. Zwar sind weitere Arbeiten nötig, um die Sicherheit zu klären und den besten Weg zur Zielerreichung beim Menschen zu finden, doch diese Ergebnisse heben eine vielversprechende Strategie hervor: den Tumorstoffwechsel und die Gen-Schalter umprogrammieren, damit das Immunsystem eine faire Chance erhält.
Zitation: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Tumorstoffwechsel, Histon-Lactylierung, tumor Mikroumgebung, Krebs-Immuntherapie