Clear Sky Science · de
Entdeckung antimikrobieller Peptide, die Acinetobacter baumannii angreifen, mittels einer vortrainierten und feinabgestimmten Few‑Shot‑Learning‑Pipeline
Warum das für die Gesundheit im Alltag wichtig ist
Medikamentenresistente Infektionen nehmen so schnell zu, dass sie bis zur Mitte des Jahrhunderts jährlich mehr Menschen töten könnten als Krebs. Einer der beunruhigendsten Verursacher ist Acinetobacter baumannii, ein hartnäckiger Krankenhauskeim, der viele Antibiotika abwehrt und häufig Patienten auf Beatmungsgeräten befällt. Diese Studie zeigt, wie Wissenschaftler künstliche Intelligenz mit Laborversuchen kombinierten, um schnell neue, winzige Wirkstoffkandidaten zu entdecken, die dieses Bakterium abtöten können und dabei weit weniger Schaden im Körper anrichten als unsere derzeitigen letzten Rettungsmedikamente.
Ein Krankenhaus‑Superkeim, der schwer zu töten ist
Acinetobacter baumannii ist ein gramnegatives Bakterium, das sich besonders auf Intensivstationen wohlfühlt, vor allem bei Patienten, die auf Beatmungsgeräte angewiesen sind. Seine robuste Außenhülle und sein schnell evolvierendes Genom machen es gegen viele Standardantibiotika resistent. Heute ist eines der wenigen verbleibenden Mittel ein Wirkstoff namens Polymyxin B, der jedoch schwere Nierenschäden verursachen kann und gegen den das Bakterium weiterhin Resistenzen entwickeln kann. Gleichzeitig wurde eine vielversprechende Klasse kleiner Proteinfragmente, sogenannte antimikrobielle Peptide, gegen andere Mikroben untersucht, doch nur sehr wenige wirken gezielt und gut gegen A. baumannii. Traditionelles Trial‑and‑Error‑Screening ist schlicht zu langsam und zu teuer, um die astronomisch große Zahl möglicher kurzer Peptidsequenzen zu durchforsten.
Mit klugen Algorithmen einen riesigen Suchraum durchkämmen
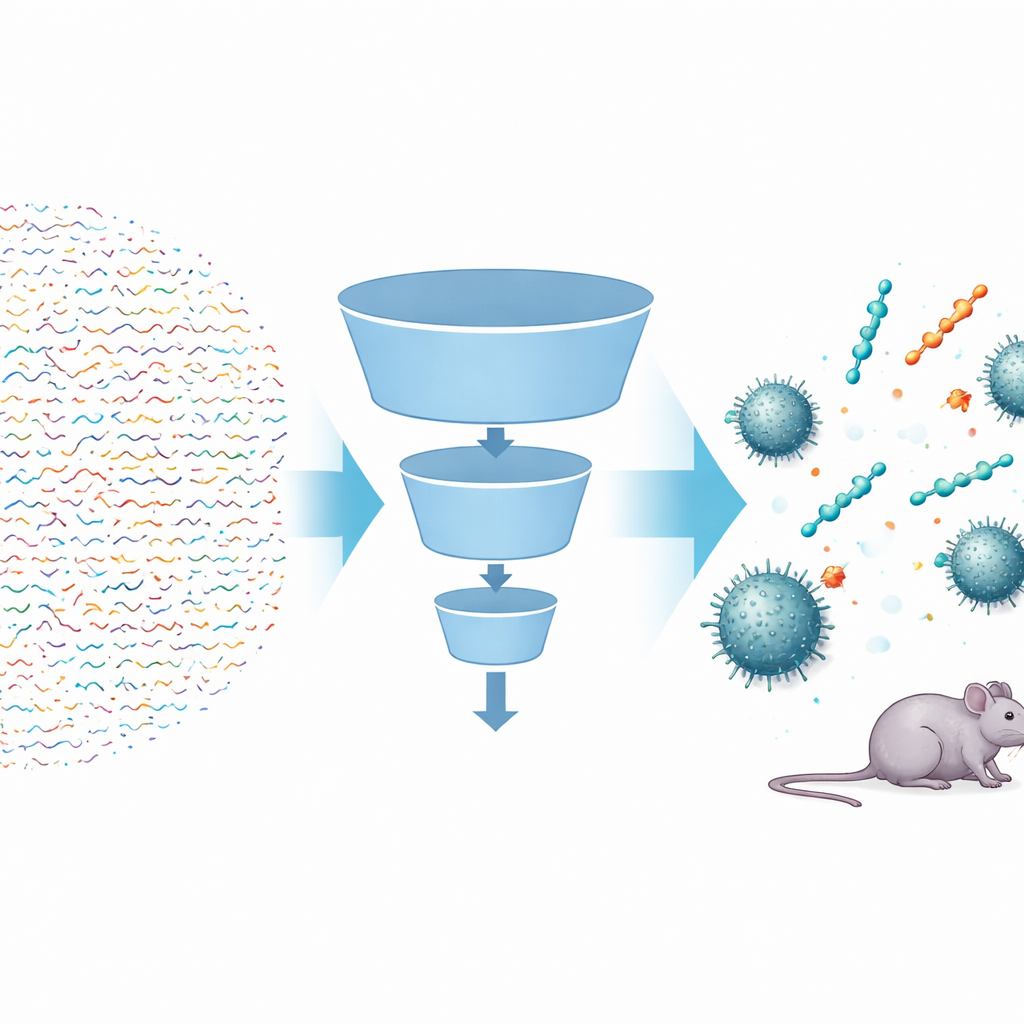
Die Forschenden bauten eine mehrstufige KI‑Pipeline namens FSLSMEP, um ganze Bibliotheken kurzer Peptide — solche mit sechs, sieben oder acht Bausteinen — zu scannen, was zehn- bis hunderte Milliarden Kandidaten ergibt. Die Herausforderung war, dass ihnen nur 148 bekannte Peptide vorlagen, die gegen A. baumannii wirken — bei Weitem zu wenige für herkömmliche maschinelle Lernmethoden. Um das zu umgehen, begannen sie mit einem leistungsfähigen vortrainierten Modell, das bereits Hunderte Millionen natürlicher Proteinsequenzen „gelesen“ und allgemeine Regeln über das Verhalten solcher Moleküle gelernt hatte. Dieses Modell wurde dann in zwei Stufen feinabgestimmt: zuerst mit einer größeren Menge von Peptiden, die gegen das verwandte Bakterium Pseudomonas aeruginosa aktiv sind, und schließlich mit den spärlichen A. baumannii‑Daten. Dabei wirkten drei gekoppelte Module — eines zum Sortieren wahrscheinlicher von unwahrscheinlichen Peptiden, eines zum Ranken und eines zur Schätzung der möglichen Wirksamkeit — wie aufeinanderfolgende Filter in einem Trichter.
Von Computer‑Vorhersagen zu Erfolgen im Reagenzglas
Nachdem zunächst die wenig vielversprechenden Peptide mittels einfacher chemischer Regeln aussortiert wurden, speiste das Team fast vier Millionen Kandidaten in seine Pipeline. Der Klassifikator entfernte die meisten Sequenzen, die nicht antimikrobiell erschienen; das Ranking‑Modell bevorzugte solche, deren Merkmale auf starke Aktivität hindeuteten; und das Regressionsmodell sagte die minimale Wirkstoffkonzentration voraus, die nötig ist, um Bakterienwachstum zu stoppen. Aus 64 Millionen Sechser‑Peptiden schlug das System nur zehn Spitzenkandidaten vor. Als diese synthetisiert und im Labor getestet wurden, zeigten neun echte antibakterielle Aktivität — eine beeindruckende Trefferquote in der Wirkstoffforschung. Dieselben trainierten Modelle wurden dann ohne erneutes Training auf wesentlich größere Sieben‑ und Achter‑Peptidräume angewandt, aus denen die Forschenden weitere topplazierte Sequenzen zur Prüfung auswählten. Auch hier erwiesen sich die meisten als aktiv, einschließlich Heptapeptiden, die gegen manche Stämme so wirksam wie Polymyxin B waren.
Starke Killer mit sanfterer Wirkung
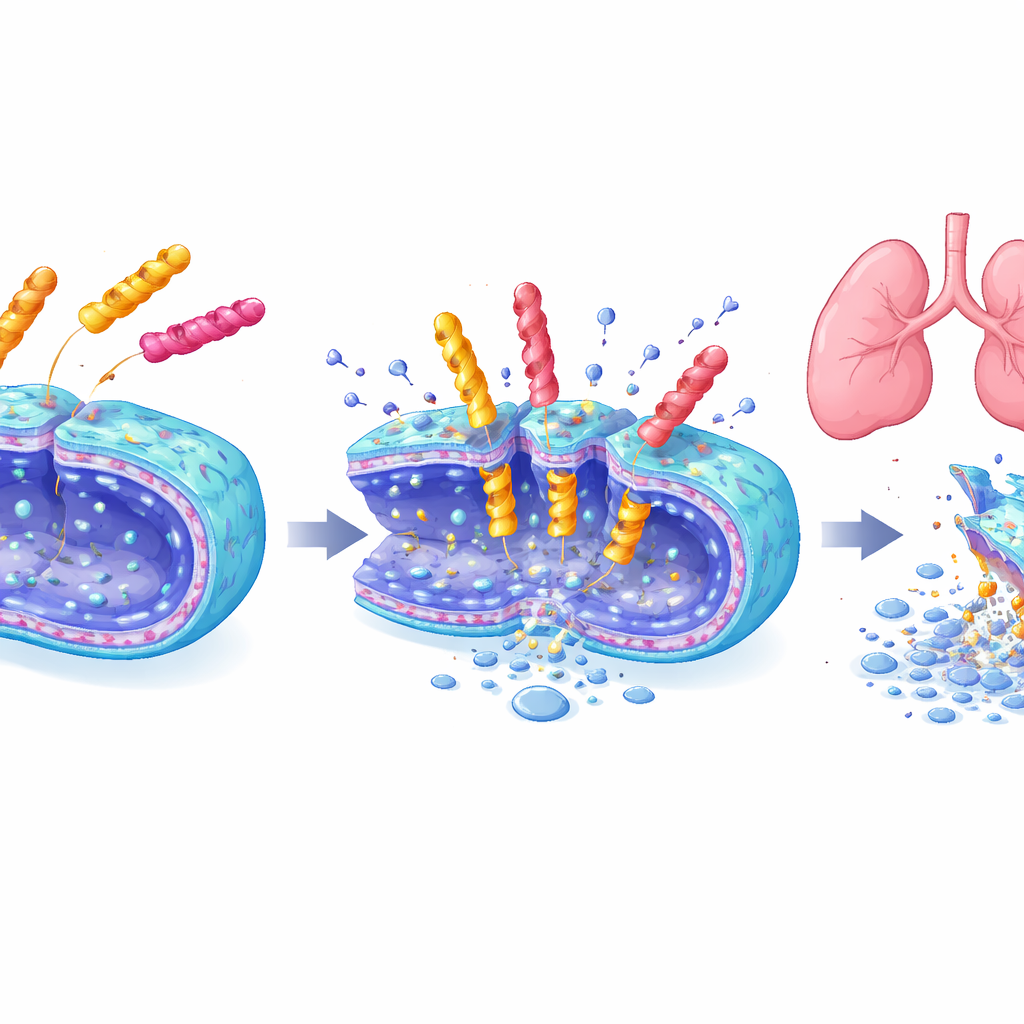
Drei Leitpeptide — jeweils eines aus den Bibliotheken mit sechs, sieben und acht Bausteinen — wurden eingehend untersucht. Sie vernichteten A. baumannii‑Populationen in Minuten bis Stunden, beschädigten bakterielle Membranen, wie unter Elektronenmikroskopen sichtbar, und wirkten auch gegen mehrere andere gefährliche Mikroben. Zugleich richteten sie kaum Schaden an kultivierten Säugetierzellen oder an roten Blutkörperchen an, im Gegensatz zu einigen bestehenden antimikrobiellen Peptiden. In Langzeit‑Expositionstests entwickelten Bakterien nicht leicht Resistenzen gegen diese neuen Moleküle, während die Resistenz gegen Polymyxin B schnell zunahm. Am eindrücklichsten war, dass in einem Mausmodell für Lungenentzündung eine inhalative Dosis des Heptapeptids EME7(7) Lungeninfektionen ebenso wirksam beseitigte wie Polymyxin B, dabei aber die Nieren nicht schädigte, wohingegen Polymyxin B deutliche Nierenschäden und erhöhte Blutmarker für Nierenstress hervorrief.
Was das für künftige Medikamente bedeutet
Diese Arbeit zeigt, dass eine sorgfältig gestaltete KI‑Pipeline aus einem winzigen, unvollständigen Datensatz eine leistungsfähige Maschine zur Entdeckung neuer antimikrobieller Peptide machen kann. Durch die Kombination von breitem Vortraining, schrittweiser Feinabstimmung und mehreren Filterebenen erkundeten die Forschenden effizient ganze Bibliotheken kurzer Peptide und fanden Kandidaten, die sowohl einen gefährlichen Krankenhaus‑Superkeim bekämpfen als auch für lebenswichtige Organe sicherer erscheinen. Die gleiche Strategie gelang auch bei der Suche nach Peptiden, die gegen den Pilzpathogen Candida albicans aktiv sind, was darauf hindeutet, dass sie wiederverwendet werden könnte, um viele andere Typen therapeutischer Peptide zu finden. Für Patientinnen und Patienten könnte dieser Ansatz schließlich in neue Medikamente münden, die hartnäckige Infektionen behandeln, ohne die schweren Nebenwirkungen und die rasche Resistenzentwicklung, die heutige letzte Reserveantibiotika plagen.
Zitation: Huang, J., Zhang, W., Wang, A. et al. Discovery of antimicrobial peptides targeting Acinetobacter baumannii via a pre-trained and fine-tuned few-shot learning-based pipeline. Nat Commun 17, 2475 (2026). https://doi.org/10.1038/s41467-026-69306-2
Schlüsselwörter: antimikrobielle Peptide, Antibiotikaresistenz, Acinetobacter baumannii, maschinelles Lernen Medikamentenentdeckung, Few‑Shot‑Learning