Clear Sky Science · de
Die vorhersehbaren Bindungskinetiken von DNA‑PAINT nutzen, um Superauflösungsbilder zu entrauschen
Schärfere Einblicke in die winzige Welt
Moderne Mikroskope können inzwischen einzelne Moleküle in Zellen „sehen“, doch diese Bilder sind oft von irreführenden Hintergrundpunkten durchsetzt. Diese Studie stellt eine Methode vor, um solche Bilder zu säubern, indem sie die natürliche Art nutzt, wie DNA‑Stücke sich über die Zeit anlagern und wieder lösen. Das Ergebnis sind klarere Darstellungen der molekularen Maschinerie in Zellen, was von grundlegender Biologie bis zur Wirkstoffforschung wichtig ist.
Wie ein Blinktrick verborgene Details offenbart
Eine leistungsfähige Bildgebungstechnik, DNA‑PAINT genannt, macht sich das zufällige Anhaften kurzer DNA‑Stränge für die Superauflösung zunutze. Ein DNA‑Strang ist an das Zielprotein gekoppelt; ein komplementärer Strang mit einem Fluorophor schwimmt in Lösung. Bindet der freie Strang kurz an seinen Partner, erzeugt das einen winzigen Lichtblitz. Durch das Aufzeichnen vieler solcher Blinks und das exakte Bestimmen ihrer Positionen können Forschende die Lage von Proteinen mit Nanometerpräzision rekonstruieren — deutlich schärfer als mit konventionellen Lichtmikroskopen.
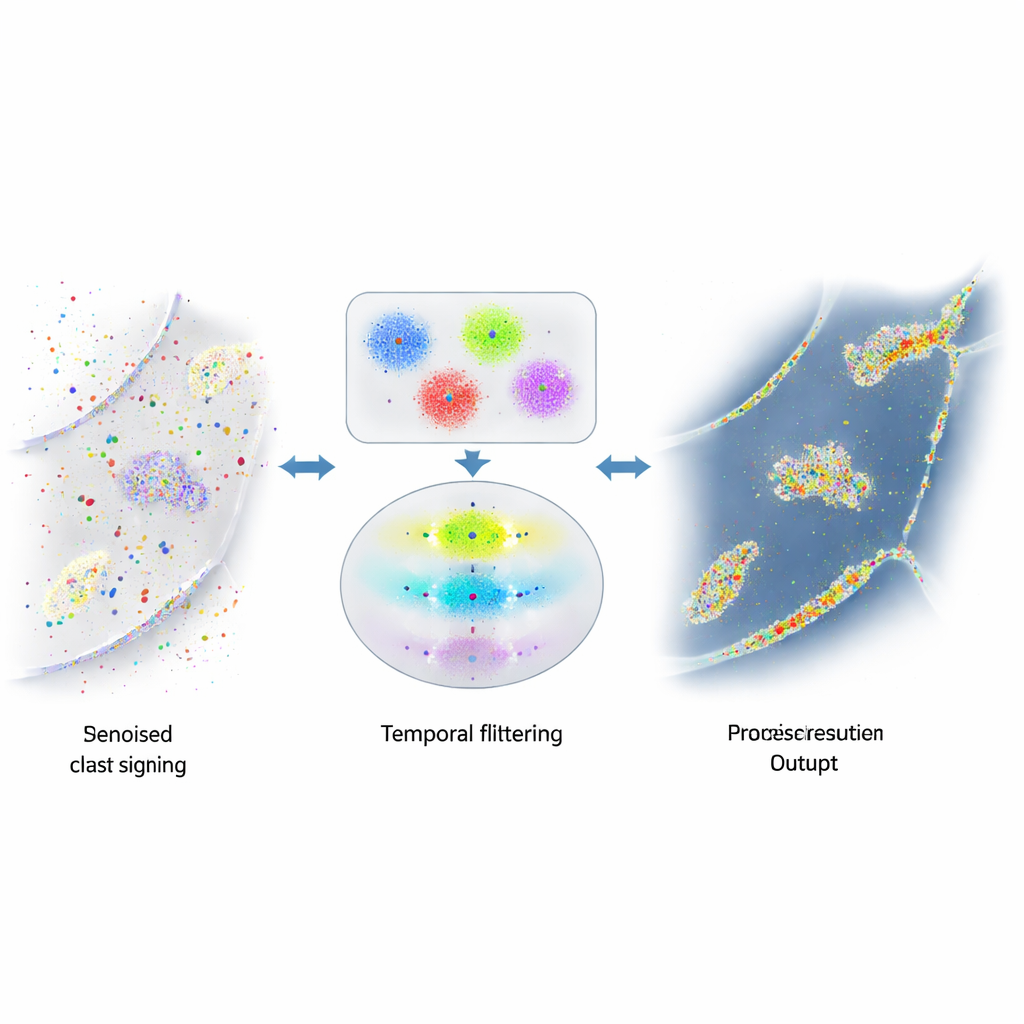
Wenn nützliche Signale im Rauschen untergehen
Die Stärke von DNA‑PAINT — viele frei bewegliche fluoreszierende Stränge — schafft auch ein Problem. Diese Stränge haften gelegentlich dort, wo sie nicht sollten, zum Beispiel an zufälligen Zelloberflächen oder an der zahlreichen DNA im Zellkern. Diese zufälligen Blitze sehen genauso aus wie die echten und überladen das Endbild mit falschen Punkten und Clustern. Frühere Ansätze zur Rauschminderung konzentrierten sich darauf, die Chemie zu verändern, um unerwünschtes Anhaften seltener zu machen, oder auf grobe Regeln, um offensichtliche Ausreißer zu erkennen. Dennoch blieb eine bedeutende Menge irreführenden Signals bestehen und begrenzte die Zuverlässigkeit bei der Bestimmung von Proteinmengen oder räumlichen Beziehungen.
Zeit nutzen, um Wahrheit von Täuschung zu trennen
Die Autorinnen und Autoren erkannten, dass echte DNA‑Paare in DNA‑PAINT einer einfachen Zeitregel folgen: Die Pausen zwischen echten Bindungsereignissen zeigen ein vorhersehbares, exponentielles Muster. Zufällige Haftereignisse tun dies nicht. Sie entwickelten einen mehrstufigen Algorithmus, der zunächst nahe beieinander liegende Blinks anhand ihres Orts in kleine Cluster gruppiert und dafür eine Kombination aus dichtebasiertem Clustering und k‑means verwendet, um komplexe Formen in lokalisierungsgroße Einheiten zu zerlegen. Für jedes Cluster erstellen sie anschließend eine „Zeitspur“ der Bindungsereignisse und fassen dabei sorgfältig schnelle Ein‑Aus‑Blinkfolgen desselben Bindungsereignisses zu einem einzelnen Ereignis zusammen. Abschließend wenden sie einen statistischen Test an, um zu prüfen, ob die Abstände zwischen Ereignissen in jedem Cluster dem erwarteten exponentiellen Verhalten entsprechen. Cluster, die den Test bestehen, werden als echt gewertet; jene, die ihn nicht bestehen, werden als Rauschen verworfen.
Die Methode an echten Zellen geprüft
Um ihren Ansatz zu testen, bildete das Team das Zelladhäsionsprotein E‑Cadherin in Fruchtfliegen‑Eihüllen ab, wobei manche Zellen das markierte Protein produzierten und benachbarte Zellen nicht. So entstanden nebeneinander liegende Bereiche mit echtem Signal und Bereiche, die nur Hintergrund enthalten sollten. Durch Einstellen, wie viele Bindungsereignisse ein Cluster zeigen muss, bevor es geprüft wird, fanden sie Parameter, die über 90 % der fehlerhaften Cluster entfernten, während mehr als 98 % der echten Cluster an Zellgrenzen erhalten blieben. In entrauschten Bildern wurden feine Strukturen wie dünne röhrenförmige Gebilde und Vesikel deutlich sichtbarer. Dieselbe Strategie funktionierte in anderen Systemen, einschließlich Mitochondrien und Mikrotubuli, und sogar bei Proteinen mit diffuser, amorpher Verteilung, bei denen räumliche Muster allein keinen Hinweis auf Echtheit geben.
Klarere molekulare Karten für künftige Studien
Indem diese Methode dem „Rhythmus“ der DNA‑Bindung zuhört, statt nur zu betrachten, wo Blinks auftreten, entfernt sie zuverlässig irreführenden Hintergrund aus DNA‑PAINT‑Daten. Für Nichtfachleute ist das Ergebnis einfach: schärfere, verlässlichere molekulare Karten innerhalb von Zellen. Das erleichtert das Zählen von Proteinmolekülen, die Abschätzung, wie eng verschiedene Proteine beieinander liegen, und das Erstellen genauerer Bilder des inneren Lebens von Zellen. Da die DNA‑basierte Bildgebung weiter wächst, wird eine solche intelligente Entrauschung wesentlich sein, um rohe, punktartige Bilder in belastbare biologische Erkenntnisse zu verwandeln.
Zitation: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Schlüsselwörter: DNA-PAINT, Superauflösungsmikroskopie, Bildentrauschung, Einzelmolekülbildgebung, Proteinabbildung