Clear Sky Science · de
STING-Aktivierung löst zytotoxische und Immunantworten in Meningeomen über inflammatorische Zelltodwege aus
Die körpereigenen Alarmsignale gegen Hirntumoren richten
Meningeome gehören zu den häufigsten Hirntumoren; obwohl Operation und Strahlentherapie oft hilfreich sind, kehren manche Tumoren immer wieder zurück. Diese hartnäckigen Wucherungen können Krampfanfälle, Kopfschmerzen und Behinderungen verursachen, und es gibt bislang keine breit akzeptierten medikamentösen Therapien. Diese Studie untersucht einen Ansatz, bei dem die Tumorzellen und die benachbarten Immunzellen ein starkes internes Alarmsignal aussenden sollen, mithilfe eines Moleküls, das ein angeborenes Gefahren-Erkennungssystem namens STING aktiviert. Ziel ist es, nicht nur Tumorzellen direkt zu töten, sondern auch das Immunsystem zu wecken und das dichte Gerüst des Tumors aufzubrechen.
Ein Tumor in einer ruhigen immunologischen Nachbarschaft
Die Autoren kartierten zunächst die zelluläre „Nachbarschaft“ in menschlichen Meningeomen mittels Einzelzellsequenzierung und räumlicher Bildgebung. Sie fanden, dass diese Tumoren reich an angeborenen Immunzellen sind, insbesondere Makrophagen, während klassische tumorbekämpfende T‑Zellen und natürliche Killerzellen (NK‑Zellen) selten und häufig erschöpft waren. Um die Tumorzellen liegt eine dichte Schale aus Kollagen und anderen Matrixproteinen, die eine gepanzerte, geschichtete Struktur bildet. Viele Makrophagen in diesen Regionen tragen inhibitorische Rezeptoren, die durch Kollagen aktiviert werden und so eine stark unterdrückte Umgebung schaffen, in der Immunzellen zwar vorhanden, aber daran gehindert sind, gegen den Krebs vorzugehen.
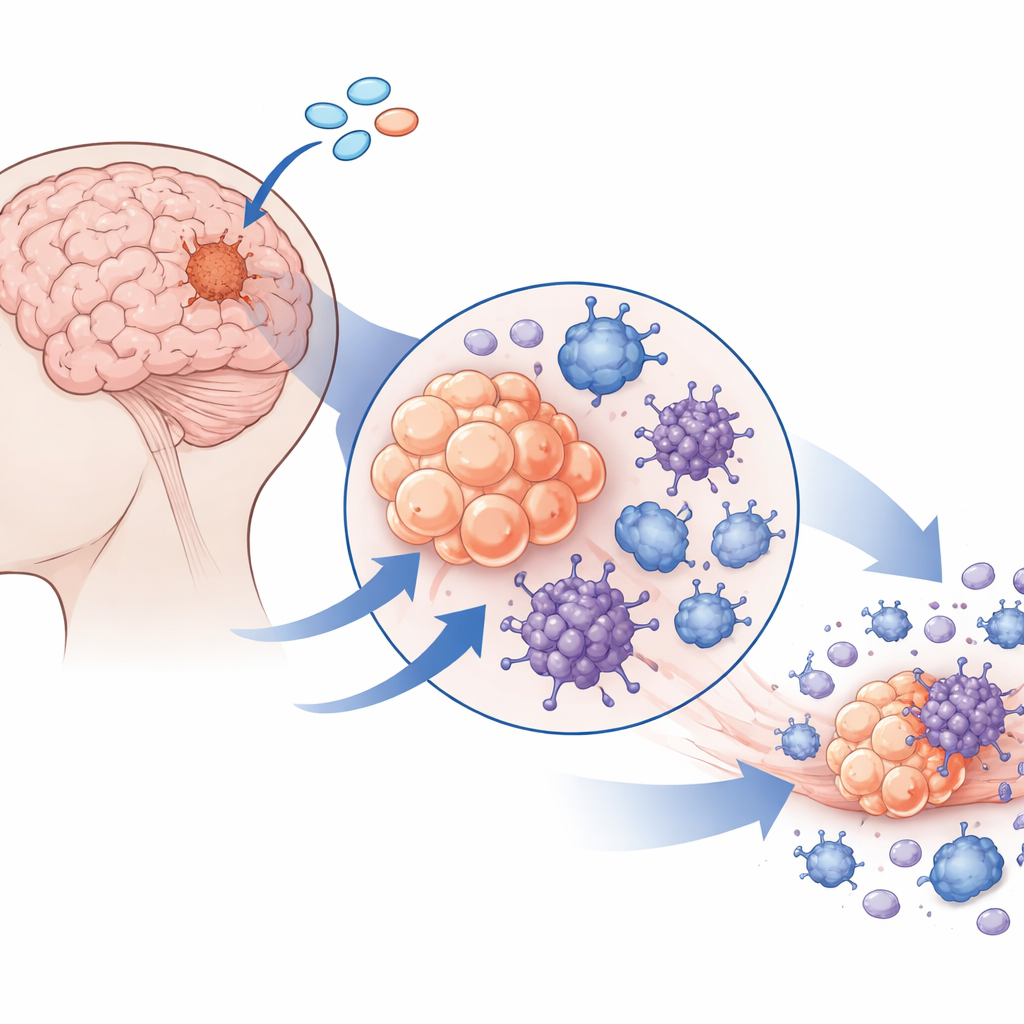
Eine Schaltfläche entdecken, die Tumorzellen noch besitzen
Als Nächstes suchte das Team nach Signalwegen, die dieses unterdrückte Milieu in ein entzündetes, tumorschädliches umschalten könnten. Sie konzentrierten sich auf STING, einen Sensor, der normalerweise auf fehlplatziertes DNA‑Material in Zellen reagiert und antivirale sowie entzündliche Antworten auslöst. Im Gegensatz zu vielen anderen Hirntumoren zeigten Meningeomzellen ungewöhnlich hohe STING‑Spiegel. Das hing mit offener Chromatinstruktur und niedriger DNA‑Methylierung am STING‑Gen zusammen, was bedeutet, dass das Gen epigenetisch dafür bereitsteht, aktiv zu sein. STING war nicht nur in Tumorzellen reichlich vorhanden, sondern auch in benachbarten Gefäßzellen und Makrophagen, was darauf hindeutet, dass ein einziges Medikament gleichzeitig viele Schlüsselakteure in der Tumormikroumgebung beeinflussen könnte.
Tumorzellen zum feurigen Selbstzerstören zwingen
Die Forscher behandelten frisch entnommene Patientenproben von Meningeomen mit einem potenten STING‑Agonisten namens 8803. Selbst wenn Immunzellen entfernt wurden, starben Tumorzellen, was einen direkten Effekt belegt. Durch Zugabe von Wirkstoffen, die selektiv verschiedene Zelltodwege blockieren, und durch Analyse der Genaktivität zeigten sie, dass 8803 nicht einfach stille Apoptose auslöste. Stattdessen trieb es Meningeomzellen in mehrere entzündliche Formen des Zelltods — Pyroptose, Nekroptose und Ferroptose — bei denen Zellen aufplatzen, anstatt ordentlich demontiert zu werden. Ein entscheidender Schritt war die Aktivierung und Spaltung eines Proteins namens Gasdermin D, das Poren in der Zellmembran bildet. Elektronenmikroskopie zeigte Tumorzellen mit durchlöcherten Membranen und geschädigten Mitochondrien; das Blockieren reaktiver Sauerstoffspezies verringerte die Abtötung, was mitochondrialen Stress mit diesem feurigen Untergang verknüpft.
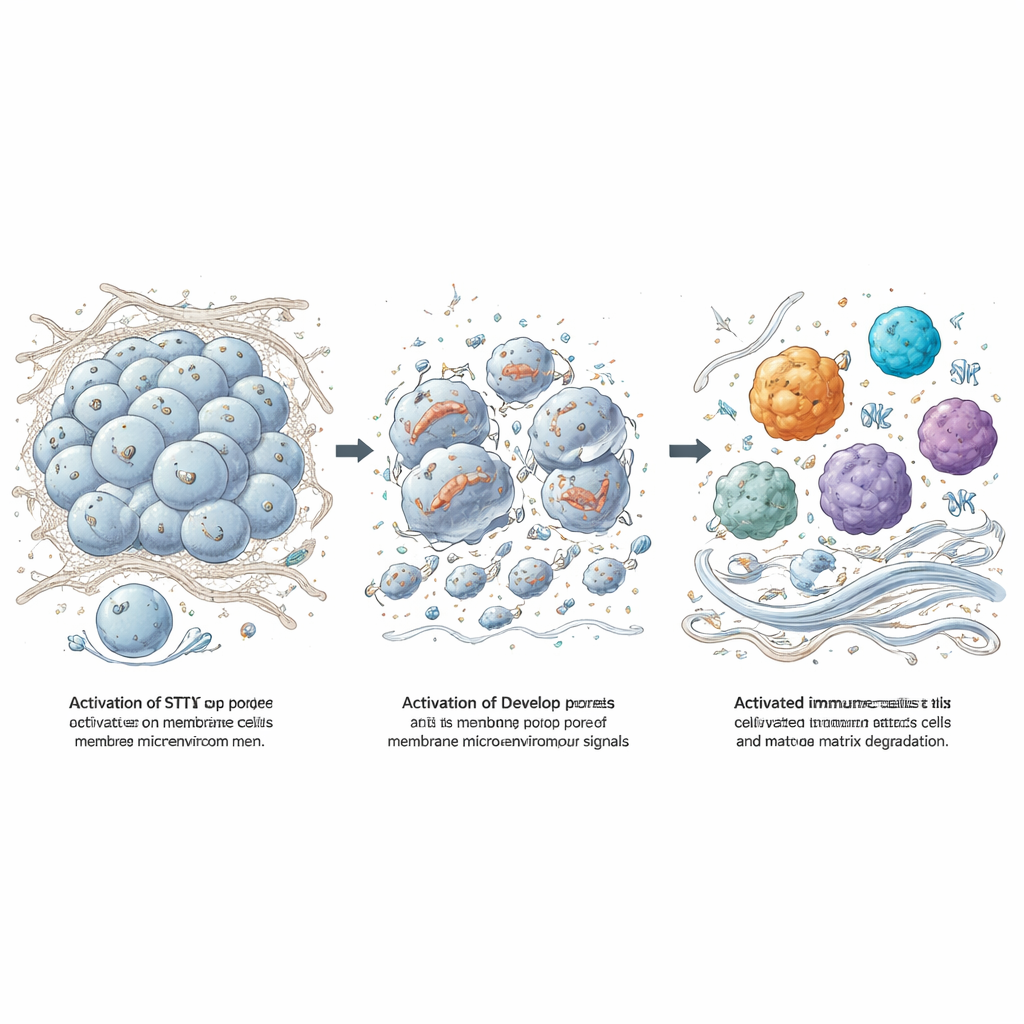
Von Tumortrümmern zu Immunaktivierung und Matrixabbau
Wenn Tumorzellen auf diese dramatische Weise sterben, geben sie „Gefahr“-Moleküle frei, die Immunzellen aufrütteln können. Das Team setzte Mausmakrophagen lysierten Meningeomzellen aus und beobachtete einen Anstieg entzündlicher Faktoren und von Enzymen, die Kollagen abbauen, insbesondere die Matrix‑Metalloproteinase‑3 (MMP‑3). Arbeiten mit Mäusen, denen bestimmte Signaladapter fehlten, zeigten, dass Toll‑like‑Rezeptoren, ein weiteres Gefahrenerkennungssystem, für diese Reaktion entscheidend sind, während die STING‑Aktivierung durch 8803 eine zusätzliche Schicht der Immunstimulation beiträgt. In Mausmodellen von Meningeomen führten direkte Injektionen von 8803 in die Tumoren zu Schrumpfung oder Stabilisierung des Wachstums, verlängerten das Überleben und verwandelten den Tumorbereich von einer ruhigen, kollagenreichen Masse in eine Stelle, die von aktiven Makrophagen, NK‑Zellen, T‑Zellen und deutlich reduzierter Kollagenfärbung geprägt war.
Warum dieser Ansatz die Behandlung von Patienten verändern könnte
Insgesamt zeigt die Studie, dass Meningeome eine eingebaute Verwundbarkeit besitzen: Ihre Tumorzellen behalten einen zugänglichen STING‑Schalter, der durch 8803 umgelegt werden kann und sie in explosive, entzündliche Formen des Zelltods treibt. Dieser Prozess tötet Krebszellen und überflutet zugleich die Umgebung mit Alarmsignalen, die Immunzellen anziehen und aktivieren, und hilft außerdem, das Kollagengerüst abzutragen, das zur Raumforderung beiträgt. Weil Meningeome typischerweise lokal begrenzt und nicht weit metastasierend sind und weil die Standardoptionen bei rezidivierender Erkrankung begrenzt sind, könnte ein lokal applizierter STING‑Agonist wie 8803 eine neue, gezielte Möglichkeit bieten, Tumormasse zu reduzieren und die immunologische Umgebung nachhaltig umzuprogrammieren.
Zitation: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Schlüsselwörter: Meningeom, STING-Signalweg, Immuntherapie bei Hirntumoren, inflammatorischer Zelltod, Tumormikroumgebung