Clear Sky Science · de
Erklärbare KI-gestützte Analyse menschlicher Pankreas-Abschnitte identifiziert Merkmale von Typ-2-Diabetes
Warum diese Forschung für die tägliche Gesundheit wichtig ist
Typ-2-Diabetes betrifft Hunderte Millionen Menschen, dennoch fällt es Ärzten weiterhin schwer, klare physische Zeichen der Krankheit im Inneren der Bauchspeicheldrüse — dem Organ, das Insulin produziert — zu erkennen. Diese Studie nutzt leistungsfähige künstliche Intelligenz in Kombination mit fortschrittlicher Mikroskopie, um subtile Muster im menschlichen Pankreasgewebe zu lesen, die für das bloße Auge unsichtbar sind. Dadurch werden neue strukturelle Merkmale aufgedeckt, die mit Typ-2-Diabetes verknüpft sind, und es ergeben sich neue Ansatzpunkte für Diagnose, Prävention und Therapie.
Die Bauchspeicheldrüse in beispielloser Detailtiefe betrachten
Traditionell haben Wissenschaftler Pankreasgewebe von verstorbenen Spendern untersucht, um Veränderungen zu finden, die mit Typ-2-Diabetes assoziiert sind, etwa Narbenbildung, Fettablagerungen oder Verlust insulinproduzierender Zellen. Diese Untersuchungen lieferten eine lange Liste möglicher Auffälligkeiten, doch keine war zuverlässig genug, damit Pathologen allein anhand eines Objektträgers sicher sagen könnten, ob eine Person Diabetes hatte. In dieser Arbeit stellten die Forschenden eine einzigartige Sammlung von Ultra-High-Resolution-Bildern aus Pankreasproben zusammen, die während Operationen von 100 lebenden Spendern entnommen wurden — 35 mit Typ-2-Diabetes und 65 ohne. Jede Probe wurde auf verschiedene Weise gefärbt, um unterschiedliche Zelltypen hervorzuheben: hormonproduzierende Zellen in den Inseln, Blutgefäße, Fettzellen und Nervenfasern. Dieser reichhaltige visuelle Datensatz ist für einen Menschen zu komplex, um vollständig zu verarbeiten — genau hier zeigt künstliche Intelligenz ihre Stärke. 
KI darauf trainieren, das diabetische Pankreas zu erkennen
Das Team trainierte Deep-Learning-Modelle, um Gewebe von Personen mit und ohne Typ-2-Diabetes zu unterscheiden. Da jedes Ganzglasbild Milliarden von Pixeln enthält, teilten sie die Bilder zunächst in viele kleine Patches auf. Ein vortrainierter Vision Transformer extrahierte Merkmale aus jedem Patch, und ein spezialisierter Multiple-Instance-Learning-Klassifikator verband dann die Informationen aus allen Patches einer ganzen Probe, um zu entscheiden, ob sie von einem diabetischen oder nicht-diabetischen Spender stammte. Um Überanpassung zu vermeiden, nutzten sie wiederholte Kreuzvalidierung und mittelten anschließend die Vorhersagen von 15 separaten Modellen. Die beste Leistung erzielten multiplexe Fluoreszenzaufnahmen, die gleichzeitig Alpha-Zellen, Delta-Zellen und Nervenfasern hervorhoben, und erreichten eine Fläche unter der Kurve von 0,956 — ein starkes Indiz dafür, dass die KI zuverlässig diabetesbezogene Muster „sehen“ konnte, die Pathologen bislang nicht formalisiert haben.
Die Blackbox erklären lassen
Alleinige Vorhersagen waren jedoch nicht das Ziel; den Autoren ging es um biologische Einsichten. Deshalb setzten sie erklärbare KI-Techniken ein, die zeigen, auf welche Regionen und Pixel das Modell bei seinen Entscheidungen geachtet hat. Aufmerksamkeitskarten hoben die einflussreichsten Bereiche über ganze Objektträger hinweg hervor, während Attributionsmethoden bis auf die Ebene einzelner Zellen und Strukturen hineinzoomten. Um diese farbigen Heatmaps in Zahlen zu überführen, trainierte das Team separate Segmentierungsnetze, die automatisch Inseln, Fettzellcluster und Binde- (fibrotisches) Gewebe umreißen konnten. Anschließend quantifizierten sie Merkmale wie Inselgröße, gesamte Fettfläche, Anzahl der Fettcluster, Abstand zwischen Inseln und nahegelegenen Fettdepots sowie Ausmaß der Fibrose und analysierten, wie diese „histologischen Biomarker“ sich auf den Diabetesstatus und die Insulinsekretion bezogen — unter Berücksichtigung von Alter, Geschlecht, Body-Mass-Index und weiteren klinischen Faktoren. 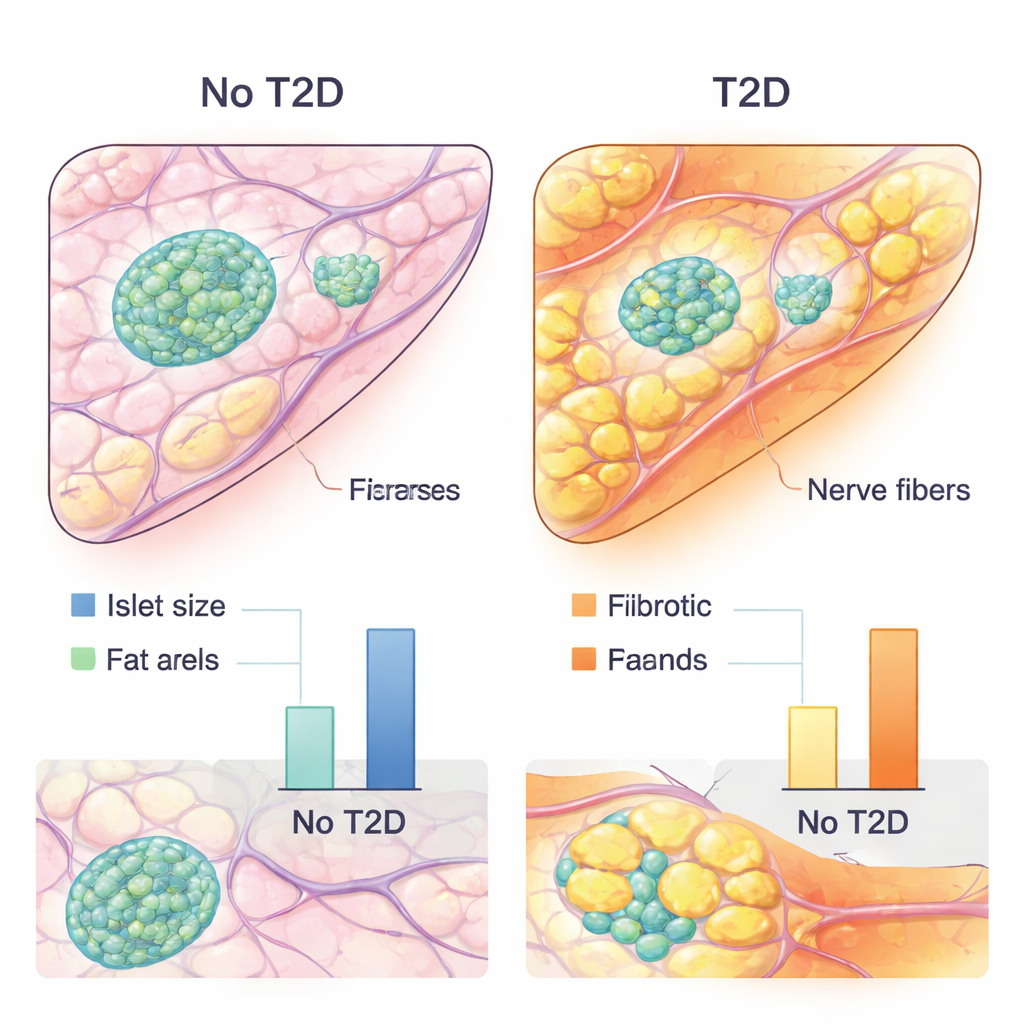
Neue Hinweise: Fett, Nerven, Narben und Schrumpfung der Inseln
Die KI-gestützte Analyse offenbarte mehrere konsistente Merkmale des diabetischen Pankreas. Menschen mit Typ-2-Diabetes hatten tendenziell kleinere Inseln und größere Fettzellcluster innerhalb der Bauchspeicheldrüse. Wichtig ist, dass die Inseln bei diabetischen Spendern näher an diesen Fettablagerungen lagen, was auf einen direkteren lokalen Einfluss des Fettgewebes auf hormonproduzierende Zellen hindeutet. Auch die Menge an verbindendem, narbenähnlichem Gewebe war bei Diabetes erhöht und mit einer schlechteren Insulinsekretion verknüpft. Gleichzeitig legten die KI-Modelle überraschend großen Wert auf Strukturen, die für Tubulin beta 3 gefärbt waren — einen Marker für Nervenfasern — insbesondere wenn diese Fasern durch oder in der Nähe von Inseln verliefen. Dies deutet auf Veränderungen der Pankreasinnervation hin — also darauf, wie Nerven mit Inselzellen interagieren — als potenziell wichtigen und bislang unterschätzten Beitrag zu Typ-2-Diabetes. Zusammengenommen legen diese Befunde nahe, dass nicht nur die Betazellen selbst zählen, sondern auch ihre Nachbarschaft: nahegelegene Fettzellen, Narbengewebe, Blutgefäße und Nerven scheinen alle die Gesundheit der Inseln mitzuformen.
Was das für die künftige Versorgung bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: Typ-2-Diabetes hinterlässt einen subtilen, aber erkennbaren Abdruck in der Architektur der Bauchspeicheldrüse. Durch die Kombination hochauflösender Bildgebung mit erklärbarer KI übersetzt diese Studie jene Muster in messbare Merkmale — wie Inselgröße, Fettverteilung, Nervenvorkommen und Fibrose —, die mit Diabetes und der verbleibenden Insulinproduktionsfähigkeit korrelieren. Zwar ist dieser Ansatz noch kein diagnostisches Werkzeug für die Routineversorgung, er bietet jedoch eine kraftvolle Roadmap zur Entdeckung neuer Wirkstoffziele und zur Verfeinerung unseres Verständnisses der Diabetesentstehung. Langfristig könnten Erkenntnisse aus solcher KI-gestützter Gewebeanalyse Ärzten helfen, besser vorherzusagen, wer gefährdet ist, den Krankheitsverlauf zu überwachen und Therapien zu entwickeln, die nicht nur Betazellen, sondern auch das umliegende pankreatische Umfeld schützen.
Zitation: Klein, L., Ziegler, S., Gerst, F. et al. Explainable AI-based analysis of human pancreas sections identifies traits of type 2 diabetes. Nat Commun 17, 1558 (2026). https://doi.org/10.1038/s41467-026-69295-2
Schlüsselwörter: Typ-2-Diabetes, Pankreas, künstliche Intelligenz, Histopathologie, Biomarker