Clear Sky Science · de
Phyllosilikat-Adsorption begrenzte die Phosphor-Bioverfügbarkeit in frühen ferruginösen Ozeanen
Warum frühe Ozeane heute wichtig sind
Phosphor ist ein stiller Arbeitspferd des Lebens: Er baut Zellmembranen, DNA und die energietragenden Moleküle in allen Organismen auf. Auf der frühen Erde aber dürfte dieses lebenswichtige Element für Mikroben überraschend schwer zu bekommen gewesen sein. Diese Studie untersucht, wie verbreitete tonähnliche Minerale in eisenreichen, sauerstoffarmen alten Meeren Phosphor an sich banden, transportierten und einen Großteil davon in Meeresbodensedimenten einschlossen. Das Verständnis dieses verborgenen Verkehrs hilft zu erklären, warum Leben und Sauerstoff so lange brauchten, um unseren Planeten zu verändern.

Der Schlüsselbaustein des Lebens mit einem Versorgungsproblem
Heute gelangt Phosphor hauptsächlich durch Verwitterung von Gesteinen an Land in die Ozeane, Flüsse transportieren ihn zum Meer, und Mineralien sowie Organismen binden, recyceln und vergraben ihn schließlich in Sedimenten. Der größte Teil des für Lebewesen zugänglichen Phosphors sitzt vorübergehend an Mineraloberflächen oder in organischer Substanz, nicht in widerstandsfähigen Kristallen. Vor Milliarden von Jahren sah die Erdoberfläche jedoch ganz anders aus: die Atmosphäre war sauerstoffarm, die Ozeane reich an gelöstem Eisen, und die Chemie von Fluss- und Meerwasser wich stark vom heutigen Zustand ab. Wissenschaftler haben diskutiert, ob frühe Ozeane an Phosphor mangelten oder gelegentlich damit überschwemmt wurden und welche Rolle Tonsilikate — dünne, blattartige Silikate, bekannt als Phyllosilikate — beim Transport und der Speicherung dieses Nährstoffs spielten.
Experimente, die frühe Gewässer nachstellen
Die Autoren stellten frühes Fluss- und Meerwasser im Labor unter sauerstofffreien Bedingungen nach und verwendeten realistische Mischungen aus Salzen, Eisen und gelöstem Siliziumdioxid. Dann maßen sie, wie viel gelöstes Phosphat (die hauptsächliche gelöste Form von Phosphor) an mehrere verbreitete Phyllosilikate gebunden wurde: aluminiumreiche Tone wie Kaolinit und Montmorillonit sowie eisen- und magnesiumreiche Tone wie Lizardit und Nontronit, die bei der seafloor-Alteration vulkanischer Gesteine entstehen. In vielen Tests steigerte das Hinzufügen moderater Mengen an gelöstem Eisen in seiner reduzierten Form, Fe(II), die Phosphatadsorption auf diesen Mineralien deutlich, während hohe Werte gelösten Siliziums diese Adsorption tendenziell schwächten. Mikroskopie und Spektroskopie bestätigten, dass Phosphor an vorhandene Mineraloberflächen anhing und nicht neue Phosphatkristalle bildete.
Wie Eisen den Tonen hilft, Phosphor zu binden
Warum ist Fe(II) so wirksam? Mit molekularen Simulationen zeigte das Team, dass zweiwertige Metallionen, besonders Fe(II), als nanoskalige Brücken zwischen negativ geladenen Phosphatgruppen im Wasser und den ebenfalls negativ geladenen Tonoberflächen fungieren. Diese Metalle können in der Nähe der Mineraloberfläche sitzen und gleichzeitig Phosphat binden, elektrische Abstoßung überwinden und Phosphor am Ton verankern. Fe(II) bindet stärker sowohl an Phyllosilikate als auch an Phosphat als Calcium oder Magnesium, die anderen dominierenden zweiwertigen Ionen im Meerwasser, und hat dadurch in eisenreichen frühen Ozeanen einen überproportionalen Einfluss. Die Simulationen zeigten außerdem, dass Phosphatarten, die bei leicht saurem pH häufiger vorkommen, weniger stark binden, was erklärt, warum die Adsorption mit der Wasseracidität variierte. Gelöstes Siliziumdioxid konkurriert wiederum mit Phosphat um dieselben Oberflächenplätze und verdrängt Phosphor, wenn Konzentrationen und pH-Wert hoch genug sind.
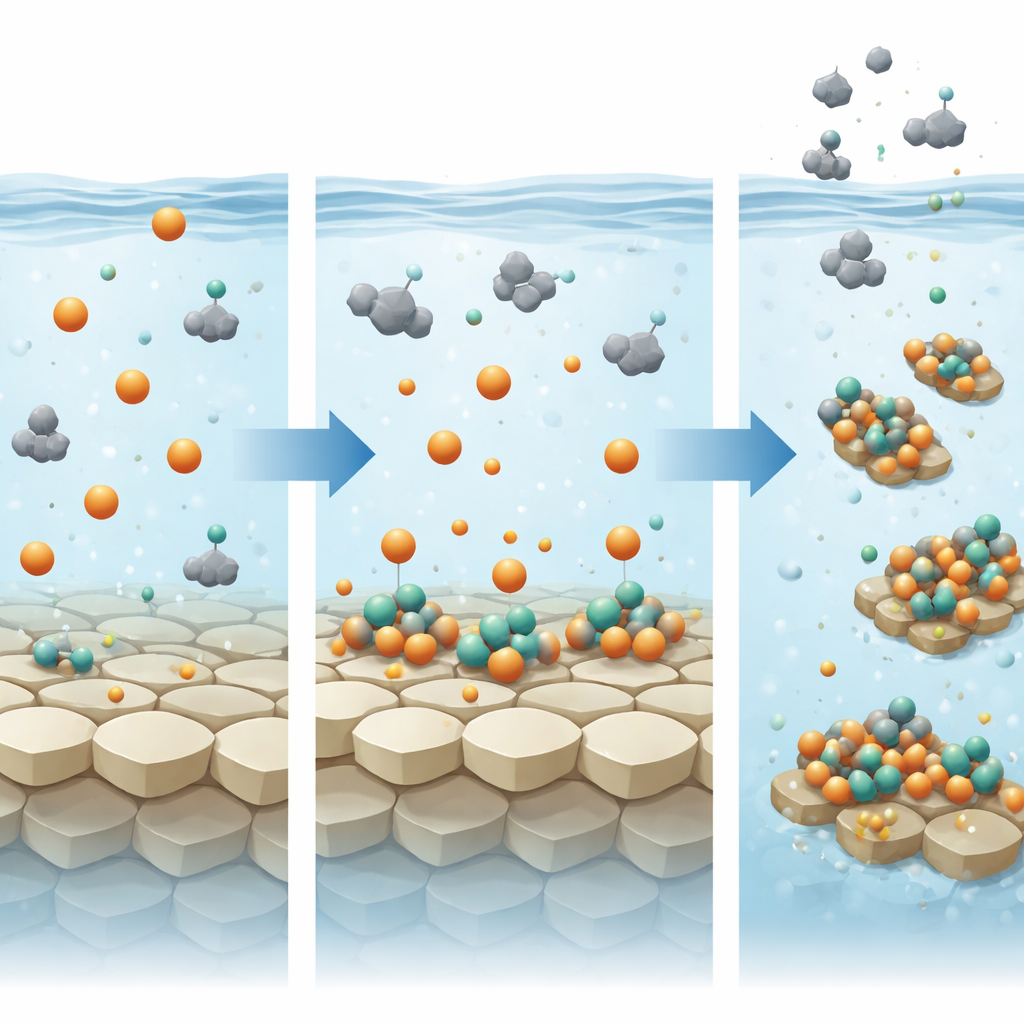
Transport und Verlagerung von Phosphor auf einem sich verändernden Planeten
Mit diesen mechanistischen Einsichten bauten die Autoren einfache probabilistische Modelle, um von Laboransätzen zu globalen Bilanzen zu skalieren. Als Kontinente im späten Archaikum aufstiegen und die Verwitterung zunahm, erzeugten Flüsse wahrscheinlich reichlich Tonpartikel. Die Ergebnisse deuten darauf hin, dass diese Tone in eisenreichen Flüssen große Mengen Phosphat aufsaugten und während des Transports die dominante Form biologisch verfügbaren Phosphors bildeten. Sobald diese Partikel Küstenmeere erreichten, förderte die Anwesenheit von Fe(II), Calcium und Magnesium im Meerwasser eher, dass sie ihre Ladung hielten und noch mehr Phosphor behielten, sodass sie schnell in Sedimente absanken. Separate Simulationen zeigen, dass Phyllosilikate, die direkt durch seafloor-Verwitterung mafischer und ultramafischer Kruste gebildet wurden, ebenfalls eine starke Senke für gelöstes Phosphat darstellten, insbesondere als die Kontinente noch klein und der Flussinput begrenzt war.
Folgen für frühes Leben und Sauerstoff
Setzt man die Erkenntnisse zusammen, argumentiert die Studie, dass Tonminerale in antiken, eisenreichen Ozeanen sowohl als Transportmittel als auch als Tresore für Phosphor fungierten. Sie halfen vermutlich, reaktiven Phosphor vom Land ins Meer zu befördern, verschlossen aber einen Großteil davon schnell in Sedimenten, wo er langsam in stabilere Phosphatminerale umgewandelt wurde. Diese doppelte Rolle hielt die gelösten Phosphorkonzentrationen niedrig, drosselte die marine Produktivität und verzögerte den Aufbau von Sauerstoff in der Atmosphäre, selbst nachdem sauerstoffproduzierende Mikroben entstanden waren. Mit der Zeit, als die Erdoberfläche oxidierte und sich die Eisenchemie veränderte, übernahmen andere Minerale die Hauptaufgabe der Phosphoradsorption und milderten diese Einschränkungen. Indem die Studie nachzeichnet, wie unscheinbare Tone den frühen Phosphorkreislauf gestalteten, hilft sie zu erklären, warum der Aufstieg komplexen Lebens und einer sauerstoffreichen Welt ein langsamer, stufenweiser Prozess war und keine abrupte Revolution.
Zitation: Cui, X., Zhang, Z., Li, Q. et al. Phyllosilicate adsorption limited phosphorus bioavailability in early ferruginous oceans. Nat Commun 17, 2422 (2026). https://doi.org/10.1038/s41467-026-69293-4
Schlüsselwörter: frühe Erdmeere, Phosphorkreislauf, Tonsilikate, archäische Biosphäre, Nährstoffbegrenzung