Clear Sky Science · de
Adgrg6/Gpr126 wird für die Integrität der kompakten Wand und die Festlegung trabekulärer Identität während der kardialen Trabekulation benötigt
Warum die Architektur der Herzwand wichtig ist
Jeder Herzschlag beruht auf einer fein gestalteten inneren Herzwand. In sich entwickelnden Embryonen bildet sich diese Wand zunächst als glatte Schicht und wächst dann zu einem Wald aus muskulären Leisten, den sogenannten Trabekeln, heran, die dem Herzen helfen, effizient zu pumpen. Geht dieser Prozess schief, können Kinder und Erwachsene schwere Kardiomyopathien entwickeln. Diese Studie untersucht, wie ein wenig bekannter Rezeptor, Gpr126, Herzmuskelzellen dabei unterstützt zu entscheiden, ob sie in der glatten Außenwand verbleiben oder Teil dieser inneren Leisten werden.
Ein Rezeptor mit geteilten Funktionen im Herzen
Gpr126 gehört zu einer Familie von Adhesions-G-Protein-gekoppelten Rezeptoren, die in der Zellmembran sitzen und die Umgebung der Zelle wahrnehmen. Diese Rezeptoren sind besonders interessant, weil viele vorhandene Medikamente verwandte Rezeptoren ansprechen, was sie zu attraktiven therapeutischen Kandidaten macht. Gpr126 ist ungewöhnlich, weil es natürlicherweise in zwei Hauptteile gespalten wird: ein N-terminales Fragment (NTF), das aus der Zelle herausragt und bei der Zell–Zell-Adhäsion helfen kann, und ein C-terminales Fragment (CTF), das die Membran durchspannt und interne Signalwege auslöst. Frühere Arbeiten verbanden Gpr126 mit der Herzentwicklung, aber unklar war, welche Rolle die einzelnen Fragmente während der Trabekelbildung tatsächlich spielen.
Zebrafische nutzen, um die Herzentwicklung zu beobachten
Die Forscher nutzten Zebrafische, deren transparente Embryonen Echtzeitaufnahmen des schlagenden Herzens ermöglichen. Sie untersuchten zwei genetische Varianten von gpr126. Die eine (stl47) produziert nur ein winziges, stark verkürztes Protein; die andere (st49) erzeugt ein stabiles, sekretorisches NTF-Fragment, dem der CTF-Signalteil fehlt. Durch Kombination dieser Mutanten mit fluoreszenten Reporterlinien konnte das Team einzelne Herzmuskelzellen sehen, die Bildung der Trabekel verfolgen und Schlüsselmoleküle wie N-Cadherin (das Zellen zusammenhält) und Notch (einen Signalweg, der Zellen sagt, welche Identität sie annehmen sollen) beobachten.
Die Wand zusammenhalten vs. die Leisten bilden
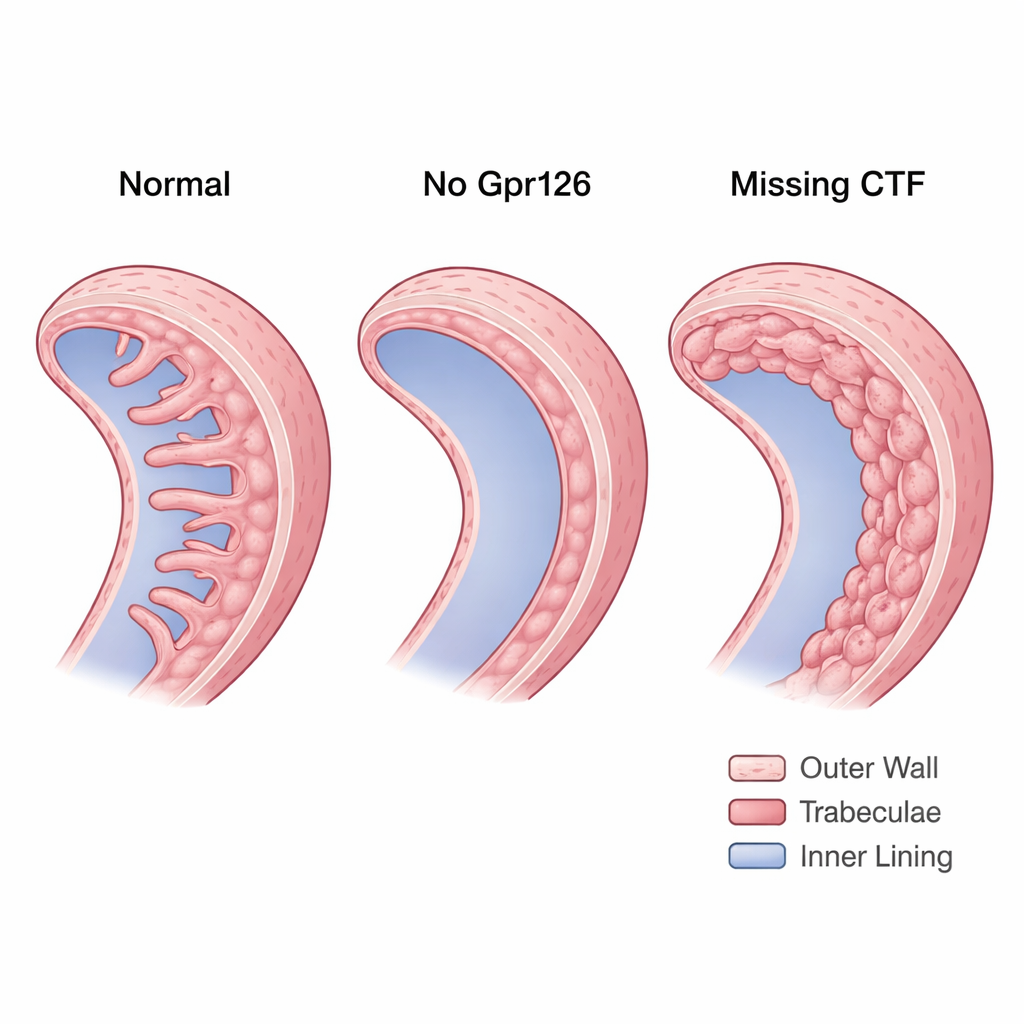
Die stl47-Mutanten, denen im Wesentlichen beide funktionellen Fragmente fehlen, zeigten, dass Gpr126 für die Ausbildung normaler Trabekel erforderlich ist. In maternalen-zygotischen stl47-Embryonen — in denen kein funktionelles Gpr126 von beiden Eltern stammt — entwickelten viele Herzen fehlende oder stark reduzierte Trabekel. N-Cadherin, das in gesunden Herzen sauber an den Seiten der Kardiomyozyten der kompakten Wand konzentriert ist, erschien verteilt über die Zelloberfläche. Diese Desorganisation deutete darauf hin, dass ohne das NTF die Zell–Zell-Adhäsion in der kompakten Wand instabil wird und somit die Grundlage fehlt, auf der Trabekel entstehen sollten.
Zu viel Wand, zu wenig Identität
Die st49-Mutanten, die weiterhin das NTF, aber nicht das CTF produzieren, zeigten das umgekehrte Problem. Statt fehlender Trabekel bildeten ihre Herzen eine dicke, mehrschichtige innere Wand. Die zusätzlichen Schichten waren keine echten Trabekel: Die Zellen blieben polarisiert wie Zellen der kompakten Wand und versäumten es, ihre N-Cadherin-Kontakte in das punktförmige Muster umzubauen, das für leistenbildende Zellen typisch ist. Mit einem Notch-Aktivitätsreporter fand das Team heraus, dass diese Herzen abnorm hohe Notch-Signalgebung im Myokard aufwiesen. Hohe Notch-Aktivität hält bekanntlich Zellen in der kompakten Wand und verhindert, dass sie sich ablösen und zu Trabekeln werden. Wichtig war, dass durch die Wiedereinführung nur des CTF in Endokardzellen Trabekel wiederauftraten und die Notch-Aktivität in Richtung Normalwert sank — ein Beleg dafür, dass CTF-Signalgebung entscheidend ist, um Kardiomyozyten eine trabekuläre Identität zu verleihen.
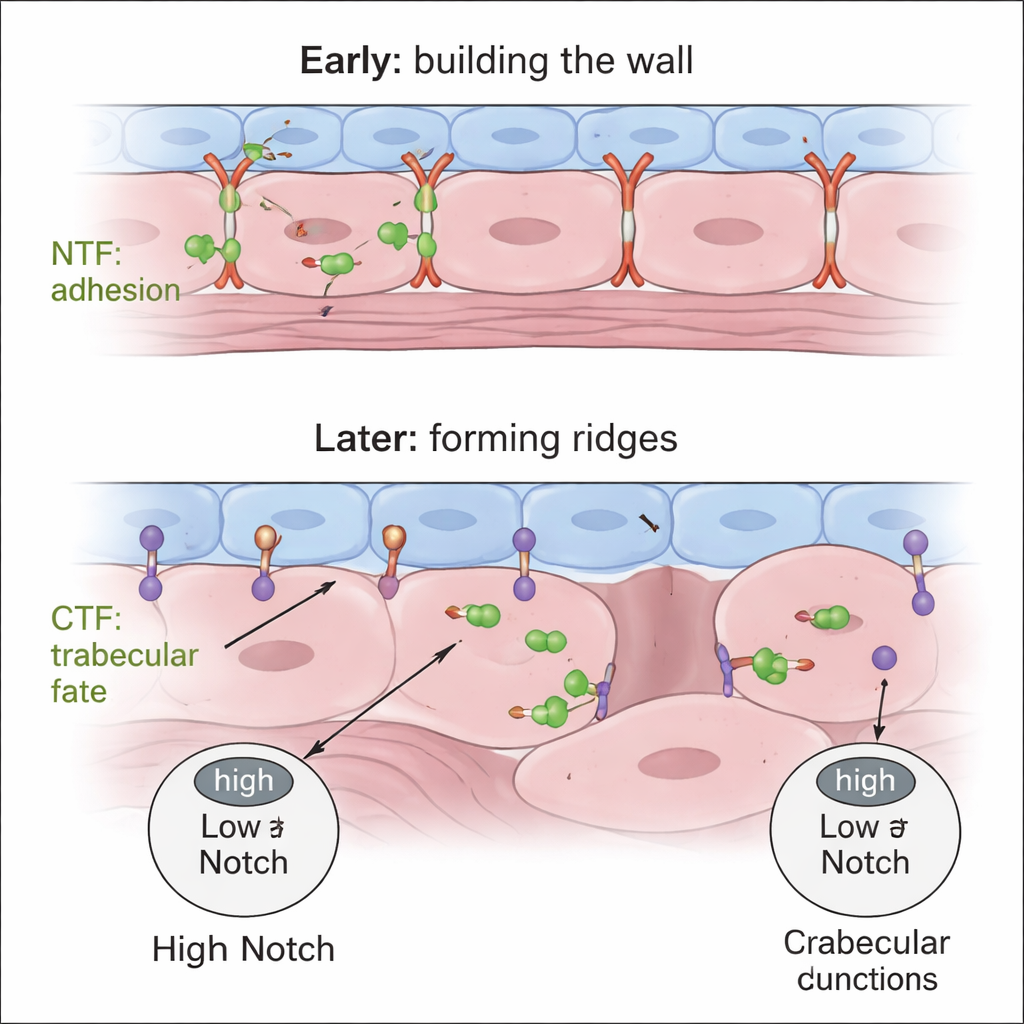
Signale austarieren für ein gesundes Herz
Insgesamt stützen die Ergebnisse ein Zwei-Schritt-, Zwei-Teil-Modell. Zuerst hilft das sekretierte NTF von Gpr126 den Kardiomyozyten der kompakten Wand, enge, korrekt positionierte Verbindungen aufrechtzuerhalten und so eine stabile einschichtige Wand zu sichern. Später moduliert das CTF — aus Endokardzellen wirkend — die myocardiale Notch-Signalgebung, sodass nur einige Kardiomyozyten depolarisieren, ihre Verbindungen lockern und nach innen vorstehen, um Trabekel zu bilden, während ihre Nachbarn in der kompakten Wand verbleiben. Fehlt das NTF, organisiert sich die Wand nie richtig; fehlt das CTF, wächst die Wand übermäßig und die Zellen nehmen keine trabekuläre Identität an. Diese domänenspezifische Kontrolle der Architektur der Herzwand hebt Gpr126 als mögliche Verbindung zwischen Zelladhäsion, Signalwegen wie Notch und strukturellen Herzkrankheiten hervor und legt nahe, dass das gezielte Einstellen unterschiedlicher Teile desselben Rezeptors eines Tages helfen könnte, Entwicklungsfehler zu korrigieren.
Zitation: Srivastava, S., Gunawan, F., Vergarajauregui, S. et al. Adgrg6/Gpr126 is required for compact wall integrity and establishing trabecular identity during cardiac trabeculation. Nat Commun 17, 1484 (2026). https://doi.org/10.1038/s41467-026-69292-5
Schlüsselwörter: kardiale Trabekulation, Gpr126, Herzentwicklung, Notch-Signalgebung, Zebrafisch-Modell