Clear Sky Science · de
Der genetische Treiber der akuten nekrotisierenden Enzephalopathie, RANBP2, reguliert die Entzündungsreaktion auf Infektion mit Influenza‑A‑Virus
Wenn die Grippe dem Gehirn schadet
Die meisten Menschen verbinden Influenza mit einer Woche Fieber, Husten und Bettruhe. In seltenen Fällen, besonders bei Kindern, kann sich eine routinemäßige Grippeinfektion jedoch plötzlich zu einer lebensbedrohlichen Hirnerkrankung entwickeln, der akuten nekrotisierenden Enzephalopathie (ANE). Familien und Ärztinnen und Ärzte vermuteten lange, dass Gene mitbestimmen, wer diese katastrophale Komplikation entwickelt. Diese Studie legt dar, wie ein einzelnes zelluläres Torwächterprotein, RANBP2, normalerweise das Grippevirus in Schach hält und verhindert, dass die eigene Entzündungsreaktion den Körper außer Kontrolle gerät.
Eine seltene, aber verheerende Grippekomplikation
ANE tritt abrupt nach einem fieberhaften Erkrankungsbild, oft durch Influenza, auf und kann rasch Anfälle, Koma und bleibende neurologische Schäden verursachen. Etwa die Hälfte der weltweit bekannten ANE‑Fälle steht im Zusammenhang mit Influenza‑A‑Viren, insbesondere dem H1N1‑Stamm. Kinder, die bestimmte Veränderungen im RANBP2‑Gen erben, haben ein deutlich erhöhtes Risiko; dieser Zustand ist als ANE1 bekannt. Bisher war jedoch unklar, welche Funktion dieses Protein während einer Grippeinfektion tatsächlich hat und warum seine Veränderung die Entzündung im Gehirn so schwerwiegend macht.
Zellulare Tore und virale Genome
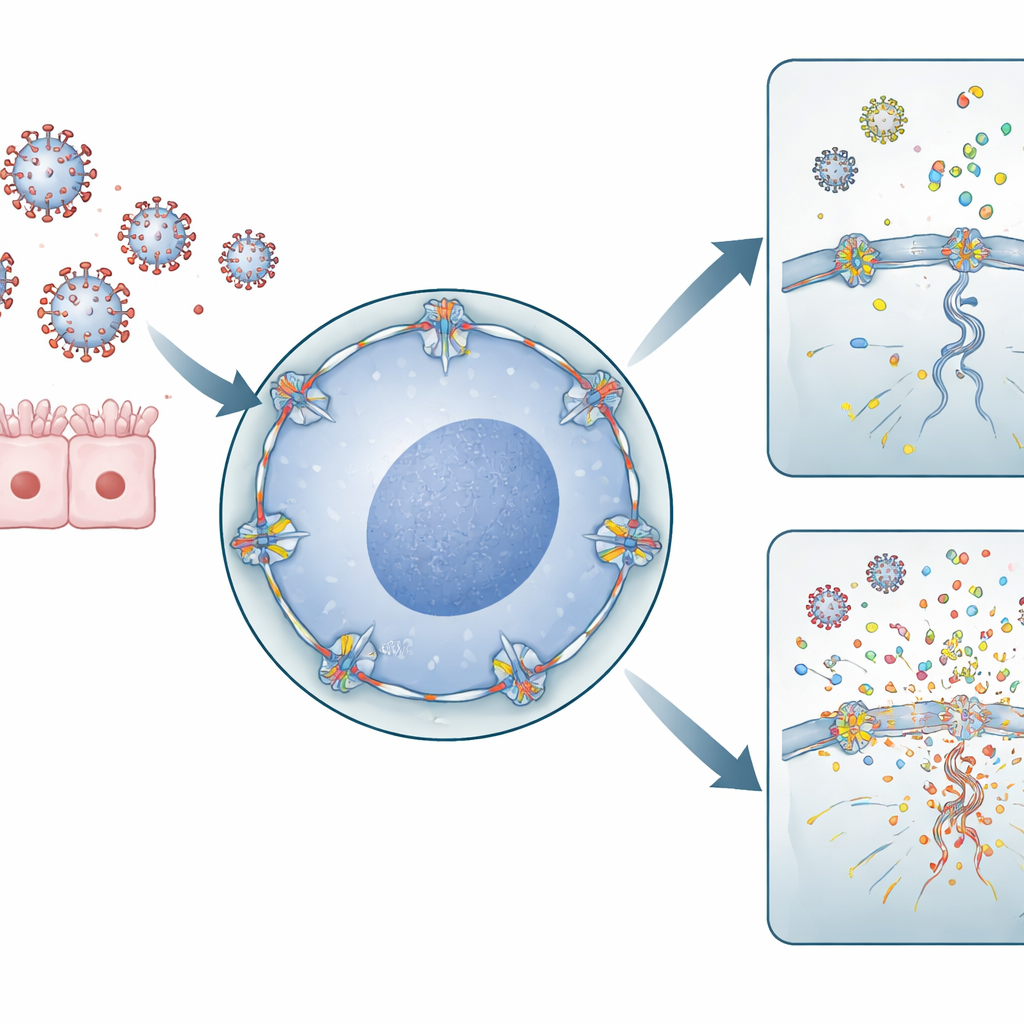
Das Influenza‑A‑Virus hat für ein RNA‑Virus einen ungewöhnlichen Lebenszyklus: Es muss in den Zellkern eindringen, um sein genetisches Material zu kopieren. Dazu passiert es Kernporen—große Durchgänge in der Kernhülle, die den Verkehr zwischen Kern und umgebendem Zytoplasma steuern. RANBP2 ist eine Hauptkomponente an der Außenseite dieser Poren. Die Autorinnen und Autoren verwendeten aus Lunge stammende menschliche Zellen und Immunzellen, um RANBP2‑Spiegel zu verringern oder die mit ANE verknüpfte Mutation einzuführen. Sie fanden heraus, dass bei fehlendem oder fehlplatziertem RANBP2 die Grippe‑Genome im Kern stärker repliziert wurden und virale Genabschnitte unausgewogen ins Zytoplasma exportiert wurden. Überraschenderweise ergab dieses Übermaß an viraler RNA nicht mehr infektiöse Partikel, wohl aber eine veränderte Verteilung und Akkumulation viraler Materialien innerhalb der Zelle.
Wenn virale Überreste das Alarmsystem füttern
Das Immunsystem nutzt molekulare Sensoren, die verstreute Stücke viraler RNA im Zytoplasma als Gefahrensignal erkennen. Das Team zeigte, dass in Zellen ohne normales RANBP2 zusätzliche virale RNA‑Segmente im Zytoplasma akkumulierten und genau die Muster erzeugten, auf die diese Sensoren abgestimmt sind. In aus Lunge abgeleiteten Zellen löste das höhere Spiegel entzündlicher Moleküle wie IL‑6 und IL‑1β aus. In primären menschlichen Makrophagen—den vordersten Immunzellen aus Blutspendern—führte der Verlust von RANBP2 zu einem auffälligen Anstieg proinflammatorischer Chemokine, darunter CXCL8, CXCL10, CCL2, CCL3 und CCL4. Diese chemischen Boten locken zusätzliche Immunzellen an und aktivieren sie, wodurch die gesamte Reaktion auf die Infektion verstärkt wird.
Eine krankheitsassoziierte Mutation, die einen Schutzfaktor fehlplatziert
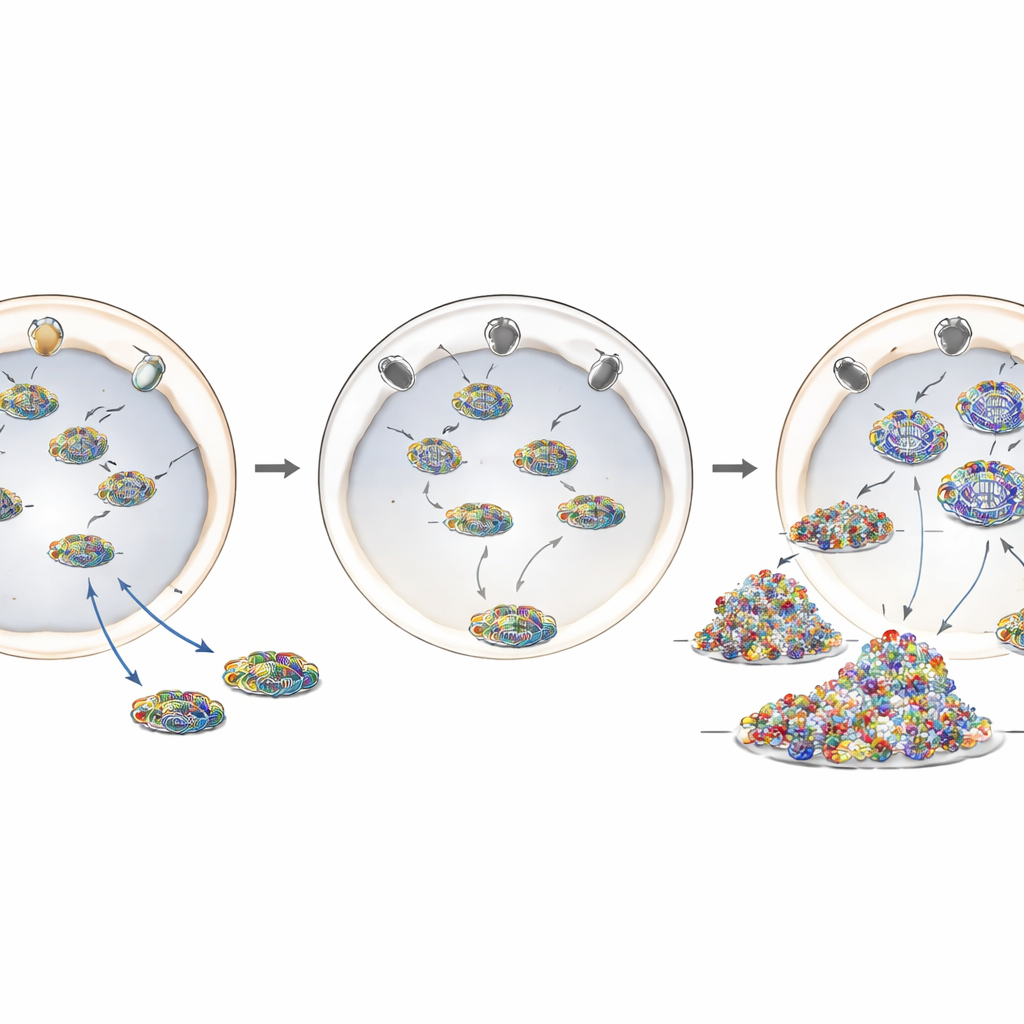
Um ANE1 näher zu modellieren, nutzten die Forschenden CRISPR‑Cas9‑Genomeditierung, um die häufigste krankheitsassoziierte Veränderung, T585M, in das menschliche RANBP2‑Gen einzuführen. In diesen editierten Zellen waren die RANBP2‑Proteinmengen weitgehend normal, aber seine Lage war es nicht: Anstatt einen leuchtenden Rand um die Kernhülle zu bilden, war ein Großteil des Proteins ins Zellinnere verschoben. Zellen mit dieser Mutation, egal ob in einer oder beiden Kopien des Gens, verhielten sich ähnlich wie RANBP2‑depletierte Zellen. Sie unterstützten eine gesteigerte Replikation des Influenzagenoms, zeigten mehr virales Material im Zytoplasma und reagierten nach der Infektion mit einer stärkeren Entzündungsantwort. Das deutet darauf hin, dass die korrekte Positionierung von RANBP2 an den Kernporen—und nicht allein seine Menge—entscheidend für seine schützende Funktion ist.
Warum das für gefährdete Kinder wichtig ist
In der Summe zeichnen die Befunde RANBP2 als zellulären Wächter, der feinabstimmt, wie Influenzagenom in den Kern hinein- und wieder herausgelangt. Fehlt RANBP2 oder ist es fehlplatziert, wird virale RNA übermäßig repliziert und chaotisch exportiert, sodass das Zytoplasma mit molekularen Überresten verstopft wird, die die Immun‑Signalgebung stark verstärken. Für die meisten Gewebe kann dies eine härtere, aber überlebbare Grippe bedeuten. Bei gefährdeten Kindern mit ANE1 jedoch könnte eine derartige eskalierende Entzündung—insbesondere wenn sie das Gehirn erreicht—die plötzlichen, schweren neurologischen Schäden nach ansonsten gewöhnlichen Infektionen erklären. Das Verständnis dieses Wegs könnte helfen, Risikopatienten früh zu identifizieren und anti‑entzündliche Behandlungsstrategien zu entwickeln, bevor die Immunantwort vom Schutz zur Zerstörung umschlägt.
Zitation: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Schlüsselwörter: Influenza, akute nekrotisierende Enzephalopathie, RANBP2, Hyperinflammation, Kernporen