Clear Sky Science · de
Elektrostatische Eigenschaften ungeordneter Regionen steuern die Suche von Transkriptionsfaktoren und deren Pioneer‑Aktivität
Wie Protein‑„Schwänze“ beim Einschalten von Genen helfen
Jede Zelle in Ihrem Körper muss schnell entscheiden, welche Gene eingeschaltet werden, obwohl ihre DNA dicht im Chromatin verpackt ist. Dieser Artikel untersucht, wie flexible, elektrisch geladene Anhängsel wichtiger Gensteuerungsproteine wie eingebaute Suchhilfen wirken, die es manchen Proteinen ermöglichen, versteckte DNA‑Schalter zu finden und das umliegende Material aufzubrechen, während andere damit Schwierigkeiten haben. Das Verständnis dieser verborgenen Kontrollschicht erklärt, wie Stammzellen ihre Flexibilität bewahren und wie Zellen ihre Identität ändern.
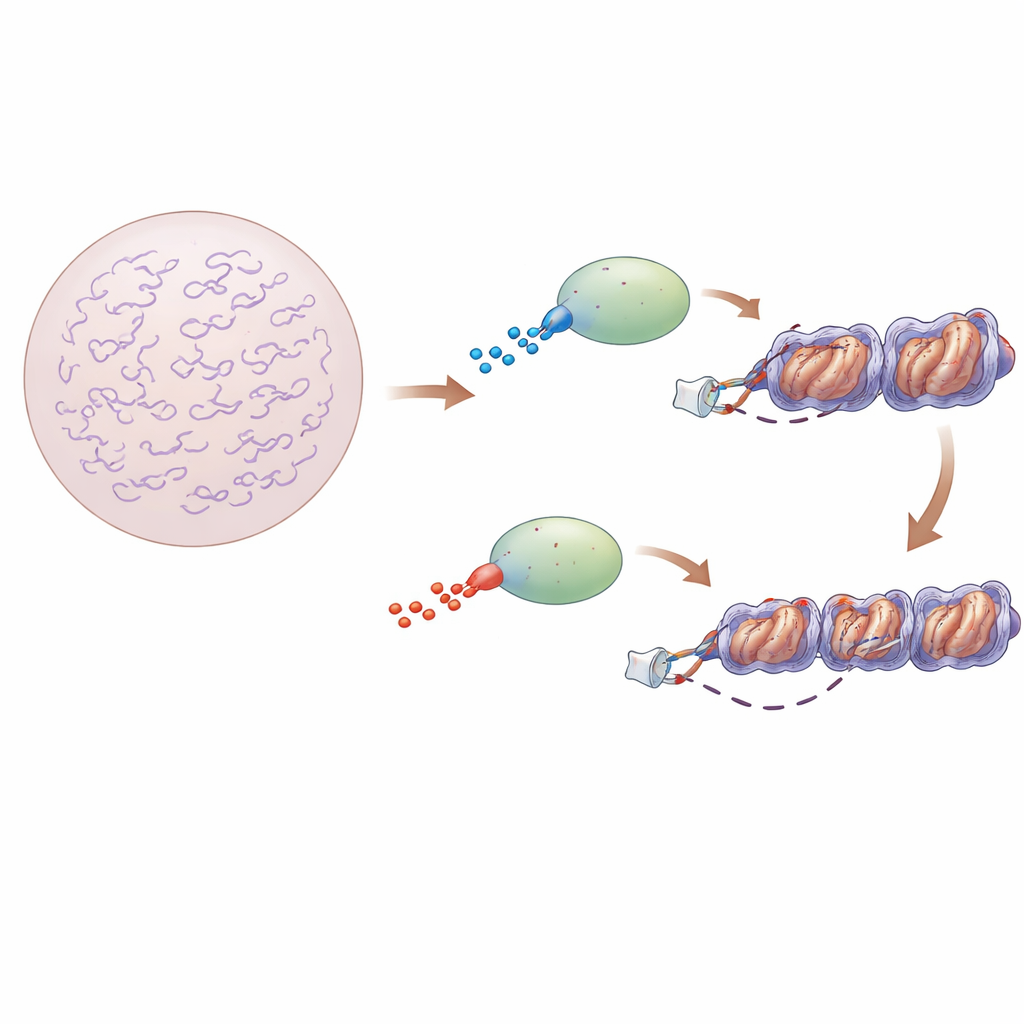
Genschalter in einer überfüllten DNA‑Landschaft
Transkriptionsfaktoren sind Proteine, die kurze DNA‑Sequenzen finden und nahegelegene Gene aktivieren. In Bakterien ist die DNA relativ freiliegend, und klassische Modelle beschreiben diese Proteine so, dass sie wiederholt ins Lösungsmittel entweichen und dann entlang unbedeckter DNA gleiten, bis sie ihr Ziel treffen. In Tierzellen hingegen ist die DNA um spulenartige Proteine gewickelt und bildet Nukleosomen, die weiter zu kompaktem Chromatin gefaltet sind. Diese Enge macht es unklar, wie Transkriptionsfaktoren dennoch schnell genug die richtigen Stellen finden, um Tausende von Genen zu steuern.
Flexible Proteinregionen mit verdecktem Einfluss
Viele Transkriptionsfaktoren besitzen strukturierte, an die DNA bindende Kerne, flankiert von langen, ungeordneten Aminosäureabschnitten. Diese flexiblen Regionen falten sich nicht zu festen Strukturen, tragen aber elektrische Ladungen. Die Autoren konzentrierten sich auf zwei eng verwandte Faktoren, Sox2 und Sox17, die nahezu denselben DNA‑bindenden Kern teilen, sich in Zellen jedoch sehr unterschiedlich verhalten. Sox2 ist ein klassischer „Pioneer“‑Faktor, der an in kompaktem Chromatin verborgene DNA binden kann und für die Erhaltung von Stammzellen in einem flexiblen, pluripotenten Zustand essenziell ist. Sox17 wirkt dagegen typischerweise später in der Entwicklung und kann deutlich schlechter an eng verpackte DNA binden. Der entscheidende Unterschied: Die Region direkt nach dem DNA‑Bindungs‑Kern von Sox2 ist stärker positiv geladen, während das entsprechende Segment in Sox17 eher negativ geladen ist.
Einzelne Moleküle bei der DNA‑Suche beobachten
Um zu sehen, wie diese Ladungsunterschiede den Suchprozess beeinflussen, nutzten die Forschenden Einzelmolekülmikroskopie sowohl in lebenden Maus‑Stammzellen als auch mit gereinigten Komponenten auf Glasoberflächen. Sie konstruierten Varianten von Sox2 und Sox17, die diese geladenen „Schwänze“ tauschen, sowie Varianten, die nur den DNA‑bindenden Kern enthalten. In Zellen verfolgten sie fluoreszent markierte Proteine einzeln und maßen, wie schnell sie diffusieren, wie lange sie gebunden bleiben und wie oft sie auf DNA auftrafen. Proteine mit dem positiv geladenen Sox2‑Schwanz banden häufiger an Chromatin und zeigten öfter länger anhaltende Wechselwirkungen als solche mit dem Sox17‑Schwanz, obwohl alle Versionen im Wesentlichen dieselben DNA‑Buchstaben erkannten.
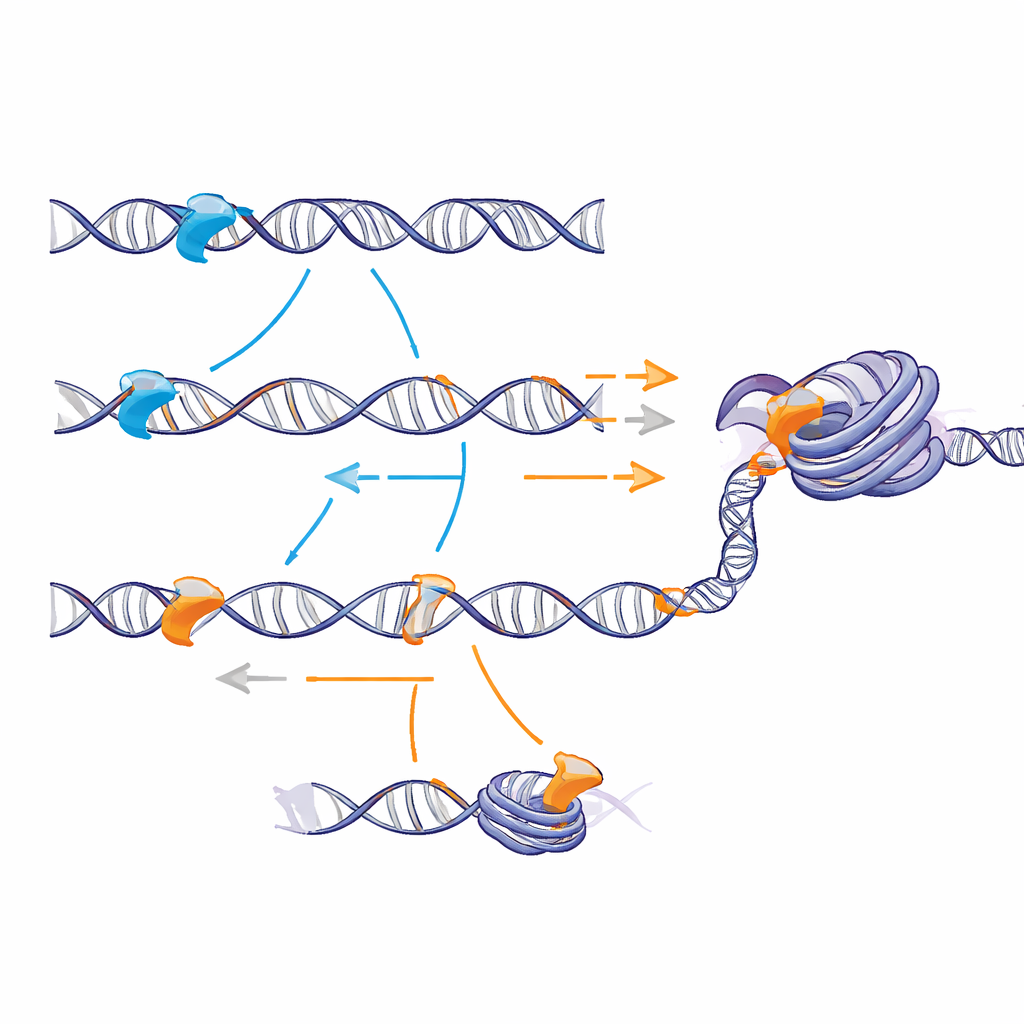
Langsameres Gleiten, aber bessere Erkennung
In sorgfältig kontrollierten Röhrchenexperimenten mit Abschnitten freier DNA veränderten die geladenen Schwänze nicht, wie oft Proteine zunächst aus der Lösung mit der DNA kollidierten. Stattdessen beeinflussten sie das Geschehen, sobald ein Protein gelandet war. Durch die Kombination von Experimenten mit mathematischer Modellierung zeigten die Autoren, dass der Sox2‑Schwanz das Gleiten des Proteins langsamer macht, es aber wahrscheinlicher macht, sein spezifisches Ziel zu „bemerken“, wenn es darüber hinweggleitet. Der Sox17‑Schwanz erlaubt schnellere Bewegung, erhöht aber die Chance, die richtige Stelle einfach zu überflutschen, ohne sich zu verankern. Das zeigt einen Kompromiss zwischen Geschwindigkeit und Erkennung: Ein klebrigerer, positiv geladener Schwanz gestaltet die Energielandschaft rauer genug, um die Wahrscheinlichkeit einer erfolgreichen Zielerfassung zu erhöhen.
Invasion und Öffnung kompakten Chromatins
Als das Team Nukleosomen und kurze Chromatinfasern in vitro nachbaute, wurde der Kontrast deutlicher. Der Sox2‑Schwanz förderte häufige, kurzlebige Kontakte sowohl mit der umwickelten DNA als auch mit den Histon‑Spulen, die gelegentlich in länger anhaltende, spezifische Bindungen an verborgenen Zielstellen übergingen. An Modellen von Chromatinfasern führte dies zu stabilerer Bindung und besserem Zugang zu inneren Stellen als mit dem Sox17‑Schwanz. In Stammzellen erhöhte künstlich exprimiertes Sox2 die Bindung in natürlich geschlossenen Chromatinregionen und machte diese Bereiche zugänglicher, gemessen mit einem Test, der erfasst, wie leicht Enzyme die DNA schneiden können. Die Sox2‑Variante mit dem Sox17‑Schwanz band schlechter und öffnete das Chromatin weniger effizient, obwohl sie weiterhin dieselben DNA‑Motive erkannte.
Was das für die Zellidentität bedeutet
Insgesamt zeigt die Studie, dass die elektrische Ladung ungeordneter Protein‑„Schwänze“ steuern kann, wie Transkriptionsfaktoren die DNA durchsuchen und wie effektiv sie kompaktes Chromatin durchdringen und lockern können. Ein stärker positiv geladener Schwanz, wie bei Sox2, fördert häufige unspezifische Kontakte und schärft die Zielerkennung, unterstützt starke Pioneer‑Aktivität und hilft, die offene Chromatinlandschaft von Stammzellen aufrechtzuerhalten. Diese Prinzipien dürften auf viele andere Gensteuerungsproteine übertragbar sein und fügen eine neue Gestaltungsregel dafür hinzu, wie Zellen ihre genetische Aktivität programmieren und umprogrammieren.
Zitation: Sakong, S., Fierz, B. & Suter, D.M. Electrostatic properties of disordered regions control transcription factor search and pioneer activity. Nat Commun 17, 2512 (2026). https://doi.org/10.1038/s41467-026-69284-5
Schlüsselwörter: Transkriptionsfaktoren, Chromatin, Sox2, intrinsisch ungeordnete Regionen, Pioneer‑Aktivität