Clear Sky Science · de
Eine Rolle der Interaktion zwischen Condensin und Mediator bei der Organisation mitotischer Chromosomen
Wie teilende Zellen ihr genetisches Haus in Ordnung halten
Jedes Mal, wenn sich eine Zelle teilt, muss sie Meter an DNA sorgfältig verpacken und trennen, damit jede Tochterzelle ein vollständiges Chromosomenset erhält. Scheitert dieser Prozess, kann dies zum Zelltod, zu Entwicklungsstörungen oder zu Krebs führen. Diese Studie legt offen, wie zwei große molekulare Maschinen – eine, die die Genaktivität steuert, und eine andere, die DNA kompakt macht – zusammenarbeiten, um Chromosomen während der Zellteilung zu falten, und zeigt eine versteckte Verbindung zwischen den während der Mitose aktivierten Genen und der zuverlässigen Weitergabe der Chromosomen.
Wesentliche Akteure: der Verpacker und der Koordinator
Im Zellkern fungiert ein Proteinkomplex namens Condensin als molekularer Verpacker, der DNA schleift und verdichtet, sodass die dicken Chromosomen entstehen, die in der Mitose sichtbar sind. Ein weiterer großer Komplex, der Mediator, hilft dabei zu steuern, welche Gene ein- oder ausgeschaltet werden, indem er mit der RNA-Polymerase zusammenarbeitet, dem Enzym, das DNA in RNA kopiert. Die Autorinnen und Autoren untersuchten diese Komplexe in der Spalthefe (fission yeast), einem etablierten Modellorganismus, dessen Chromosomenbiologie der menschlicher Zellen auffallend ähnelt. Sie entdeckten, dass eine Untereinheit von Condensin, Cnd1, physisch an eine Mediator-Untereinheit namens Pmc4 bindet. Diese Interaktion findet an hochaktiven Genen und an einer besonderen Gruppe von Genen statt, die nur während der Mitose eingeschaltet werden. Diese „mitotischen Gene“ liegen an den Rändern großer chromosomaler Nachbarschaften oder Domänen und scheinen als Grenzmarker zu fungieren.
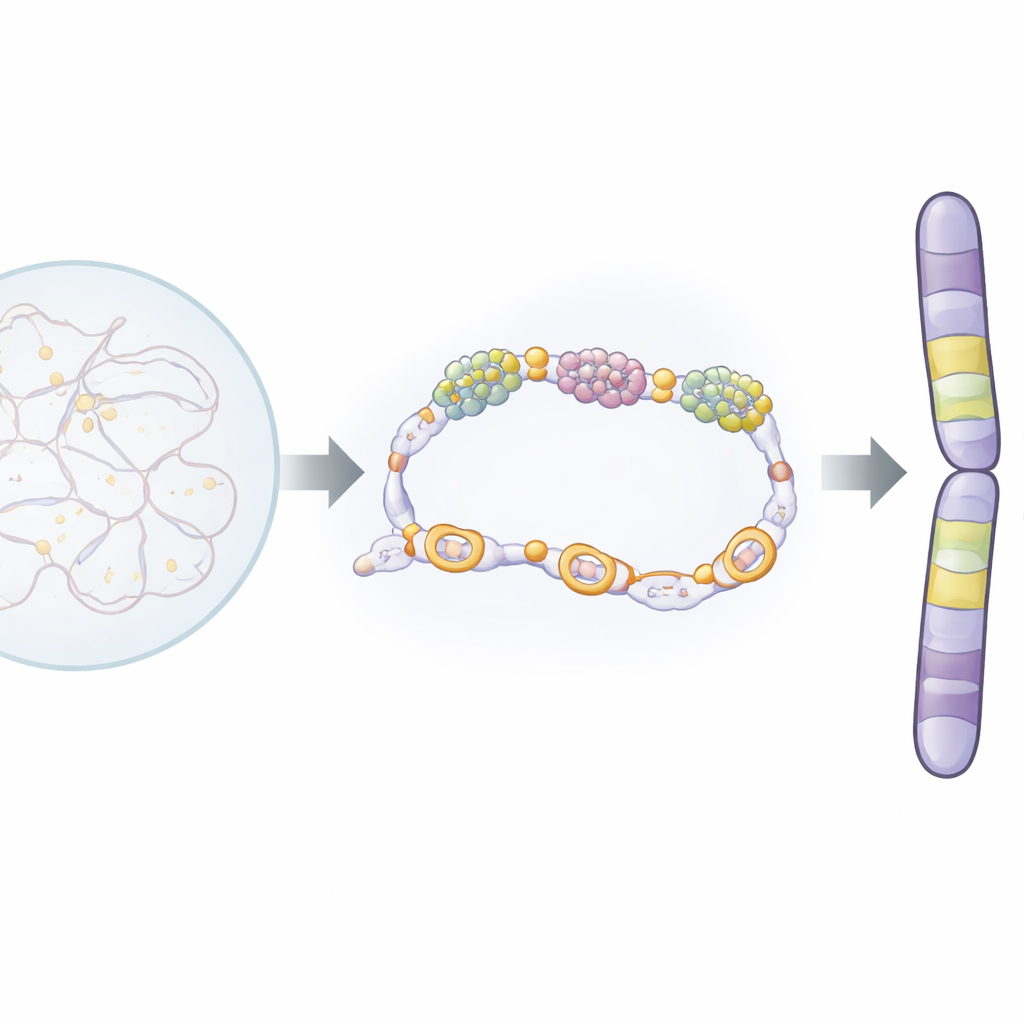
Ein einziger molekularer Handschlag mit großen Folgen
Um zu testen, wie wichtig dieser Handschlag ist, erzeugten die Forschenden eine sehr präzise Mutation in Cnd1 und änderten nur eine Aminosäure (K658E), sodass Cnd1 Pmc4 nicht mehr binden kann, während sich der Condensin-Komplex ansonsten normal bildet. Hefezellen mit dieser Mutation waren lebensfähig, zeigten jedoch häufiger Chromosomenfehlverteilungen und hinterließen während der Mitose nachhängende DNA-Fragmente. Mithilfe von 3D-Genomkartierung (Hi-C) und mikroskopischen Distanzmessungen zwischen ausgewählten DNA-Positionen zeigte das Team, dass die mutierten Zellen schwächere condensin-getriebene Kontakte und weniger kompakte chromosomale Domänen aufwiesen. Mit anderen Worten: Ohne eine funktionierende Cnd1–Pmc4-Interaktion konnte Condensin Chromosomen während der Zellteilung nicht effizient zu robusten, domänenbasierten Strukturen falten.
Genaktivität als Grenzbildner
Die Studie untersuchte danach, wie der Mediator zu dieser Faltung beiträgt. Bei Reduktion von Pmc4 verringerte sich das Condensin-Binden an vielen Genen, und die Stärke der durch Condensin gebildeten Domänen nahm ab. Auffällig wurde, dass die Grenzen zwischen benachbarten Domänen verschwommen und DNA-Interaktionen über zuvor scharfe Grenzen hinwegflossen. Detaillierte RNA-Messungen zeigten, dass der Verlust von Pmc4 die Expression einer Untergruppe von während der Mitose aktivierten Genen, die vom Transkriptionsfaktor Ace2 gesteuert werden, deutlich reduzierte. Diese Grenzgene weisen normalerweise eine sehr hohe Besetzung durch Mediator, Condensin und einen grundlegenden Transkriptionsfaktor namens TBP auf. Die Daten stützen ein Modell, in dem Mediator und TBP zunächst Condensin an Promotoren hochaktiver und mitotischer Gene rekrutieren; im Verlauf der Transkription wird Condensin entlang der Genkörper geschoben und trägt dazu bei, benachbarte DNA in Schleifen zu verknüpfen, wobei Ace2-Zielgene die Ränder jeder kondensierten Domäne setzen.
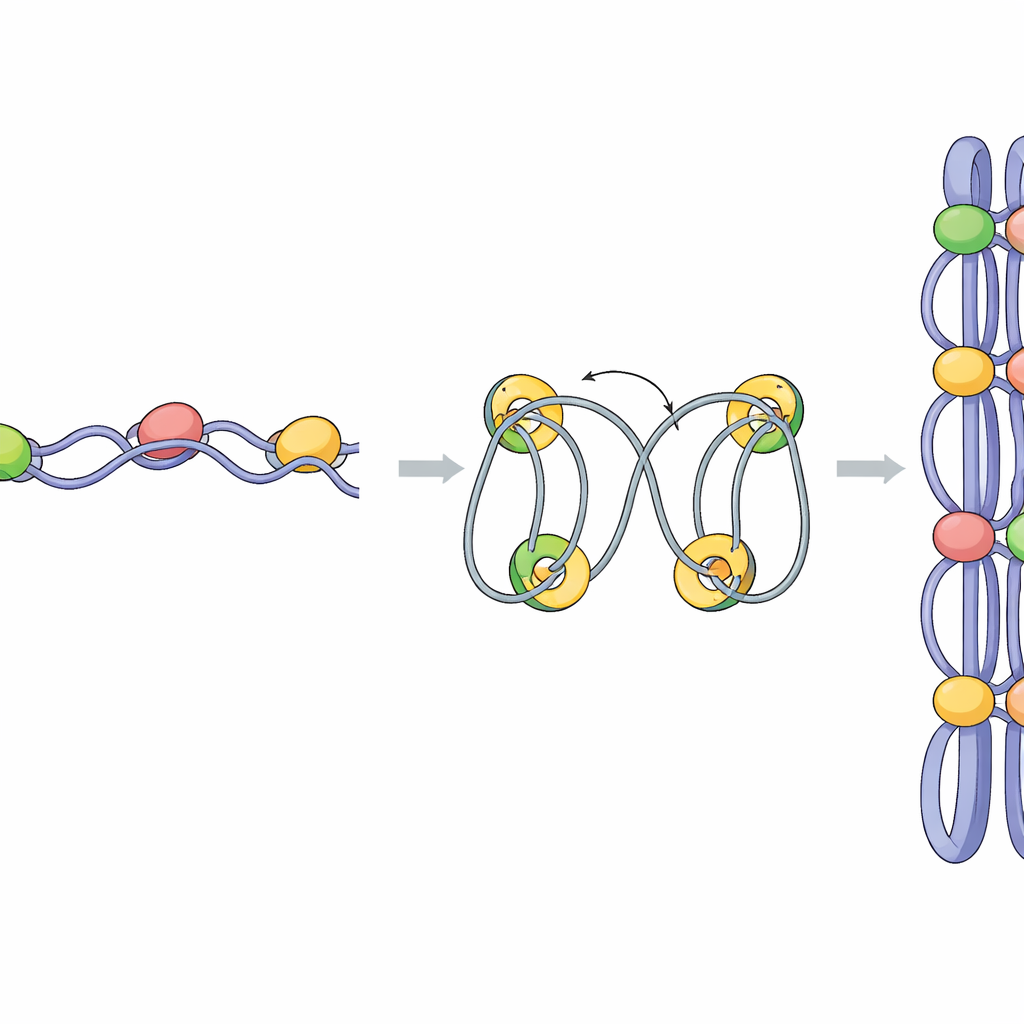
Eine mögliche Rolle flüssigkeitsähnlicher Tröpfchen
Beim Menschen ist bekannt, dass Mediator durch einen Prozess namens Phasentrennung flüssigkeitsähnliche Tröpfchen bildet, die die Transkriptionsmaschinerie in kleinen nukleären Hubs konzentrieren können. Die Autorinnen und Autoren fanden, dass sich der Mediator der Spalthefe ähnlich verhält: Die Untereinheit Pmc4 kann im Reagenzglas Tröpfchen bilden, und die Behandlung von Zellen mit 1,6-Hexandiol, einer Chemikalie, die solche Kondensate stört, löste schnell Mediator-Foci im Zellkern auf. Eine milde Hexandiol-Behandlung schwächte Mediator- und Condensin-Bindung an Schlüsselgenen und verwischte spezifisch die Grenzen zwischen chromosomalen Domänen, obwohl die Gesamtverdichtung der Chromosomen weiterhin stattfand. Das legt nahe, dass Mediator-reiche Tröpfchen an mitotischen Grenzgenen dabei helfen könnten, den Beginn und das Ende von Domänen zu formen, indem sie Transkription und Condensin-Aufladung an diesen Stellen konzentrieren.
Von Hefelektionen zur menschlichen Gesundheit
Abschließend untersuchte das Team, ob eine ähnliche Partnerschaft auch in menschlichen Zellen besteht. Mittels eines Interaktionsassays fanden sie, dass MED4, das humane Gegenstück zu Pmc4, spezifisch an CAP-D3 bindet, eine Condensin-II-Untereinheit, die eng mit der Hefen-Untereinheit Cnd1 verwandt ist. Eine menschliche CAP-D3-Mutation, die der Hefemutation K658E entspricht, störte diese Interaktion und führte zu mitotischen Fehlern wie fehl ausgerichteten Chromosomen und Mikronuklei. Auch die Depletion von MED4 erzeugte Segregationsdefekte. Diese Parallelen deuten darauf hin, dass die Kopplung zwischen Mediator und Condensin eine konservierte Strategie ist, mit der Zellen Genaktivität mit Chromosomenfaltung koordinieren und so dafür sorgen, dass DNA während der Zellteilung ordentlich verpackt und gleichmäßig verteilt wird.
Warum das für das Verständnis von Krankheiten wichtig ist
Diese Arbeit zeigt, dass die Faltung von Chromosomen während der Mitose nicht nur auf rohe Kompression zurückzuführen ist. Vielmehr hängt sie davon ab, wo und wann bestimmte Gene angeschaltet werden, wobei mediatorgetriebene Transkription an Grenzgenen Condensin rekrutiert, um großskalige Domänen zu gestalten. Indem sie zeigt, wie eine einzige Interaktion zwischen zwei Komplexen sich auf die Chromosomenarchitektur und die Segregationsgenauigkeit auswirken kann, bietet die Studie einen Rahmen, um zu verstehen, wie subtile Veränderungen in der Genregulationsmaschinerie oder der Condensin-Funktion zu chromosomaler Instabilität beitragen könnten — ein Kennzeichen vieler Krebsarten und genetischer Erkrankungen.
Zitation: Iwasaki, O., Tashiro, S., Chung, C.YL. et al. A role for condensin-mediator interaction in mitotic chromosome organization. Nat Commun 17, 2509 (2026). https://doi.org/10.1038/s41467-026-69270-x
Schlüsselwörter: Chromosomenarchitektur, Condensin, Mediator-Komplex, Mitosen, 3D-Genom-Organisation