Clear Sky Science · de
Trifunktionelles Flavoenzym-katalysiertes asymmetrisches 4‑alkyl‑Butenolid‑Aufbau in der Avenolid‑Biosynthese
Warum winzige Ringe in Bakterien für uns wichtig sind
Viele lebensrettende Medikamente, von Wurm‑Abtötungsmitteln bis zu Pflanzenschutzmitteln, beruhen auf einem kleinen chemischen Motiv namens Butenolid. Heute werden diese Ringe meist aus erdölbasierten Ausgangsstoffen in mehrstufigen Industrieprozessen hergestellt, die Energie verbrauchen und Abfall erzeugen. Diese Studie zeigt, wie Bodenbakterien einen solchen Ring bauen: das Hormon Avenolid, das die Produktion der Blockbuster‑Antiparasitika Avermectine einschaltet. Das Verständnis dieses natürlichen Weges weist auf sauberere, billigere Methoden zur Herstellung nützlicher Chemikalien hin und könnte helfen, neue Antibiotika zu erschließen.
Der besondere Ring im Zentrum vieler Wirkstoffe
Butenolide sind kompakte, fünfgliedrige Ringe, die Chemiker schätzen, weil sie vielseitig reagieren und in vielen Naturstoffen und modernen Arzneimitteln vorkommen. Sie prägen Moleküle mit anticanceren, antifungalen, antientzündlichen und insektiziden Aktivitäten, die in Medizin und Landwirtschaft genutzt werden. Traditionelle Syntheserouten zu diesen Ringen erfordern jedoch meist mehrere sorgfältig kontrollierte Schritte, teure Katalysatoren und petrochemische Ausgangsstoffe. Diese Kombination treibt Kosten und Umweltbelastung in die Höhe und veranlasst Forscher, nach biologischen Abkürzungen zu suchen, die die Natur bereits perfektioniert hat.
Ein bakterielles Hormon, das ein Blockbuster‑Medikament anschaltet
Im Bodenbakterium Streptomyces avermitilis wirkt das butenolidhaltige Molekül Avenolid als winziges Hormon. In extrem niedrigen Konzentrationen bindet es an ein regulatorisches Protein und löst eine molekulare Bremse an den Genen, die Avermectine produzieren—starke Wirkstoffe, die parasitäre Würmer und einige Insekten lähmen. Vorherige genetische Arbeiten hatten angedeutet, dass zwei Enzyme, SavA und SavB, Avenolid aufbauen, doch die tatsächlichen Schritte waren unbekannt. Das Team transferierte die relevanten Gene zunächst in einen leichter handhabbaren Verwandten, Streptomyces albidoflavus, und optimierte die Wachstumsbedingungen, bis der gentechnisch veränderte Stamm Milligramm‑Mengen reinen Avenolids produzierte—genug, um den Weg im Detail zu analysieren. 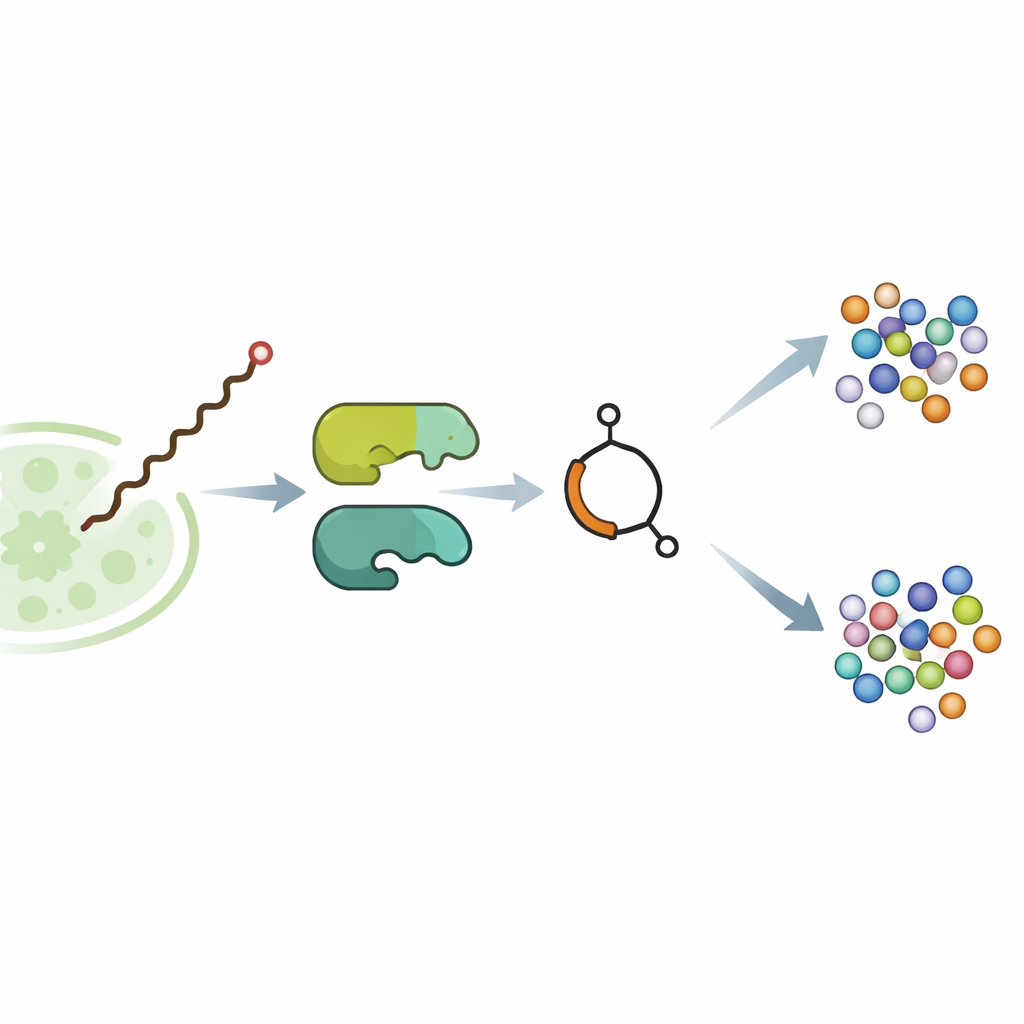
Ein einzelnes Enzym, das drei Aufgaben in Folge erfüllt
Die zentrale Überraschung der Studie ist SavA, ein Flavin‑haltiges Enzym, das drei unterschiedliche chemische Umwandlungen an einem fettsäureähnlichen Startbaustein aus dem normalen Zellstoffwechsel durchführt. In Reaktionen im Reagenzglas mit sorgfältig synthetisierten Nachahmer‑Substraten zeigten die Forscher, dass SavA zunächst Wasserstoffatome entfernt, um eine Doppelbindung einzuführen, dann an einer spezifischen Position eine sauerstoffhaltige Gruppe einfügt und schließlich die Ketten‑Schließung zum Butenolidring fördert. Isotopenexperimente mit mit schwererem Sauerstoff angereichertem O2 bestätigten, dass der Ring‑Sauerstoff direkt aus der Luft stammt. Strukturelle Modellierung und gezielte Mutationen identifizierten eine einzelne Aminosäure als Base, die die Reaktion auslöst, und zeigten, wie das gebundene Flavin‑Cofaktor zwischen oxidierter und reduzierter Form zyklisch wechselnd wirkt, ohne verbraucht zu werden.
Ein abschließendes Enzym, das die Seitenkette feinabstimmt
Sobald SavA das chirale Butenolid‑Gerüst gebaut hat, übernimmt SavB—ein Cytochrom‑P450‑Enzym—und verziert die angehängte Kohlenstoffkette. In Anwesenheit seiner Redoxpartner und eines üblichen zellulären Cofaktors führt SavB eine präzise Abfolge von Oxidationen an zwei benachbarten Kohlenstoffatomen aus. Zeitaufgelöste Analysen enthüllten zwei Zwischenmoleküle: zuerst ein einfach hydroxyliertes Produkt, dann eine Ketoform, bevor das voll funktionsfähige Avenolid erscheint. Kernspinresonanzmessungen bestätigten die Positionen und die dreidimensionale Anordnung dieser neuen Gruppen. Die Arbeit zeigt, dass SavB diese Sauerstoffeinführungen in definierter Reihenfolge und mit strenger Kontrolle der Orientierung vornimmt—ein wichtiges Merkmal für die biologische Aktivität des Hormons. 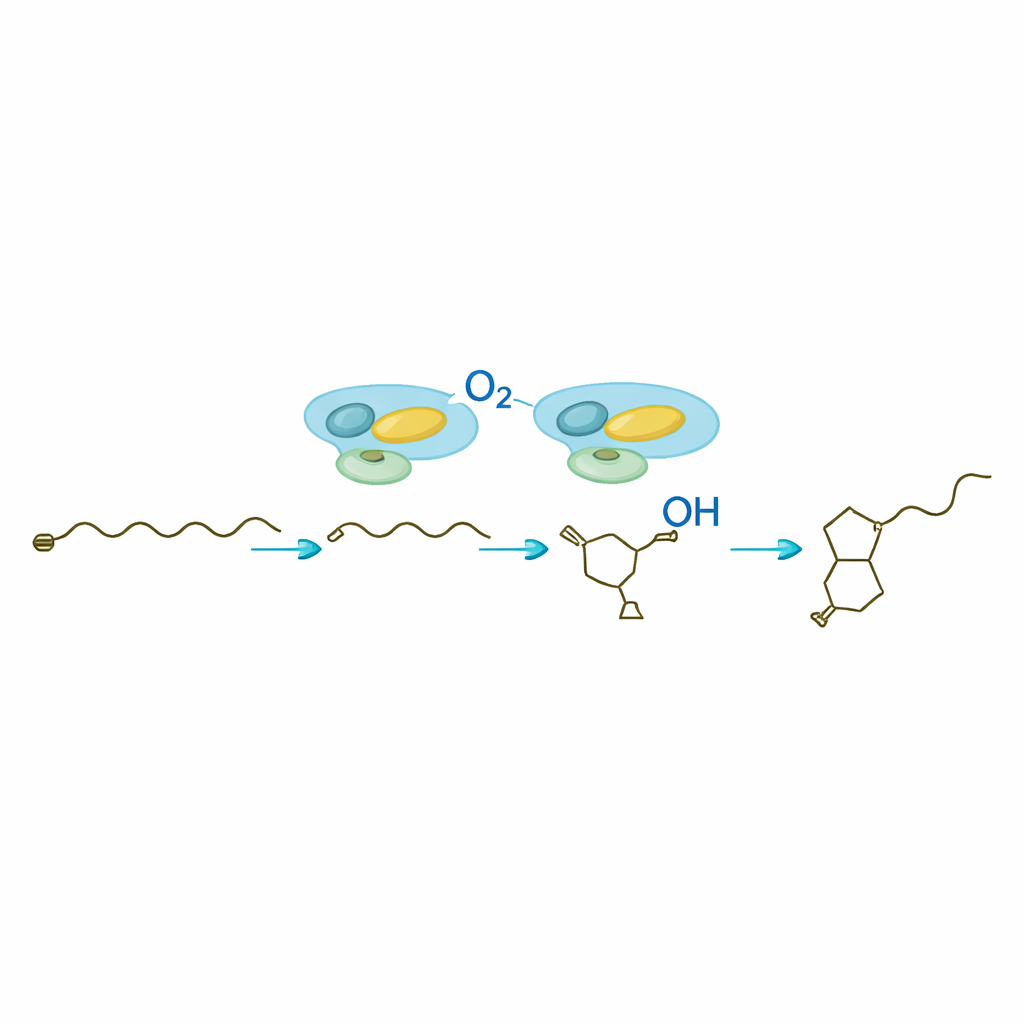
Grüne Chemie‑Lehren aus bakteriellen Enzymen
Gemeinsam wandeln SavA und SavB einen gewöhnlichen, von Fettsäuren abgeleiteten Baustein in ein fein abgestimmtes Signalmolekül um und verwenden dabei nur den Sauerstoff aus der Luft und standardmäßige zelluläre Helfer. Anders als viele industrielle Prozesse benötigt SavA keine zusätzlichen Reduktionsmittel oder Opferreagenzien; sein Flavin‑Cofaktor transportiert einfach Elektronen, während das Substrat selbst die treibende Kraft liefert. Die Autoren heben SavA als eine neue Art vielbegabten Flavoenzyms mit großem Potenzial als Biokatalysator für die nachhaltige Herstellung von Butenoliden und verwandten Strukturen hervor. Praktisch gesehen könnte die Nutzung oder das Engineering solcher Enzyme eines Tages Fabriken—oder gentechnisch veränderte Mikroben—ermöglichen, wichtige Arzneimittelbausteine und Agrarchemikalien aus erneuerbaren Rohstoffen unter milden Bedingungen herzustellen und so sowohl Kosten als auch Umweltbelastung zu senken.
Zitation: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Schlüsselwörter: Butenolid‑Biosynthese, Flavoenzym SavA, Avenolid‑Hormon, Biokatalyse, Streptomyces‑Signalgebung