Clear Sky Science · de
Degrader des Dengue‑Virus‑Kapsidproteins zeigen differenzierte Pharmakologie im Vergleich zu Kapsid‑Inhibitoren
Die Hülle des Virus gegen sich selbst wenden
Das Dengue‑Fieber infiziert jedes Jahr Hunderte Millionen Menschen, doch behandelbare antivirale Medikamente fehlen bislang. Diese Studie untersucht einen neuen Weg, das Dengue‑Virus zu entwaffnen, indem eines seiner wichtigsten Bausteine in infizierten Zellen zerstört wird, anstatt nur dessen Aktivität zu blockieren. Die Arbeit zeigt, dass sorgfältig entworfene Moleküle ein zentrales Virusprotein für die Entsorgung durch das zelluläre Abfallmanagement markieren können, wodurch die Virenproduktion reduziert und die Fähigkeit des Virus, sich vor unseren Immunabwehrmechanismen zu verbergen, abgeschwächt wird.
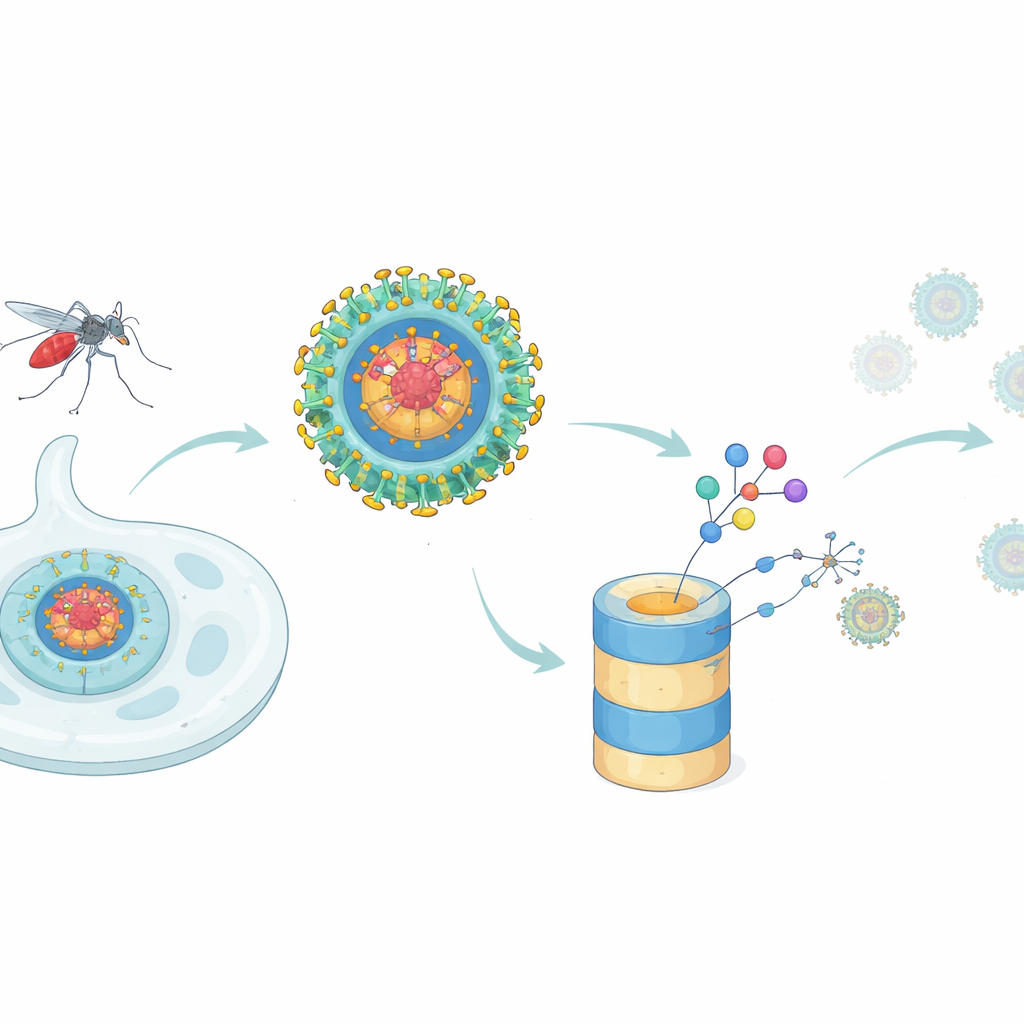
Taktikwechsel gegen Dengue
Die meisten antiviralen Medikamente wirken wie Stöpsel in einer Maschine: Sie besetzen eine funktionelle Stelle eines Virusproteins und versuchen, dessen Funktion zu blockieren. Dieser Ansatz stößt an Grenzen, wenn ein einzelnes Virusprotein viele verschiedene Aufgaben erfüllt oder wenn kleine Mutationen die Bindung des Medikaments schwächen. Das Kapsidprotein von Dengue ist ein typisches Beispiel: Es bildet die Kernhülle, die das virale Genom in neue Partikel verpackt, greift aber auch in die Wirtszelle ein, indem es mit zahlreichen menschlichen Proteinen interagiert und die Interferon‑Antwort abschwächt, einen vorderen Alarm des angeborenen Immunsystems. Die Autoren untersuchten, ob ein neueres Wirkstoffkonzept — gezielter Proteinabbau — klassische Inhibitoren übertreffen kann, indem es das Kapsidprotein tatsächlich aus infizierten Zellen entfernt.
Entwurf eines molekularen „Kopfgeldjägers“
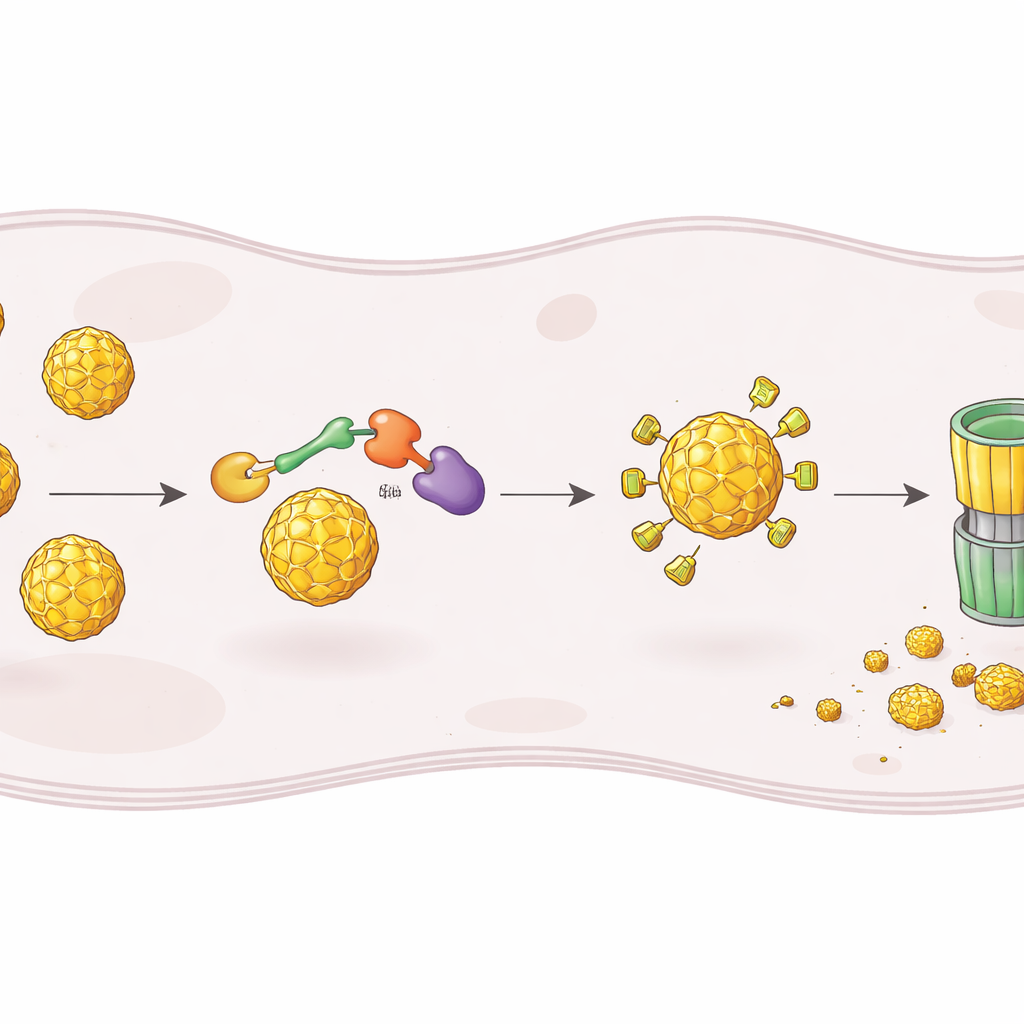
Um einen solchen Degrader zu bauen, starteten die Forscher von ST148, einem bekannten kleinen Molekül, das an das Dengue‑Kapsid bindet und die Assembly neuer Viruspartikel stört. Chemisch verknüpften sie ST148 mit einem zweiten Modul, das einen humanen Enzymkomplex rekrutiert, der Proteine für den Abbau markiert. Die resultierenden chimären Moleküle, PROTACs genannt, sind so gestaltet, dass sie das Kapsid mit einem Ende und ein E3‑Ligase‑Komplex mit dem anderen Ende greifen, wodurch das Kapsid mit Ubiquitin markiert und in das proteasomale Abbausystem der Zelle eingeschleust werden kann. Durch das Testen vieler Linkerlängen und Ligase‑rekrutierender Gruppen identifizierten sie eine herausragende Verbindung, bezeichnet als RPG‑01‑132, die zuverlässig die Kapsid‑Spiegel in infizierten Zellen verringerte — abhängig von der CRBN‑Form der Ligase und von einer intakten Proteasomfunktion.
Stilllegung von Virenproduktion und Immunevasion
Sobald ein funktionierender Degrader vorlag, untersuchte das Team seine tatsächlichen Effekte auf die Dengue‑Infektion. In leberabgeleiteten Zellen, die mit Dengue‑Virus infiziert waren, bewirkte RPG‑01‑132 einen starken Abfall der freigesetzten infektiösen Viren, bei Konzentrationen, bei denen es nur teilweise die Gesamtmenge an Kapsid reduzierte. Wichtig ist, dass andere virale Proteine und virale RNA unverändert blieben, was zeigt, dass die Verbindung nicht einfach die Gesamtreplikation vergiftete, sondern spezifisch durch Kapsidverlust wirkte. Elektronenmikroskopie lieferte einen visuellen Befund: Zellen, die mit dem ursprünglichen Inhibitor ST148 behandelt wurden, sammelten Stapel von teilweise gebildeten Viruspartikeln im endoplasmatischen Retikulum, konsistent mit einem Zusammenbaustopp, während Zellen, die mit dem Degrader behandelt wurden, nahezu keine sichtbaren Virionen zeigten. Der Degrader hob zudem die Fähigkeit des Kapsids auf, in einem Reporter‑System die Interferon‑β‑Signalgebung zu unterdrücken, was darauf hindeutet, dass die nicht‑strukturelle Rolle des Kapsids bei der Abschwächung der angeborenen Immunität durch dessen Abbau rückgängig gemacht werden kann.
Viralem Variantenreichtum und Arzneimittelresistenz voraus sein
Dengue‑Virus existiert in vier großen Serotypen, die unterschiedlich gut auf Kapsid‑zielende Inhibitoren ansprechen, und Resistenz kann durch einzelne Mutationen entstehen. Die Autoren verglichen den Degrader mit ST148 über repräsentative Stämme aller vier Serotypen und gegen ein Virus, das eine Mutation (S34L im Kapsid) trägt, die zuvor gezeigt wurde, dass sie ST148 unwirksam macht. Wie erwartet war ST148 am wirksamsten gegen einen Serotyp und verlor gegen das resistente Mutant an Aktivität. RPG‑01‑132 zeigte demgegenüber eine ähnliche antivirale Potenz über alle Serotypen hinweg und behielt die Aktivität gegen das S34L‑Mutant bei, während es weiterhin über denselben CRBN‑abhängigen Degradationsweg wirkte. Dies veranschaulicht einen Schlüsselvorteil der „ereignisgetriebenen“ Pharmakologie: Der Degrader muss nicht dauerhaft stark an jede Kapsid‑Molekül binden, solange er ausreichend Degradationsereignisse auslösen kann, um das Gleichgewicht zu kippen.
Was das für zukünftige Dengue‑Therapien bedeutet
Die Studie zeigt, dass das Kapsidprotein von Dengue nicht nur als strukturelle Komponente des Virus angegriffen werden kann, sondern als entfernbarer Knotenpunkt, der mehrere Schritte der Infektion und der Immunevasion unterstützt. Indem die Forscher einen klassischen Inhibitor in einen Degrader verwandelten, schufen sie eine Verbindung, die die Virenproduktion blockiert, einen Teil der Virenunterdrückung der angeborenen Immunität aufhebt und über verschiedene Virusstämme sowie eine bekannte Resistenzmutation hinweg wirksam bleibt. RPG‑01‑132 selbst muss noch optimiert werden — bessere Zellgängigkeit, stärkere Wirksamkeit in Tiermodellen und gründliche Sicherheitsprüfungen — doch es liefert einen überzeugenden Proof‑of‑Concept. Allgemeiner legt die Arbeit nahe, dass die Entführung der zellulären Entsorgungsmaschinerie neue Wege zu antiviralen Arzneimitteln eröffnen könnte, die für Viren schwerer zu umgehen sind und Proteine mit vielfältigen Funktionen in infizierten Zellen neutralisieren können.
Zitation: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Schlüsselwörter: Dengue‑Virus, Kapsidprotein, gezielte Proteinabbau, antivirale Wirkstoffentwicklung, PROTACs