Clear Sky Science · de
Kooperative Anionaktivierung an einem Kobaltzentrum durch Ionenkopplung und Ligandendesign
Warum winzige Partner um Metalle wichtig sind
Chemiker konzentrieren sich oft auf den zentralen „Darsteller“ einer Reaktion — ein Metallatom, das beim Brechen und Bilden von Bindungen hilft. Dieser Artikel zeigt jedoch, dass die stillen Partner in der Nähe, die mit bloßem Auge unsichtbar sind, das Verhalten des Metalls vollständig verändern können. Indem die Autoren den Raum um ein Kobaltatom gezielt gestalten, offenbaren sie, wie zwei nahezu austauschbare Anionen, die in der Chemie und in Batterien häufig als passive Nebenakteure betrachtet werden, zu deutlich unterschiedlichen Ergebnissen führen können. 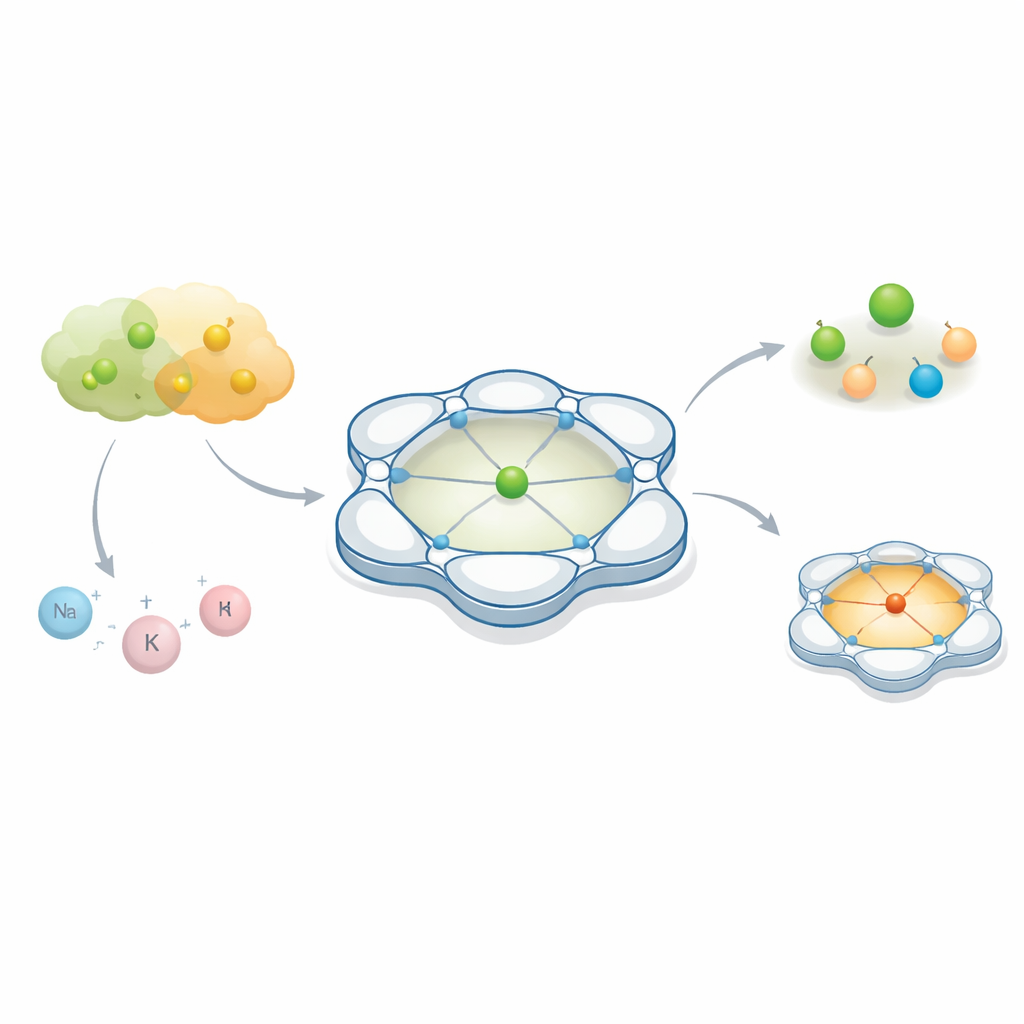
Eine maßgeschneiderte Tasche um Kobalt bauen
Die Forscher entwarfen ein käfigartiges organisches Gerüst namens Py4Im, das sich eng um ein Kobaltion legt. Dieses Gerüst besteht aus mehreren verknüpften Pyridinvorringen und einer Imidazolidineinheit, die zusammen eine starre, schalenförmige Hohlraumstruktur mit einer einzelnen N–H‑Gruppe bilden. Dieser kleine Hohlraum ist „protonisch“, das heißt, er kann Wasserstoffbrücken ausbilden, und er weist in eine bestimmte Richtung, ähnlich einer winzigen Andockbucht für eintreffende Anionen. Wenn Kobalt mit diesem Liganden kombiniert wird, entsteht eine Familie positiv geladener Komplexe, deren Gesamtform und innerer Hohlraum gleich bleiben, während das Gegenion — der negativ geladene Partner — ausgetauscht werden kann. Damit eignet sich das System ideal, um zu untersuchen, wie sich verschiedene Anionen in derselben kontrollierten Umgebung verhalten.
Zwei ähnlich aussehende Anionen, zwei sehr unterschiedliche Verhaltensweisen
Das Team verglich zwei gängige Anionen, Tetrafluorborat (BF4−) und Hexafluorophosphat (PF6−), die weit verbreitet als sogenannte schwach koordinierende Anionen eingesetzt werden. Sie sind populär, weil sie sich meist vom Metallzentrum fernhalten und stark geladene Spezies stabilisieren, ohne sich direkt einzubringen. Überraschenderweise verhalten sie sich im Py4Im‑Hohlraum nicht gleich. Unter milden Bedingungen spendet PF6− ein Fluoridion an Kobalt, bricht eine starke P–F‑Bindung und bildet einen klar definierten Kobalt–Fluorid‑Komplex. Im Gegensatz dazu weigert sich BF4−, das üblicherweise als das „sprödere“ der beiden gilt, in derselben Umgebung Fluorid abzugeben. Stattdessen ordnet es sich in einer stabilen Anordnung am Kobaltzentrum an, ohne den Bindungsbruch abzuschließen.
Zusehen, wie Ionen sich paaren und bewegen
Um diese gegensätzlichen Verhaltensweisen zu verstehen, nutzten die Autoren eine Kombination aus hochauflösenden NMR‑Techniken und quantenchemischen Rechnungen. Diffusions‑NMR‑Experimente maßen, wie schnell sich die positiven und negativen Spezies in Lösung bewegen, was Aufschluss darüber gibt, wie eng sie gepaart sind. Diese Messungen zeigten, dass BF4− ein engeres, beständigeres Ionengespann mit dem Kobaltkomplex bildet als PF6−. Der Py4Im‑Hohlraum positioniert das Anion direkt unter dem Imidazolidin‑Ring, wo Wasserstoffbrücken von der N–H‑ und benachbarten C–H‑Gruppe es festhalten. Computerberechnungen bestätigten, dass diese stärkere, gerichtete Paarung mit BF4− den Ausgangszustand so stark stabilisiert, dass das Brechen der B–F‑Bindung leicht ungünstig wird, obwohl diese Bindung intrinsisch schwächer ist als die P–F‑Bindung in PF6−. PF6−, das lockerer paart, kann sich annähern, Fluorid an Kobalt übertragen und als PF5 abgehen, was zu einem thermodynamisch erreichbaren fluoridtragenden Kobaltkomplex führt. 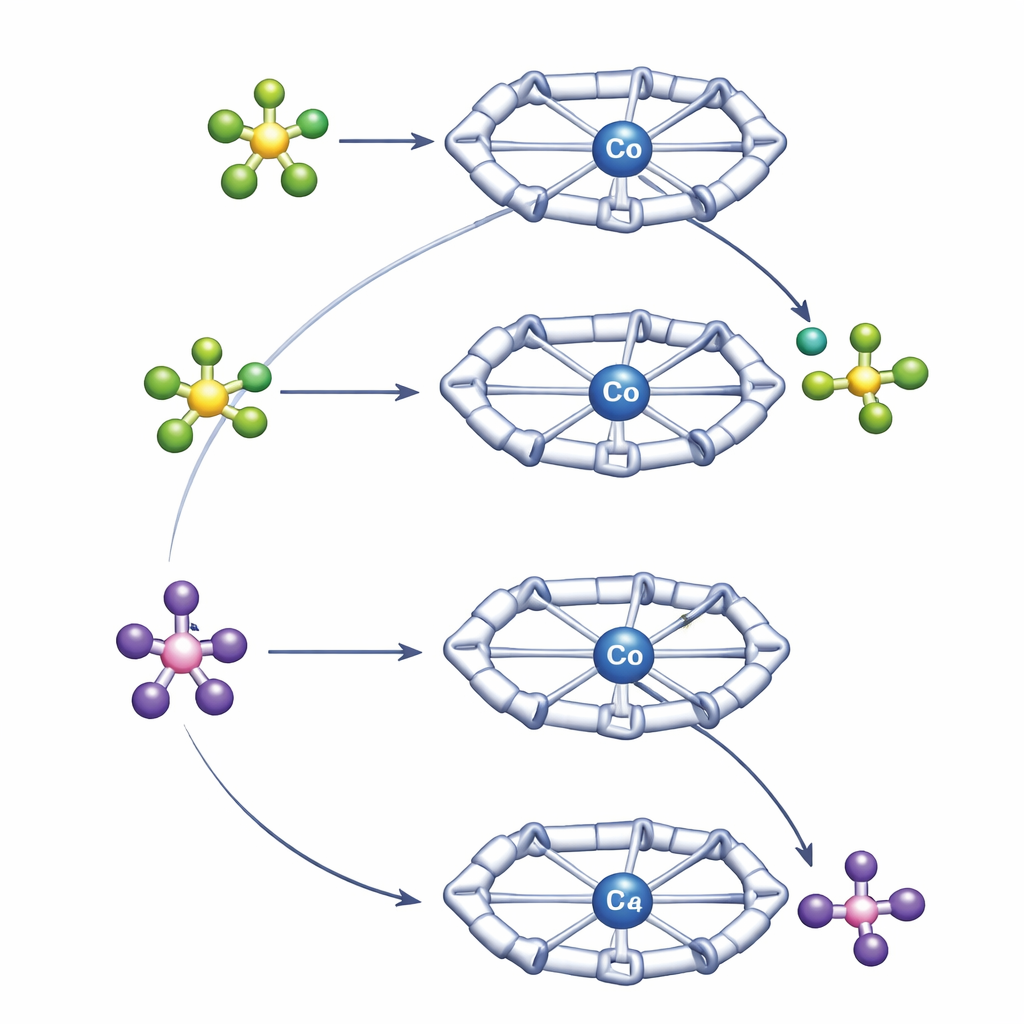
Ein gebundenes Fluorid in ein nützliches Werkzeug verwandeln
Einmal gebildet, ist der Kobalt–Fluorid‑Komplex kein Sackgassenprodukt. Die Autoren zeigen, dass er als nukleophile Fluoridquelle fungiert — vereinfacht gesagt, kann er Fluorid an positiv geladene oder elektronengearme Partner liefern. In Lösung überträgt diese Kobalt–Fluorid‑Spezies sauber Fluorid auf reaktive Kohlenstoffzentren, auf Siliziumatome in Chlorosilanen und auf Acylchloride, wodurch organische Fluoride entstehen, während sich der Kobaltkomplex in seine Chloridform zurückverwandelt oder den neuen Partner bindet. In einer geschickten Wendung demonstriert das Team außerdem, dass BF4− dazu gebracht werden kann, Fluorid abzugeben, wenn eine separate Base vorhanden ist, die das zurückbleibende BF3‑Fragment „auffängt“. Dadurch lässt sich der ansonsten widerstrebende BF4−‑Weg in einen umwandeln, der ebenfalls zum gleichen Kobalt–Fluorid‑Produkt führt.
Was das für das Design intelligenterer Katalysatoren bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass Ionen, die früher als inerte Begleitsalze galten, chemische Reaktionen tatsächlich maßgeblich steuern können. Durch das Formen einer präzisen Tasche um ein Metallzentrum und die Kontrolle darüber, wie stark Anionen daran gepaart sind, kehrten die Autoren die erwartete Reaktivität zweier nahezu identischer Spezies um. PF6−, normalerweise als sehr robust angesehen, wird zur leichteren Fluoridquelle, während BF4− durch stärkere Paarung festgehalten wird, sofern das System nicht zusätzlich unterstützt wird. Diese Arbeit liefert eine Blaupause dafür, Ligandendesign und Gegenionsauswahl gemeinsam einzusetzen, um die Reaktivität eines Metallkomplexes zu steuern — eine Idee, die Bereiche von homogener Katalyse bis zur Elektrolytgestaltung für fortschrittliche Batterien beeinflussen könnte, wo die „stummen Partner“ in Lösung alles andere als passiv sind.
Zitation: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Schlüsselwörter: Kobaltkomplexe, schwach koordinierende Anionen, Fluorid‑Transfer, Ionenkopplung, Ligandendesign