Clear Sky Science · de
Metallisches Molybdänsulfid katalysiert protometabolische Kohlendioxid-Reaktionsnetze unter extremen Bedingungen
Wie Gestein die Chemie des Lebens anstoßen könnte
Weit bevor lebende Zellen Enzyme entwickelt hatten, brauchte die Erde dennoch Wege, einfache Gase wie Kohlendioxid in die organischen Moleküle umzuwandeln, von denen Leben abhängt. Diese Studie untersucht, ob bestimmte natürlich vorkommende Minerale, ähnlich denen in der Nähe von unterseeischen Heißen Quellen, als primitive „chemische Motoren“ fungiert haben könnten. Indem gezeigt wird, dass eine metallische Form von Molybdänsulfid Kohlendioxid in ein überraschend reichhaltiges Netz organischer Verbindungen umwandeln kann, liefert die Arbeit ein konkretes Szenario dafür, wie die Kernchemie des Lebens auf einem leblosen Planeten begonnen haben könnte.

Heiße Schlote und verborgene chemische Motoren
Das moderne Leben beruht auf komplexen Reaktionsnetzen, die Kohlenstoff durch Zellen und Ökosysteme schleusen. Diese Netze sind auf Proteine angewiesen, die Enzyme heißen und selbst Produkte der Evolution sind. Die große Frage ist, was davor existierte. Die Autoren richteten ihren Blick auf hydrothermale Schlote — natürliche, heiße Wasserzüge am Meeresboden, die reich an Metallsulfiden und Wasserstoffgas sind — als wahrscheinliche Schauplätze für die frühesten Kohlenstoffreaktionen. An solchen Orten trifft heißes, unter Druck stehendes Wasser auf Gestein, das Metalle wie Eisen, Nickel und Molybdän enthält. Frühere Experimente zeigten, dass einige dieser Metalle Kohlendioxid zu kleinen Organika umwandeln können, aber meist nur auf Teilstrecken der Lebenswege, nicht als vollständige Netzwerke.
Ein Mineral, das alte Enzyme nachahmt
Das Team konzentrierte sich auf eine bestimmte Form von Molybdänsulfid, die sogenannte 1T′-Phase, deren atomare Anordnung den Metall-Schwefel-Zentren moderner Enzyme ähnelt, die Kohlendioxid verarbeiten. Unter hohen Temperaturen und Drucken in Wasser, mit Wasserstoff als Treibstoff, katalysierte dieses Mineral die Umwandlung gelösten Kohlendioxids (modelliert als Bicarbonat) in eine unerwartet breite Palette organischer Säuren. Durch gezieltes Variieren von Temperatur, Reaktionszeit und Gasdruck sowie durch Verfolgung der Produkte mit Chromatographie, Massenspektrometrie und NMR identifizierten sie 32 verschiedene Zwischen- und Endprodukte, die aus derselben einfachen Kohlenstoffquelle hervorgingen.
Die Kern-Kohlenstoffwege des Lebens ohne Enzyme rekonstruieren
Diese 32 Verbindungen sind nicht zufällig. Viele sind dieselben Moleküle, die im Zentrum des modernen Metabolismus stehen — etwa Acetat, Pyruvat, Oxalacetat, Succinat und alpha-Ketoglutarat. Zusammen lassen sie sich auf fünf Hauptwege der Kohlenstofffixierung abbilden, die zeitgenössische Mikroben nutzen: der Acetyl–CoA-Weg und Varianten des Krebs-Zyklus sowie verwandte Schleifen. In den Experimenten traten diese Wege als ein miteinander verbundenes Netzwerk auf: Acetat verknüpfte mehrere Zyklen; größere Moleküle zerfielen und bildeten sich wieder; und Schlüsselzwischenprodukte verschwanden und tauchten später je nach Bedingungen wieder auf. Die Bildung mehrkettiger Säuren erreichte hohe Effizienz, wobei bis zu etwa 70 % des umgewandelten Kohlenstoffs in Molekülen mit zwei oder mehr Kohlenstoffatomen endeten. Das Reaktionsnetz zeigte außerdem Oszillationen, bei denen die Mengen bestimmter Produkte im Zeitverlauf anstiegen und sanken, was das dynamische Verhalten lebender chemischer Systeme widerspiegelt.
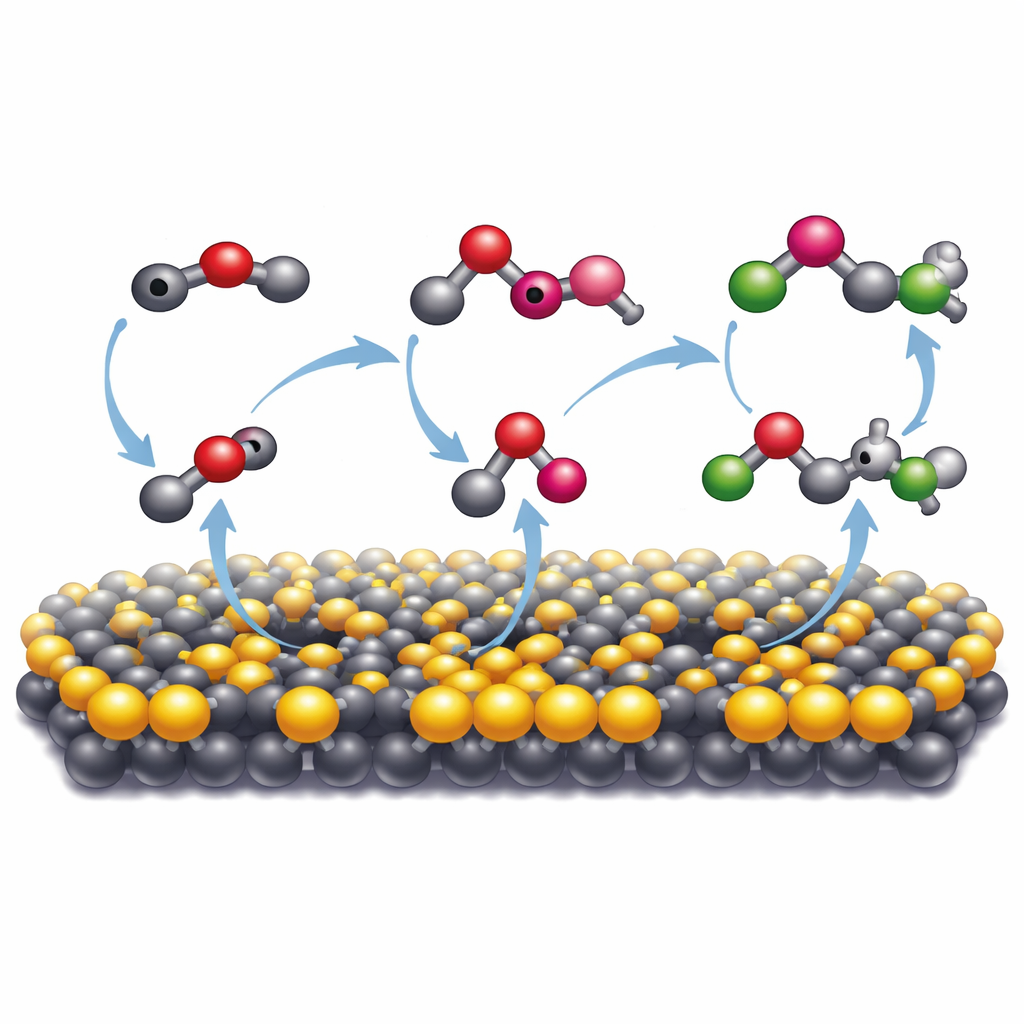
Wie das Mineral Kohlenstoffatome zur Zusammenarbeit bringt
Um zu verstehen, warum gerade dieses Mineral so effektiv war, verglichen die Forscher es mit einer gebräuchlicheren Form von Molybdänsulfid mit anderer atomarer Struktur. Nur die metallische, verzerrte Form — mit vielen fehlenden Schwefelatomen — förderte in großem Umfang die Bildung größerer Organika. Spektroskopische Techniken zeigten, dass auf dieser Oberfläche aus Kohlendioxid stammendes Kohlenmonoxid stark bindet und weiter zu hochreaktiven Fragmenten, sogenannten Radikalen, reduziert wird. Diese Radikale werden auf der Mineraloberfläche gerade so weit stabilisiert, dass sie aufeinandertreffen und neue Kohlenstoff–Kohlenstoff-Bindungen bilden können. Elektronenspin-Messungen bestätigten die Präsenz solcher Radikale, und das Hinzufügen einer Radikalfänger-Substanz unterdrückte die Mehrkohlenstoffprodukte deutlich. Computersimulationen untermauerten dieses Bild, indem sie zeigten, dass Schwefelvakanzstellen und die veränderte elektronische Struktur der 1T′-Phase es der Oberfläche erleichtern, Elektronen zu spenden und Kohlenstofffragmente nahe zueinander zu ziehen, sodass sie sich verbinden können.
Von der Gesteinschemie zum ersten Metabolismus
Zusammengenommen deuten diese Befunde darauf hin, dass bestimmte Metallsulfidminerale auf der frühen Erde komplexe, selbstorganisierende Kohlenstoffchemie betrieben haben könnten, lange bevor Enzyme existierten. In hydrothermalen Schlotumgebungen, wo heiße, wasserstoffreiche Flüssigkeiten auf Kohlendioxid und metallführende Gesteine treffen, könnte ein Mineral wie 1T′-Molybdänsulfid kontinuierlich anorganischen Kohlenstoff in ein Netz miteinander verbundener organischer Pfade umgewandelt haben, das modernen metabolischen Zyklen ähnelt. Für nicht Spezialisten ist die Kernaussage, dass die zentrale Chemie des Lebens vielleicht kein Leben brauchte, um zu beginnen: Unter den richtigen Bedingungen können einfache Gesteine, Wasser und Gas viele derselben Moleküle und Reaktionsschleifen spontan aufbauen, die lebende Zellen noch heute verwenden.
Zitation: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Schlüsselwörter: Ursprung des Lebens, präbiotische Chemie, hydrothermale Schlote, Kohlenstofffixierung, Molybdänsulfid