Clear Sky Science · de
Interpretierbare und generative Deep-Learning-Modelle erklären phasenseparierende intrinsisch ungeordnete Motive
Warum winzige Proteinabschnitte wichtig sind
In jeder unserer Zellen sammeln sich wichtige Moleküle oft zu tropfenartigen Klumpen, sogenannten biomolekularen Kondensaten. Diese Tropfen organisieren die Chemie ohne Membranbegrenzung, beeinflussen, wie Gene ein- oder ausgeschaltet werden, wie Signale weitergegeben werden und wie Zellen auf Stress reagieren. Viele solcher Tropfen entstehen durch schlaffe Proteinabschnitte, die als intrinsisch ungeordnete Regionen bekannt sind. Dennoch tun sich Biologen schwer damit, die kurzen Sequenzstücke zu identifizieren, die tatsächlich das Bilden dieser Tropfen antreiben. Diese Studie stellt ein Deep-Learning‑Framework namens PhaSeMotif vor, das sowohl diese Schlüsselsegmente finden als auch neue entwerfen kann und Forschern so ein leistungsfähiges neues Instrument bietet, um zelluläre Tropfen zu untersuchen und neu zu gestalten.
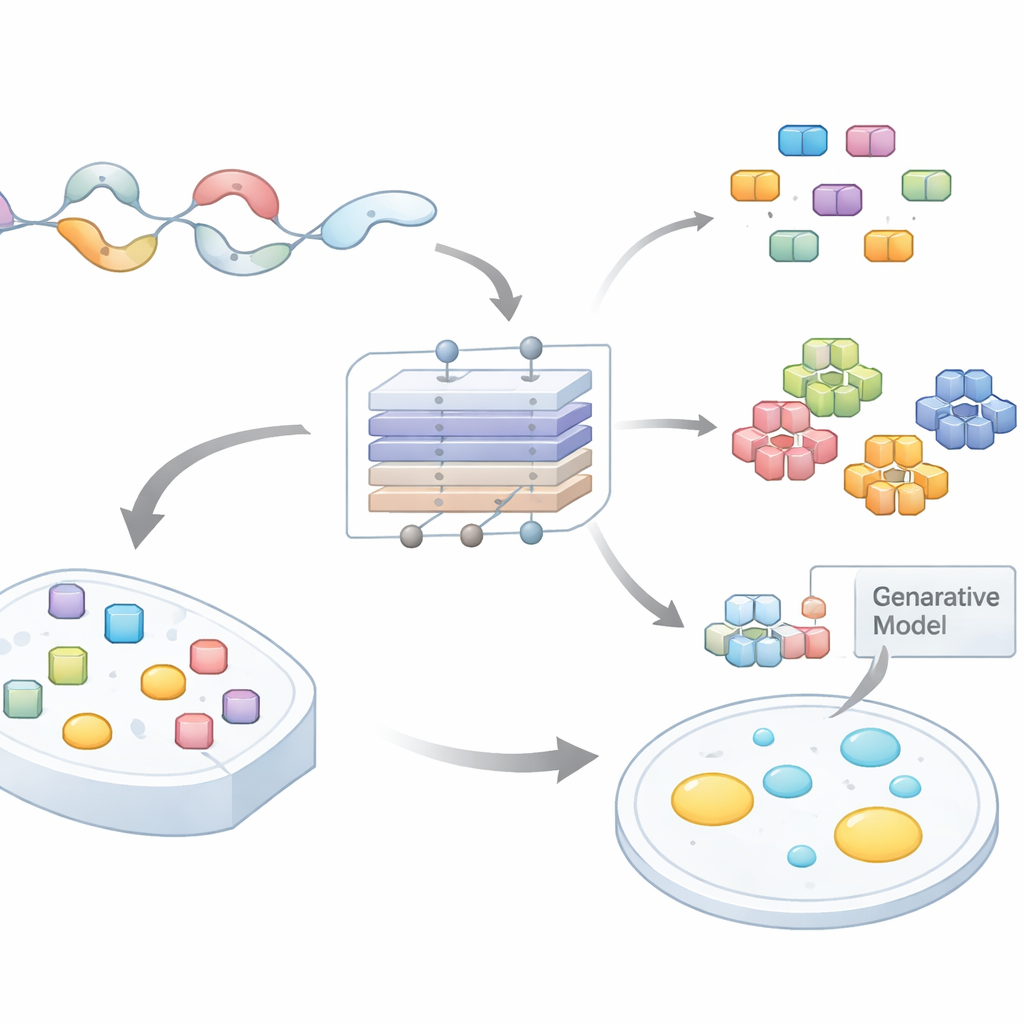
Von chaotischen Proteinenden zu überprüfbaren Hypothesen
Viele Proteine besitzen lange, flexible Enden, die sich nicht zu festen Strukturen falten. Diese ungeordneten Regionen sind in bestimmten Aminosäuren angereichert und enthalten oft wiederkehrende Muster oder kurze Motive. Eine wachsende Zahl von Studien zeigt, dass solche Motive Kondensation antreiben, indem sie viele schwache Wechselwirkungen gleichzeitig ermöglichen. Allerdings ist das Durchsuchen ganzer Proteome, um herauszufinden, welche kurzen Abschnitte relevant sind und warum, ein großes Nadelöhr. Bestehende computationale Werkzeuge bewerten meist ganze Proteine oder große Regionen und geben wenig Hinweis darauf, wo man mutieren oder was man im Labor testen sollte. Die Autoren setzten sich zum Ziel, ein Modell zu entwickeln, das nicht nur vorhersagt, ob eine ungeordnete Region Tropfen bilden kann, sondern auch welche exakten Untersequenzen die Hauptarbeit leisten.
Eine Deep-Learning-Landkarte tropfenbildender Motive
Das Team stellte umfangreiche Datensätze ungeordneter Regionen aus mehreren Arten zusammen und kennzeichnete sie danach, ob die Wirtsproteine wahrscheinlich einer Phasentrennung unterliegen. Anschließend trainierten sie ein auf Aufmerksamkeit basierendes neuronales Netz, PhaSeMotif, das eine Aminosäuresequenz beliebiger Länge entgegennimmt und einen Tropfenbildungs-Score ausgibt. Entscheidend ist, dass das Netzwerk eine Kombination aus Faltungs‑ (Convolutional) Schichten und Aufmerksamkeitsmechanismen nutzt, um zu bewerten, wie stark jedes kurze Fenster der Sequenz zu diesem Score beiträgt. Indem sie das Modell rückverfolgten (mithilfe von Techniken ähnlich der geführten Rückpropagation), extrahierten die Autoren hochwichtige Patches—kurze Motive, oft unter 20 Resten lang—die das Modell als essenziell für die Tropfenbildung einstufte.
Vorhersagen in lebenden Zellen testen
Um zu prüfen, ob diese Motive tatsächlich eine Rolle spielen, nutzten die Forscher ein lichtaktivierbares System in menschlichen Zellen. Sie verbanden vorhergesagte tropfenbildende ungeordnete Regionen mit einem lichtempfindlichen Oligomerisierungsmodul und einem fluoreszenten Marker. Unter blauem Licht kondensierten diese Konstrukte schnell zu hellen Punktstrukturen und zeigten die Phasentrennung in Echtzeit an. Das Team entfernte dann gezielt einzelne Motive, indem sie diese durch neutrale, flexible Linker gleicher Länge ersetzten. In 82 % der 17 veränderten Sequenzen wurde die Tropfenbildung deutlich abgeschwächt oder verschwand ganz, während Kontrollmutationen außerhalb der PhaSeMotif‑Segmente oft nur geringe Effekte zeigten. Wichtig ist, dass viele dieser Schlüsselmotive mit Stellen überlappten, an denen krankheitsassoziierte Mutationen bekannt dafür sind, Kondensation zu stören—ein Hinweis auf ihre biologische Relevanz.
Eine Wortschatzliste von Motivtypen aufdecken
Mit mehr als 17.000 Motiven fragten die Autoren als Nächstes, ob es gemeinsame „Geschmacksrichtungen“ tropfenbildender Segmente gibt. Sie analysierten Aminosäurezusammensetzung und Musterung und gruppierten die Motive dann in neun Cluster. Einige Cluster waren reich an aromatischen Resten und Glycin, was mit klebrigen π–π- und Kation–π‑Wechselwirkungen übereinstimmt. Andere enthielten getrennte Bereiche positiver und negativer Ladungen, was elektrostatische Anziehung und selektive Partitionierung in bestimmte Kondensate begünstigt. Weitere Cluster wurden von Prolin und Glycin dominiert, die Flexibilität unterstützen, oder von langen Glutamin‑Runs, die dichte Netzwerke von Wasserstoffbrücken bilden können. Unterschiedliche Zellkompartimente und Kondensattypen zeigten charakteristische Mischungen dieser Motivklassen, was darauf hindeutet, dass die Motivzusammensetzung mitbestimmt, wo und mit welchen Partnern ein Protein kondensiert.
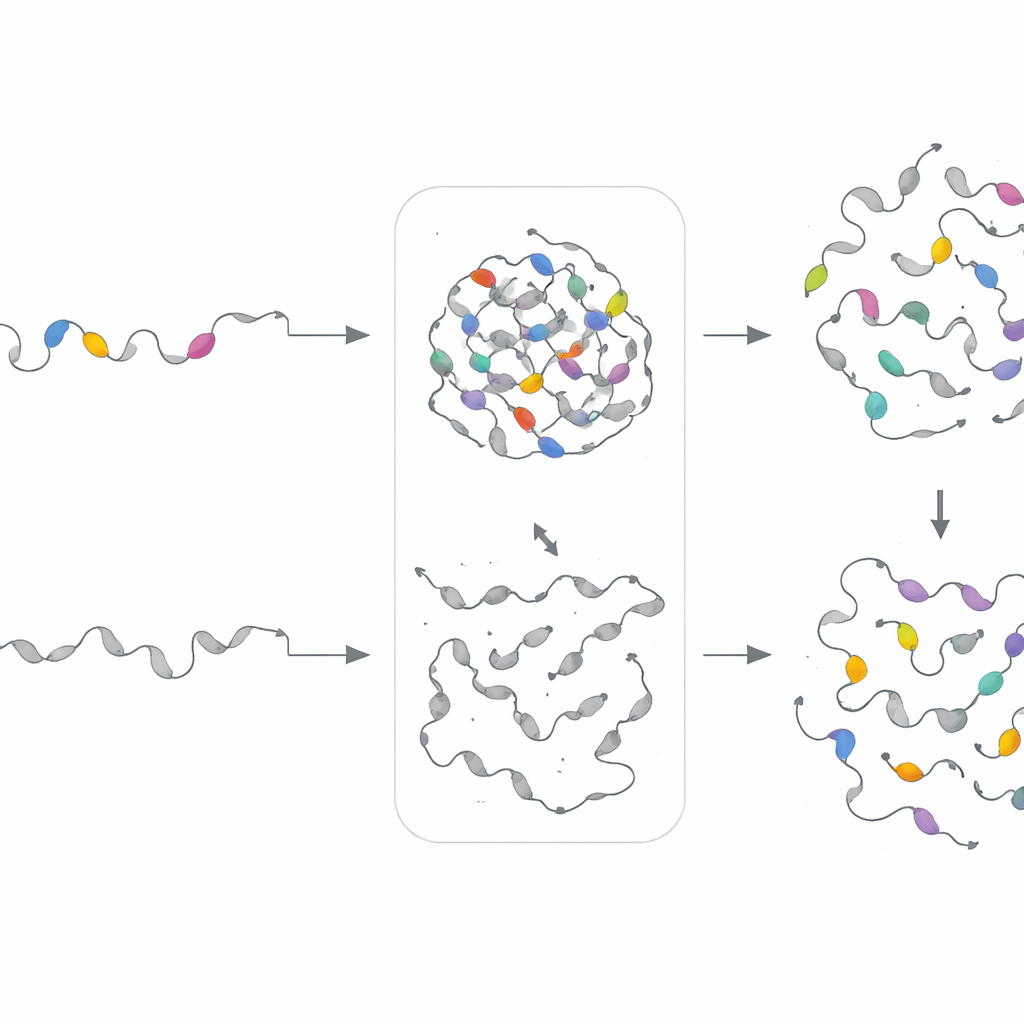
Neue Motive entwerfen, um die Regeln zu beweisen
Um zu testen, ob Motiv„rezepte“—statt exakter Sequenzen—das Tropfenverhalten steuern, bauten die Autoren separate generative Modelle für jedes Motivcluster. Diese variationalen Autoencoder lernten die statistischen Muster eines Clusters und erzeugten dann neue, künstliche Sequenzen, die dieselben kompositionellen Fingerabdrücke, aber eine andere exakte Reihenfolge aufwiesen. Die Forscher setzten diese synthetischen Motive experimentell in Proteine ein, aus denen die ursprünglichen Segmente entfernt worden waren. Bemerkenswerterweise stellten in 18 von 21 Fällen die konstruierten Motive die Phasentrennung in Zellen wieder her und konnten manchmal sogar die Geschwindigkeit oder Dichte der Tropfenbildung modulieren. Das zeigt, dass PhaSeMotif zugrundeliegende Gestaltungsregeln erfasst, die wiederverwendet werden können, um tropfenbildende Regionen zu bauen oder zu reparieren.
Was das für Biologie und Krankheit bedeutet
Indem interpretierbares Deep Learning mit generativem Design und direkten zellulären Tests verknüpft wird, verwandelt diese Arbeit den vagen Begriff „ungeordnete tropfenbildende Regionen“ in eine konkrete Menge kurzer, zusammensetzbarer Motive. Für Nicht‑Experten lautet die Kernbotschaft, dass Wissenschaftler nun die kleinen Proteinsegmente lesen und schreiben können, die steuern, wie zelluläre Tropfen sich zusammenlagern, vermischen und fehlfunktionieren. Das eröffnet Wege zu schnellerer Entdeckung krankheitsverursachender Mutationen in diesen Segmenten, zu klareren mechanistischen Studien darüber, wie Kondensate die Zellphysiologie organisieren, und schließlich zur rationalen Entwicklung von Proteinen, die Tropfen für therapeutische oder synthetische Biologie‑Anwendungen gezielt steuern.
Zitation: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Schlüsselwörter: biomolekulare Kondensate, intrinsisch ungeordnete Proteine, Phasentrennung, Deep Learning, Proteinmotive