Clear Sky Science · de
Hepatozyten, funktionell umprogrammiert durch KIAA1199-hohe kolorektale Tumorzellen, begünstigen die Ansammlung pro‑metastatischer Egr1+ Neutrophiler
Wenn Darmkrebs die Leber ins Visier nimmt
Die meisten Menschen stellen sich die Ausbreitung von Krebs so vor, dass einzelne Zellen einfach abspringen und zu neuen Organen wandern. Diese Studie zeigt eine beunruhigendere Geschichte: kolorektale Tumoren können die Leber lange bevor Krebszellen eintreffen still und leise umprogrammieren und so einen einladenden „Boden“ schaffen, in dem sich künftige Tumoren leicht festsetzen. Das Verständnis dieser verborgenen Vorbereitungsphase könnte den Weg für Behandlungen öffnen, die Lebermetastasen — die Haupttodesursache bei kolorektalem Krebs — stoppen, bevor sie entstehen.
Ein heimliches Setup, bevor Tumoren ankommen
Kolorektaler Krebs metastasiert häufig in die Leber, doch nur manche Tumoren tun dies aggressiv. Die Autorinnen und Autoren konzentrierten sich auf ein Molekül namens KIAA1199, das in Hochrisiko‑Kolorektaltumoren stark exprimiert wird. In Mausmodellen und Patient*innenproben zeigten Tumoren mit hoher KIAA1199‑Expression nicht nur schnelleres Wachstum; sie bereiteten die Leber auch zur Bildung einer „prä‑metastatischen Nische“ vor — einer Mikroumgebung, die eindringenden Krebszellen besonders freundlich gesinnt ist. Selbst wenn Lebertumoren experimentell aus einer anderen Quelle eingesetzt wurden, entwickelten Tiere mit KIAA1199‑reichen Kolontumoren deutlich mehr Lebermetastasen und starben früher. Das zeigt, dass Signale vom Primärtumor — nicht nur wandernde Krebszellen — die Leber im Voraus umgestalten.
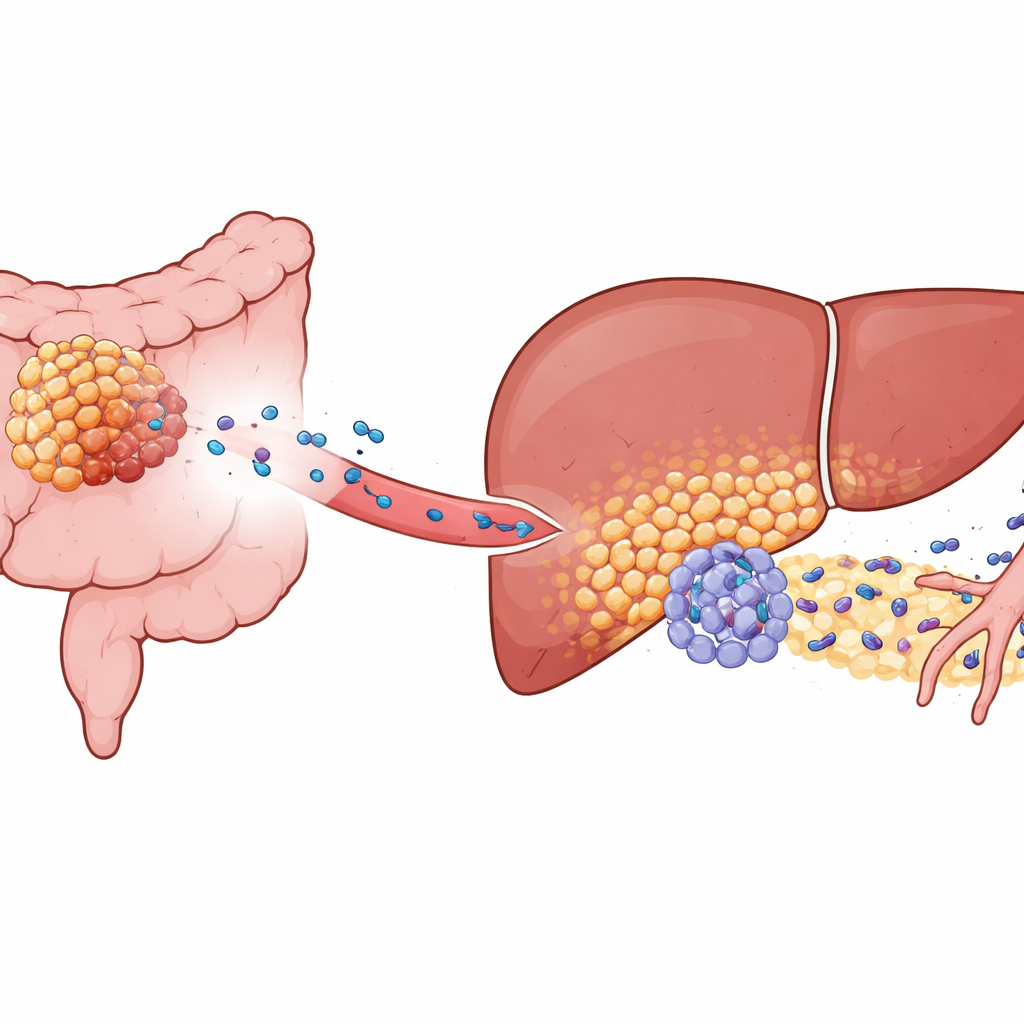
Leberzellen werden zu Helfern des Tumors umprogrammiert
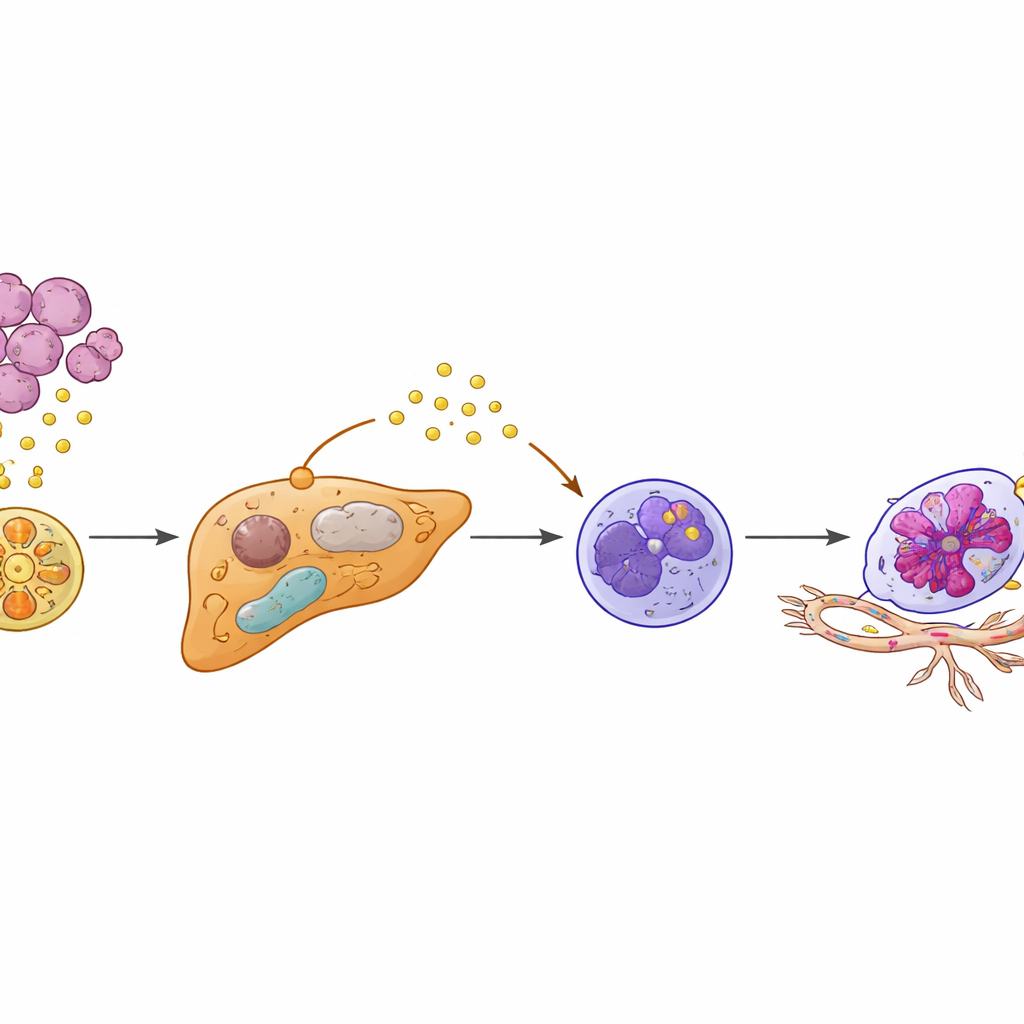
Bei genauerer Untersuchung nutzten die Forschenden Einzelzellsequenzierung und räumliches Mapping, um Lebergewebe hochaufgelöst zu analysieren. Sie entdeckten eine eigene Untergruppe von Hepatozyten — normalerweise die Arbeitspferde der Leber — die „funktionell umprogrammiert“ waren. Diese Zellen traten nur in Gegenwart von KIAA1199‑starken Tumoren auf. Statt wie üblich Stoffwechselaufgaben zu übernehmen, wechselten die veränderten Hepatozyten zu einem eher malignen‑ähnlichen Stoffwechselprofil und reduzierten die Aktivität eines schützenden Regulationsfaktors namens PPARγ, der normalerweise Entzündungs‑ und Stressreaktionen dämpft. Mit unterdrücktem PPARγ begannen diese Hepatozyten, hohe Mengen des Proteins SAA2 zu produzieren und in ihre Umgebung abzugeben, insbesondere an den Rändern, wo Lebergewebe auf eindringende Tumorzellen trifft.
Aus gewöhnlichen Verteidigern werden pro‑metastatische Neutrophile
Neutrophile — weiße Blutkörperchen, die vor allem für die Bekämpfung von Infektionen bekannt sind — verhielten sich in dieser präparierten Leber ebenfalls ungewöhnlich. Die Autor*innen fanden eine spezielle Untergruppe mit einem „Egr1+“-Signaturprofil, benannt nach einem Transkriptionsfaktor, der die Funktion dieser Zellen umgestaltet. Anstatt bereits verändert aus dem Blutstrom zu kommen, schienen Neutrophile lokal von den umprogrammierten Hepatozyten umgeschult zu werden. Von Hepatozyten freigesetztes SAA2 bindet an einen Rezeptor namens FPR2 auf benachbarten Neutrophilen und aktiviert eine interne PI3K‑AKT‑Signalachse, die Egr1 stabilisiert. Das Ergebnis sind langlebigere, hochaktive Neutrophile, die große Mengen VEGFA absondern — einen starken Treiber neuer Blutgefäßbildung. Diese Egr1+ Neutrophilen sammelten sich an der Schnittstelle zwischen Tumor und Leber, genau dort, wo neue, fragile Blutgefäße sprossen.
Aufbau von Blutgefäßen, die Tumorzellen willkommen heißen
Die Studie zeigt, dass diese umgeschulten Neutrophilen keine Beobachter sind — sie remodeln aktiv die Gefäßstruktur der Leber. Im Zellkulturmodell veranlassten von Egr1+ Neutrophilen freigesetzte Faktoren Endothelzellen zum Wachsen, Wandern und zur Bildung röhrenartiger Strukturen, die neuen Gefäßen ähneln. In Mäusen förderte die Zugabe von Egr1+ Neutrophilen Lebermetastasen und beschleunigte das Sterben. Das Blockieren zentraler Schritte der Kaskade — entweder das SAA2–FPR2‑Signal zu den Neutrophilen oder die nachgeschaltete PI3K‑AKT‑Achse — unterbrach die Überlebenssignale der Neutrophilen und die VEGFA‑Produktion, verringerte die Gefäßneubildung und die metastatische Ausbreitung. Ebenso senkte die Wiederherstellung der PPARγ‑Aktivität in Hepatozyten mit dem Diabetesmedikament Rosiglitazon die SAA2‑Werte, verhinderte das Entstehen von Egr1+ Neutrophilen und reduzierte in präklinischen Modellen deutlich Lebermetastasen.
Vom Mechanismus zur Vorhersage und Prävention
Da KIAA1199 im Tumor und SAA2 in der Leber an der Spitze dieser Kaskade stehen, prüften die Autor*innen, ob diese Proteine helfen könnten, Patient*innen mit hohem Risiko für Lebermetastasen zu identifizieren. In mehreren Patient*innenkohorten hatten Personen mit hohen Blutspiegeln beider Marker ein deutlich erhöhtes Risiko, Lebermetastasen zu entwickeln, und taten dies schneller. Ein einfacher kombinierter KIAA1199–SAA2‑Score übertraf die einzelnen Marker bei der Risikovorhersage und wurde in ein klinisches Nomogramm verpackt, das die Wahrscheinlichkeit eines individuellen Patienten für Leberbefall innerhalb der nächsten zwei Jahre schätzt. Zusammen zeichnen die Befunde ein klares Bild: KIAA1199‑starke Darmtumoren senden vesikelgetragene Signale aus, die Hepatozyten umprogrammieren, welche wiederum benachbarte Neutrophile in langlebige, gefäßbildende Komplizen verwandeln. Durch das Anvisieren dieser KIAA1199–PPARγ/SAA2–Egr1‑Achse — mittels Stoffwechselwirkstoffen, immunmodulierender Mittel oder beidem — könnte es möglich sein, nicht nur bestehende Lebermetastasen zu behandeln, sondern sie von vornherein am Entstehen zu hindern.
Zitation: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Schlüsselwörter: Lebermetastasen bei kolorektalem Krebs, prä‑metastatisches Nisch, Neutrophile, Umprogrammierung von Hepatozyten, Tumormikroumgebung