Clear Sky Science · de
Zweistufige Aktivierung des Spannungssensors des humanen KV7.4-Kanals und Wirkung einer mit Taubheit assoziierten Mutation
Wie winzige Torwächter in der Ohr das Hören formen
Im Innenohr beruht das Hören auf mikroskopischen Zellen, die Schallvibrationen in elektrische Signale für das Gehirn umwandeln. Diese Studie konzentriert sich auf ein spezifisches Protein, den Kv7.4-Kaliumkanal, der wie ein winziges Tor in der Membran dieser Zellen wirkt. Öffnet oder schließt sich dieses Tor nicht richtig, kann das Gehör im Lauf der Zeit allmählich nachlassen. Die Forscher wollten genau verstehen, wie dieses Tor auf elektrische Signale reagiert und warum eine bestimmte vererbte Mutation, die mit Taubheit in Verbindung steht, das Tor fehlregeln lässt.
Das Tor in unseren Hörzellen
Die äußeren Haarzellen der Cochlea helfen, den Schall zu schärfen und Vibrationen zu verstärken. Ihre Funktion hängt stark von Kaliumkanälen ab, einschließlich Kv7.4, die Kaliumionen aus der Zelle herausströmen lassen und nach einer Schallreizung den elektrischen Zustand der Zelle zurücksetzen. Das Kv7.4-Protein besitzt eine „Pore“, durch die Ionen passieren, und einen „Spannungssensor“, der Änderungen der elektrischen Ladung der Zelle erkennt und der Pore signalisiert, wann sie öffnen soll. Defekte im Gen, das Kv7.4 (KCNQ4) codiert, sind als Ursache einer Familienform des fortschreitenden Hörverlusts bekannt. Bislang waren jedoch die detaillierten Bewegungen des Spannungssensors und deren Steuerung der Porenöffnung nur unzureichend verstanden.
Beobachtung eines molekularen Schalters in Echtzeit
Um die Bewegungen des Spannungssensors zu verfolgen, nutzte das Team eine Methode namens Spannungsklemmen-Fluorometrie, die elektrische Messungen mit lichtbasierten Anzeigen kombiniert. Sie konstruierten eine Variante von Kv7.4, die an der Außenseite der spannungssensitiven Region eine einzelne zusätzliche chemische Stelle trägt. An diese Stelle befestigten sie fluoreszierende Farbstoffe, deren Helligkeit sich ändert, wenn sich ihre Umgebung verschiebt. Durch das Anlegen unterschiedlicher Spannungen an der Zelle und das gleichzeitige Messen von elektrischen Strömen und Fluoreszenzänderungen konnten sie verfolgen, wie sich der Sensor bewegte, während der Kanal zwischen geschlossenen und offenen Zuständen wechselte. Außerdem führten sie die aus Patienten bekannte Mutation R216H in diesen konstruierten Kanal ein, um zu sehen, wie sie diese Bewegungen veränderte.
Ein zweistufiger Schalter hinter einem langsam öffnenden Tor
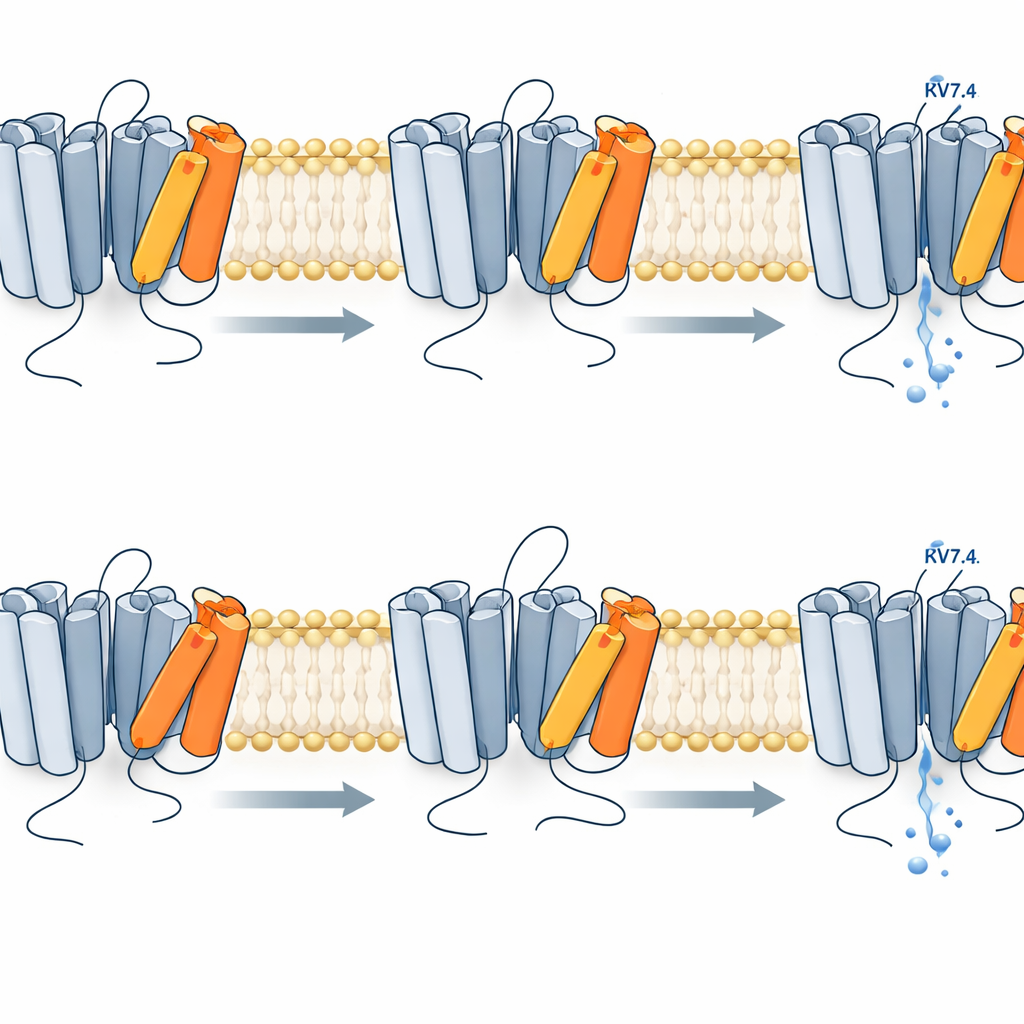
Die Experimente zeigten, dass der Spannungssensor in Kv7.4 nicht einfach von „aus“ auf „an“ springt. Stattdessen bewegt er sich in mindestens zwei unterscheidbaren Schritten. Zuerst, bei relativ niedrigen Spannungen, verschiebt sich der Sensor schnell von einer Ruhe- in eine Zwischenstellung, während die Pore noch geschlossen bleibt. Erst bei stärkerer Depolarisation vollendet der Sensor eine langsamere zweite Bewegung in einen voll aktiven Zustand, die eng mit der Porenöffnung und dem Auftreten des Kaliumstroms verknüpft ist. Dieses zweistufige Verhalten wurde deutlich, als die Forscher die zeitliche Abfolge und Spannungsbereiche der Fluoreszenzsignale mit der elektrischen Aktivität des Kanals verglichen. Der erste Schritt trat bei negativeren Spannungen und deutlich schneller auf, während der zweite Schritt sowohl im Spannungsbereich als auch in der trägen Zeitkonstante mit der Kanalöffnung übereinstimmte.
Wenn eine einzige Substitution den Sensor destabilisiert
Die mit Taubheit assoziierte R216H-Mutation verändert eine positiv geladene Baueinheit in der spannungssensitiven Helix. Mit denselben optischen und elektrischen Messungen fanden die Forscher, dass diese Mutation sowohl die beiden Sensorsprünge als auch die Porenöffnung zu positiveren Spannungen verschiebt und deren Empfindlichkeit gegenüber Spannungsänderungen verringert. Anders gesagt: Es bedarf eines stärkeren elektrischen Anstoßes, um dasselbe Aktivierungsniveau zu erreichen, und der Kanal öffnet sich seltener. Computersimulationen der dreidimensionalen Struktur des Kanals stützten diese Sicht: Beim Mutanten wackelt die entscheidende Helix, die R216H trägt, stärker und bildet weniger stabilisierende Wechselwirkungen mit benachbarten negativ geladenen Resten. Das macht die vollständig aktivierte Konfiguration weniger stabil, sodass der Sensor eher wieder in die Ruheposition zurückfällt und die Pore dazu tendiert, früher zu schließen.
Warum diese mikroskopischen Bewegungen wichtig sind
Indem die Studie zeigt, dass Kv7.4 auf eine zweistufige Bewegung des Spannungssensors angewiesen ist, um zu öffnen, und darlegt, wie eine einzelne vererbte Veränderung diese Schritte schwächen kann, liefert sie eine klare mechanistische Erklärung für eine Form des fortschreitenden Hörverlusts. In gesunden Kanälen vollendet der Sensor zuverlässig den langsamen zweiten Schritt, der das Tor öffnet und den konstanten Kaliumfluss ermöglicht, der für die normale Schallverstärkung in der Cochlea und für den richtigen Tonus der Blutgefäße im Körper erforderlich ist. In Kanälen mit der R216H-Mutation ist dieser letzte Schritt destabilisiert, sodass sich unter Alltagsbedingungen weniger Kanäle öffnen und dies im Lauf der Zeit zu Hörverlust führt. Das Verständnis dieses detaillierten Schaltmechanismus bildet die Grundlage für die Entwicklung von Wirkstoffen, die den aktiven Sensorzustand stabilisieren oder die Kanalöffnung fördern könnten, mit dem langfristigen Ziel, das Hören betroffener Personen zu schützen oder wiederherzustellen.
Zitation: Nappi, M., Frampton, D.J.A., Kusay, A.S. et al. Two-step voltage-sensor activation of the human KV7.4 channel and effect of a deafness-associated mutation. Nat Commun 17, 2381 (2026). https://doi.org/10.1038/s41467-026-69249-8
Schlüsselwörter: Hörverlust, Ionenkanäle, Kv7.4, Spannungssensor, Innenohr