Clear Sky Science · de
Reduzierte Methylierung von Histon 3.3 Lysin 4 in der medialen ganglionären Eminenz und im Hypothalamus reproduziert Phänotypen neuroentwicklungsbedingter Störungen
Wie winzige chemische Markierungen Gehirn und Körper formen
Warum führen manche genetischen Veränderungen sowohl zu Lernproblemen als auch zu ungewöhnlichem Wachstum – beispielsweise sehr klein in der Kindheit, aber fettleibig im Erwachsenenalter? Diese Studie untersucht winzige chemische Markierungen an DNA-verpackenden Proteinen im Gehirn und zeigt, wie ihre Störung in nur zwei Schlüsselregionen weitreichende Folgen haben kann: Anfälle, angstähnliches Verhalten, Gedächtnisstörungen und dramatische Veränderungen der Körpergröße bei Mäusen.
Schalter an den Dimmerknöpfen des Genoms
In jeder Gehirnzelle ist die DNA um spoelförmige Proteine gewickelt, die als Histone bezeichnet werden. Chemische Markierungen auf diesen Histonen wirken wie Dimmerknöpfe und regulieren Gruppen von Genen hoch- oder herunter. Eine solche Markierung, hinzugefügt an einer Stelle namens H3K4, steht stark mit Genaktivierung in Verbindung. Studien am Menschen haben gezeigt, dass Personen mit Defekten in Enzymen, die diese Markierung anbringen oder entfernen, häufig neuroentwicklungsbedingte Störungen aufweisen, die geistige Beeinträchtigung, Epilepsie und abnormales Körperwachstum kombinieren. Es war jedoch unklar, welche Gehirnzellen am empfindlichsten für diese Störung sind und wie ihr Funktionsverlust Erregbarkeit des Gehirns und den Stoffwechsel des gesamten Körpers verbinden könnte.
Zielgerichtet auf zwei kritische Hirnhubs
Die Forschenden erzeugten Mäuse, bei denen eine mutierte Version eines Histonproteins (H3.3K4M) nur in Zellen eingeschaltet wurde, die aus zwei embryonalen Hirnregionen stammen: der medialen ganglionären Eminenz, die viele der hemmenden „Brems“-Zellen des Gehirns produziert, und dem sich entwickelnden Hypothalamus, der Appetit, Hormone und Energiebalance steuert. Diese Mutation blockiert spezifisch die Methylierung von H3K4, ohne die Histone selbst zu beseitigen. Tests bestätigten, dass das mutierte Protein weit verbreitet in den anvisierten Bereichen vorhanden war und dass die normalen H3K4-Markierungen dort stark reduziert waren, während die Gesamtmenge an Histonen stabil blieb. Dieses Design ahmt viele menschliche Zustände nach, in denen nur eine Kopie eines H3K4-bezogenen Gens fehlerhaft ist, statt vollständig zu fehlen.
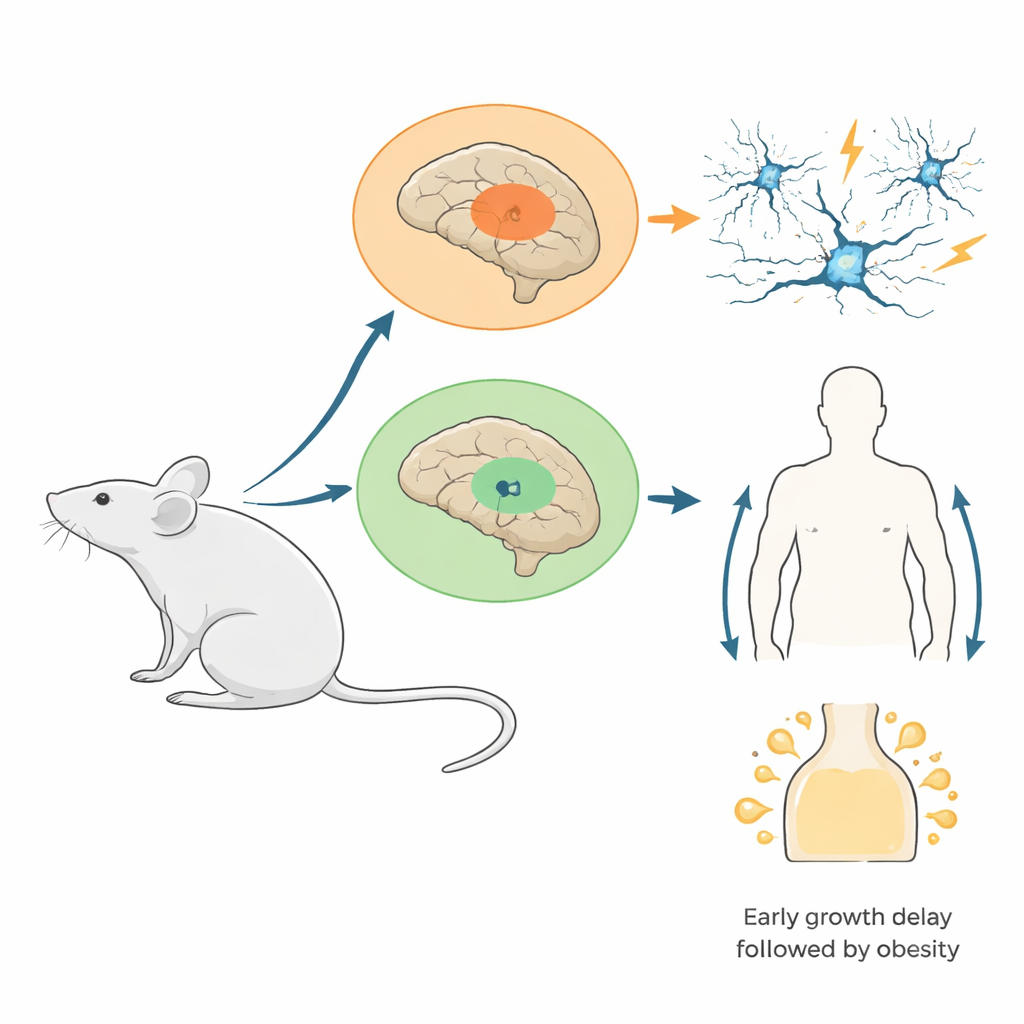
Von fehlenden Bremszellen zu anfallsbereiten Netzwerken
Als diese Mäuse heranwuchsen, wurden die Folgen für die Schaltkreise des Gehirns deutlich. Junge Mutanten hatten weniger hemmende Interneuronen in Cortex und Hippocampus, besonders ein schnell feuernder Typ, der normalerweise neuronale Rhythmen eng timt. Detaillierte Messungen zeigten, dass verbleibende Interneuronen zwar vorhanden, ihre elektrischen Eigenschaften jedoch variabler waren, was auf eine gestörte Reifung hindeutet. Bei Stimulation des Hippocampus in Hirnschnitten waren die üblichen hochfrequenten „Gamma“-Oszillationen – elektrische Rhythmen, die mit Informationsverarbeitung verknüpft sind – schwächer und langsamer, und abnorme, burstartige Ereignisse traten auf. In lebenden Tieren entwickelten viele Mutanten, insbesondere Weibchen, spontane Anfälle und zeigten eine deutlich erhöhte Empfindlichkeit gegenüber medikamentös ausgelösten Anfällen. Früh in der Entwicklung führte das Team den Verlust dieser Zellen hauptsächlich auf eine schlechte Migration der Interneuronen in die Großhirnrinde zurück, nicht auf vermehrten Zelltod oder reduzierte Zellteilung.
Umschalten der Genaktivität in anfallsrelevanten Zellen
Um diese physischen Veränderungen mit Genregulation zu verknüpfen, verwendete das Team Single-Nucleus-Sequenzierung, die sowohl Genaktivität als auch DNA-Zugänglichkeit einzelner Zellen liest. In der embryonalen medialen ganglionären Eminenz waren die meisten in Mutanten veränderten Gene herunterreguliert, darunter Schlüsselregulatoren, die Zellen in spezifische hemmende Schicksale lenken. In adulten Interneuronen verschob sich das Gleichgewicht zwischen Subtypen, und Gencluster, die an der Ausbildung von Verbindungen und der Kontrolle von Kaliumströmen beteiligt sind – Flüsse, die die Feuerrate mitbestimmen – waren fehlreguliert. Netzwerkanalysen hoben die koordinierte Störung von Kaliumkanalgenen hervor, die bereits als Einflussfaktoren für Epilepsie und Hirnrhythmik bekannt sind, und lieferten damit eine direkte molekulare Verbindung zwischen dem Verlust einer Histonmarke, veränderter Interneuron-Identität und Anfallsanfälligkeit.
Hypothalamische Unausgewogenheit und eine zweiphasige Wachstumskurve
Der Hypothalamus erzählte eine komplementäre Geschichte, die sich auf das Körperwachstum konzentrierte. Als Jungtiere waren die mutierten Mäuse kleiner und ein erheblicher Teil starb früh. Überlebende jedoch fraßen später mehr, sammelten Fett an und entwickelten hohe Leptinspiegel, was auf Adipositas und wahrscheinliche Leptinresistenz hinweist. Einzelzellanalysen des embryonalen Hypothalamus zeigten mehr teilende Vorläuferzellen, aber weniger Zellen, die für wichtige fütterungsbezogene Kerngebiete bestimmt sind, besonders in Regionen, die normalerweise den Ernährungszustand wahrnehmen und das Wachstumshormon regulieren. Im erwachsenen Hypothalamus veränderte sich die zelluläre Zusammensetzung: Astrozyten nahmen stark zu, Oligodendrozyten nahmen ab, und spezialisierte Barrierezellen, sogenannte Tanyzyten, sowie benachbarte Gliazellen verloren ihre geordnete Anordnung an der Schnittstelle des Gehirns zu zirkulierenden Hormonen und Nährstoffen. Diese strukturellen und genexpressiven Änderungen verzerren wahrscheinlich, wie das Gehirn Energiespeicher wahrnimmt und den Appetit steuert.
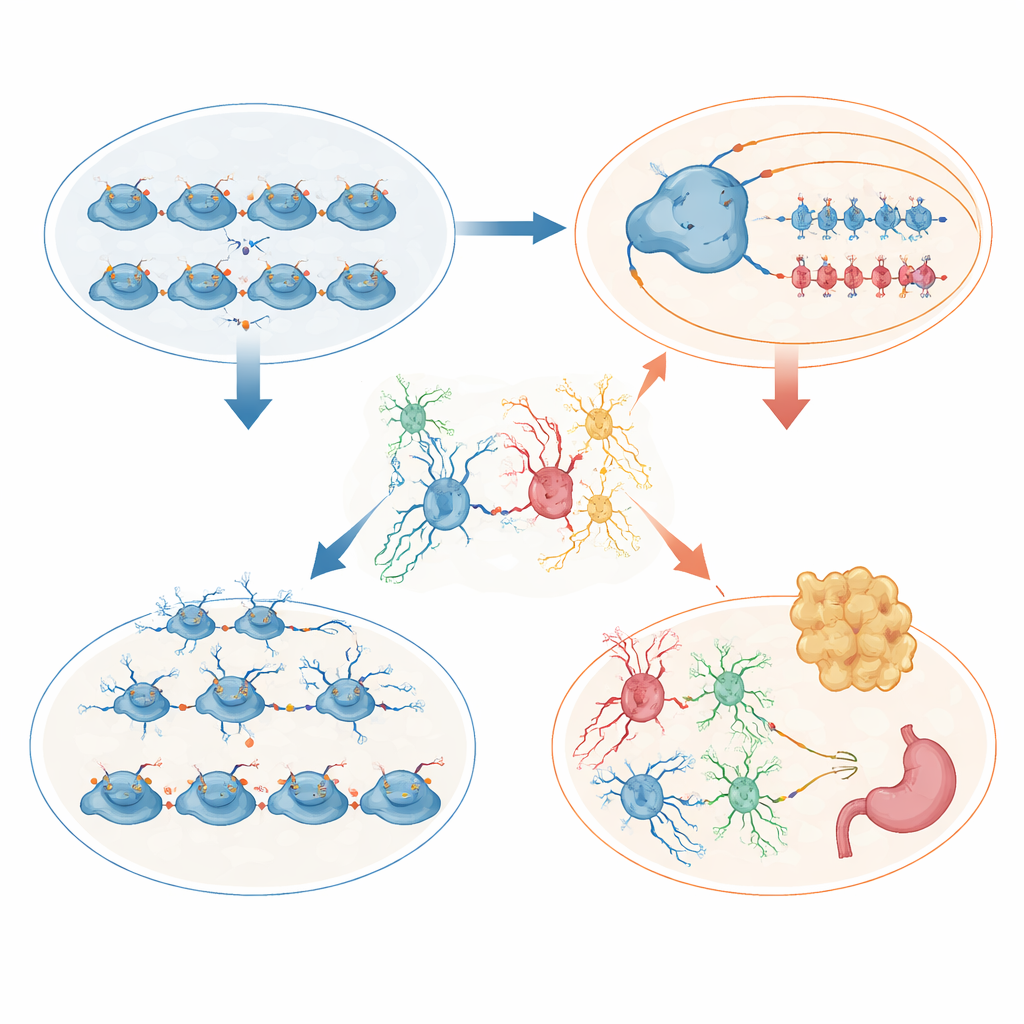
Verhaltensliche Echos menschlicher neuroentwicklungsbedingter Störungen
Das Verhalten der Mäuse spiegelte Symptome wider, die bei vielen neuroentwicklungsbedingten Erkrankungen beobachtet werden. Sie zeigten stärkere angstähnliche Verhaltensweisen, veränderten Gang, reduzierte spontane Aktivität zu Hause und schlechte Leistungen in Tests, die Gedächtnis, Objekterkennung und die Filterung von Schreckreaktionen prüfen. Einige Tests zeigten zudem vermehrt impulsartiges Verhalten. Über mehrere Messungen hinweg waren Weibchen tendenziell stärker betroffen als Männchen, was darauf hindeutet, dass geschlechtsspezifische Hormonsysteme und Genregulation mit Histonmarken interagieren könnten, um die Verwundbarkeit zu beeinflussen.
Was das für die menschliche Gesundheit bedeutet
Insgesamt zeigen die Befunde, dass das Abschwächen einer Reihe von Histonmarken in nur zwei embryonalen Hirnhubs ausreicht, um ein breites Spektrum von Problemen zu reproduzieren: weniger hemmende „Bremsen“, instabile Netzwerke, Anfälle, gestörte fütterungsbezogene Schaltkreise und abnormes Körperwachstum. Für Nicht-Spezialisten ist die zentrale Botschaft, dass epigenetische Markierungen wie die H3K4-Methylierung keine vagen Anhängsel sind, sondern präzise Steuerknöpfe, die entwickelnden Gehirnzellen helfen, zur richtigen Zeit den richtigen Typ am richtigen Ort zu werden. Wenn diese Knöpfe falsch eingestellt sind, wie bei vielen seltenen genetischen Syndromen, kann das Ergebnis eine eng verknüpfte Kombination kognitiver, verhaltensbezogener und metabolischer Symptome sein. Das Verständnis dieser gemeinsamen Ursachen könnte letztlich Therapien anleiten, die nicht nur ein einzelnes Symptom wie Anfälle oder Adipositas korrigieren, sondern das vernetzte System, das sie hervorbringt.
Zitation: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Schlüsselwörter: Epigenetik, Interneuronen, Hypothalamus, Anfälle, Adipositas