Clear Sky Science · de
Phasentrennung und Fibrillisierung zu entkoppeln bewahrt die Aktivität biomolekularer Kondensate
Warum das für die Gehirngesundheit wichtig ist
Viele Erkrankungen des Gehirns, darunter Alzheimer, gehen mit Proteinen einher, die sich mit der Zeit zu harten, faserigen Verfilzungen verklumpen. Dieselben Proteine können auch weichere, tropfenartige Strukturen innerhalb von Zellen bilden, die helfen, biochemische Vorgänge zu organisieren – ein bisschen wie winzige, flüssige Arbeitsstationen. Diese Studie stellt eine zentrale Frage: Kann man das schädliche Verhärten dieser Tropfen zu Fasern verhindern, ohne ihre nützliche Alltagsfunktion zu zerstören? Die Autoren zeigen, dass ein häufiger Zellstoffwechselmetabolit, die Aminosäure L-Arginin, genau das für ein wichtiges Alzheimer-assoziiertes Protein namens Tau leisten kann.
Vom frei schwimmenden Protein zu winzigen Tropfen
Innerhalb von Zellen bleiben bestimmte Proteine nicht immer gleichmäßig im Zellinneren verteilt. Stattdessen können sie sich zu Tropfen zusammenlagern, so genannten biomolekularen Kondensaten, die sich wie sehr weiche Gele oder dickflüssige Flüssigkeiten verhalten. Das Team konzentrierte sich auf Tau, ein Protein, das normalerweise beim Aufbau und der Stabilisierung von Mikrotubuli hilft—hohle Filamente, die in Nervenzellen wie Straßen funktionieren. Tau ist auch berüchtigt dafür, Amyloidfibrillen zu bilden, die starren Fasern, die in den Verfilzungen vieler neurodegenerativer Erkrankungen zu finden sind. Um zu untersuchen, wie Tau-Tropfen sich im Laufe der Zeit entwickeln, konstruierten die Forscher eine Version des Proteins, SynTag-Tau genannt, die aktive Kondensate bildet, die sich auf einem experimentell günstigen Zeitskalenprofil in Amyloidfibrillen verwandeln, ohne starke Zusatzstoffe.
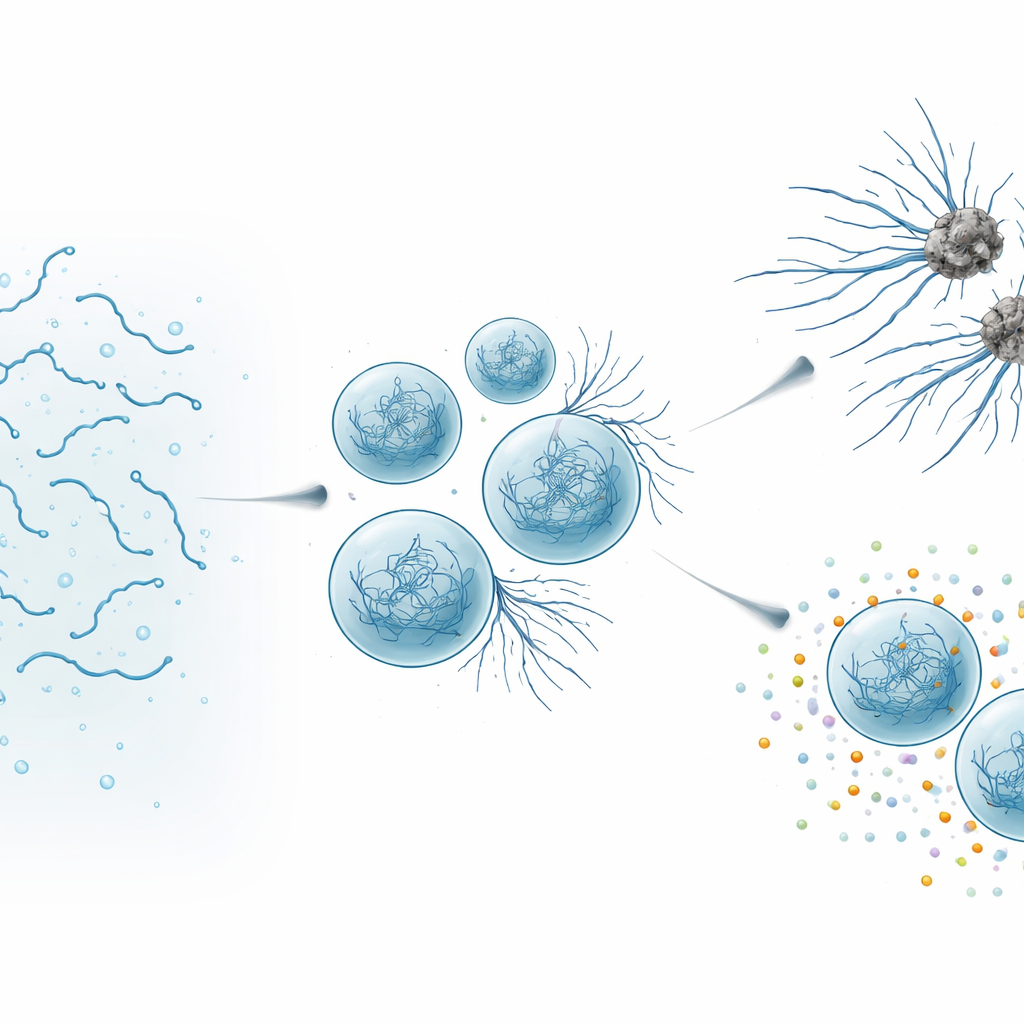
Wenn hilfreiche Tropfen schädlich werden
Mithilfe hochauflösender Mikroskopie und biophysikalischer Messungen beobachteten die Autoren, wie sich SynTag-Tau-Tropfen über Stunden veränderten. Frische Tropfen verhielten sich wie Flüssigkeiten: sie verschmolzen leicht, ihre Moleküle bewegten sich schnell und es gab keinen Hinweis auf geordnete Strukturen. Mit der Zeit verlangsamten und versteiften sich die Tropfen, und dünne Fasern begannen von ihren Oberflächen in die umgebende Lösung zu sprießen. Empfindliche optische Methoden zeigten, dass diese Fasern die dicht gepackte „Cross–Beta“-Architektur enthielten, die für Amyloid typisch ist. Wichtig war, dass die Oberfläche—die Grenze zwischen dem dichten Tropfen und der umgebenden Flüssigkeit—als Brennpunkt diente, an dem Fibrillen zuerst auftauchten. Während die Tropfen alterten und mehr Fasern ausbildeten, litt Taus normale Funktion: Die Kondensate wurden schlechter darin, Tubulin anzuziehen, den Baustein der Mikrotubuli, und verloren schließlich ihre Fähigkeit, die Mikrotubulusbildung zu unterstützen.
Kleine Moleküle, die das Gleichgewicht kippen
Die Forscher fragten dann, ob einfache Metaboliten den Übergang von Flüssigkeit zu Faser verlangsamen oder verhindern könnten, während die Tropfen selbst intakt blieben. Bei einem Screening mehrerer natürlich vorkommender kleiner Moleküle fanden sie, dass die positiv geladenen Aminosäuren L-Arginin und L-Lysin die Bildung von Amyloidfibrillen aus SynTag-Tau-Kondensaten stark verzögerten oder blockierten, ohne bei realistischen, niedrigen Millimolaren Konzentrationen die Tropfenbildung zu unterdrücken. Im Gegensatz dazu beschleunigten negativ geladene Aminosäuren wie Glutamat und Aspartat die Fibrillenbildung, und allgemein proteinstörende Chemikalien halfen entweder nicht oder störten die Tropfen selbst. Ein fluoreszenzmarkiertes Analogon von L-Arginin zeigte, dass dieses Molekül es bevorzugt, sich innerhalb der Tau-Kondensate statt außerhalb anzusiedeln, was nahelegt, dass es dort wirkt, wo es am meisten gebraucht wird.
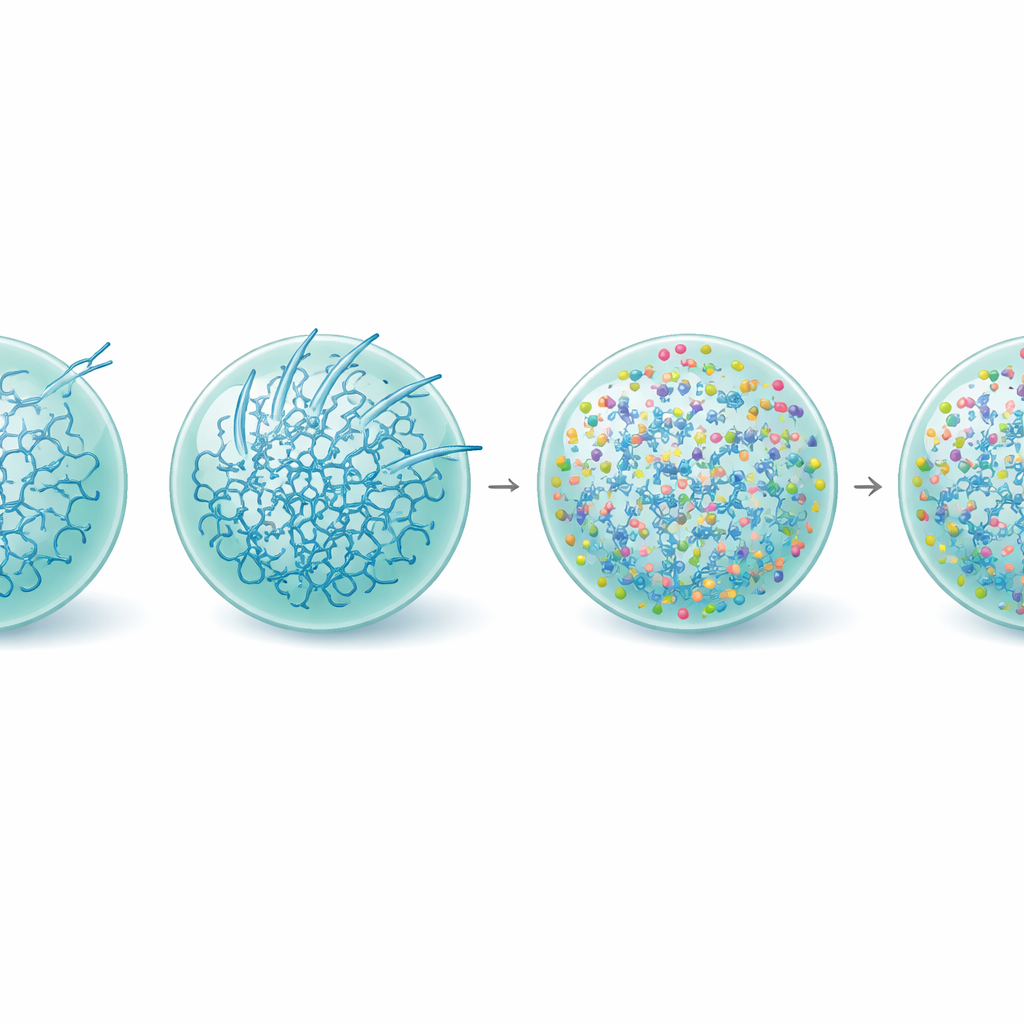
Den Tropfen versteifen und die Funktion erhalten
Bei tiefergehenden Untersuchungen analysierte das Team, wie L-Arginin das Innenleben der Tau-Tropfen verändert. Messungen der Proteinstruktur zeigten, dass bei Anwesenheit von L-Arginin der Anteil der Tau-Moleküle, die die starren, beta-reichen Formen annehmen, die mit Amyloid assoziiert sind, selbst in älteren Tropfen reduziert war. Video-basierte Nanorheologie—bei der die Bewegung winziger Partikel innerhalb der Kondensate verfolgt wird—zeigte, dass L-Arginin die Tau-Tropfen tatsächlich viskoelastischer machte, das heißt ihr internes Netzwerk wurde stärker und stärker vernetzt, blieb dabei aber flüssig-ähnlich. Diese Verstärkung scheint das System in einem metastabilen, funktionalen Zustand zu halten und erhöht die energetische Barriere für die Fibrillenbildung, besonders an der Tropfenoberfläche. Konsistent damit rekrutierten mit L-Arginin behandelte Kondensate weiterhin Tubulin gleichmäßig und unterstützten das Mikrotubuluswachstum lange nachdem unbehandelte Tropfen inaktiv geworden waren.
Was das für zukünftige Therapien bedeutet
Die Arbeit zeigt, dass die Kräfte, die die Bildung von Protein-Tropfen antreiben, und jene, die die schädliche Fasernbildung vorantreiben, verwandt, aber trennbar sind. Durch das Feinabstimmen der Chemie innerhalb von Kondensaten mit einem Metaboliten wie L-Arginin ist es möglich, den vorteilhaften, flüssigkeitsähnlichen Zustand zu bewahren und gleichzeitig den Übergang zu krankheitsassoziierten Amyloidfasern zu verzögern oder zu verhindern. Obwohl diese Studie ein speziell konstruiertes Tau-System in vitro verwendet, liefert sie einen Prinzipnachweis: Kleine Moleküle, die die Stabilität von Kondensaten selektiv stärken, könnten eines Tages Zellen davor schützen, dass sich toxische Proteinaggregate allmählich aufbauen, ohne die normalen, organisierenden Rollen biomolekularer Kondensate zu blockieren.
Zitation: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Schlüsselwörter: Tau-Protein, biomolekulare Kondensate, Amyloidfibrillen, L-Arginin, Neurodegeneration