Clear Sky Science · de
Epilepsie-assoziierte FOXJ3-Varianten verknüpfen ein Transkriptionsprogramm des PTEN-mTOR-Signalwegs mit der neuronalen Spezifikation und der kortikalen Lamination
Wenn die Verschaltung des Gehirns leicht vom Kurs abkommt
Epilepsie beginnt oft im Kindesalter, doch bei vielen jungen Patientinnen und Patienten zeigen bildgebende Untersuchungen nichts Offensichtliches. Diese Studie geht einer verborgenen Ursache nach: winzige Veränderungen in einem Gen namens FOXJ3, die unterschwellig die Art und Weise verändern, wie die äußere Hirnschicht, der Kortex, aufgebaut wird. Anhand der Untersuchung dieses Gens in Familien mit fokaler Epilepsie und in sich entwickelnden Mäusegehirnen zeigen die Forschenden, wie frühe Fehltritte bei Zellentstehung, -bewegung und -schichtung schließlich zu Anfällen führen können.
Eine subtile Fehlbildung hinter schwer behandelbaren Anfällen
Viele Kinder mit medikamentenresistenter fokaler Epilepsie tragen eine sogenannte fokale kortikale Dysplasie (FCD), bei der Bereiche des Kortex fehlgebildet sind. Diese Regionen enthalten fehlplatzierte und ungewöhnlich große Nervenzellen und sind ein häufiger Grund dafür, dass Medikamente Anfälle nicht kontrollieren. Die molekulare Ursache von FCD ist jedoch oft unbekannt, und Standard-MRTs übersehen kleine oder flache Defekte. Die Autorinnen und Autoren begannen mit einer Familie, in der mehrere Mitglieder fokale Epilepsie und Hinweise auf FCD zeigten. Sorgfältige Genomanalysen wiesen auf seltene Veränderungen in FOXJ3 hin, einem Gen, das zuvor nicht mit Epilepsie in Verbindung gebracht worden war. Zusätzliche Fälle aus großen Genetiksammlungen ergaben weitere Personen mit ungewöhnlichen FOXJ3-Varianten und fokalen Anfällen, was nahelegt, dass dieses Gen wiederholt eine Rolle bei solchen Erkrankungen spielen könnte.
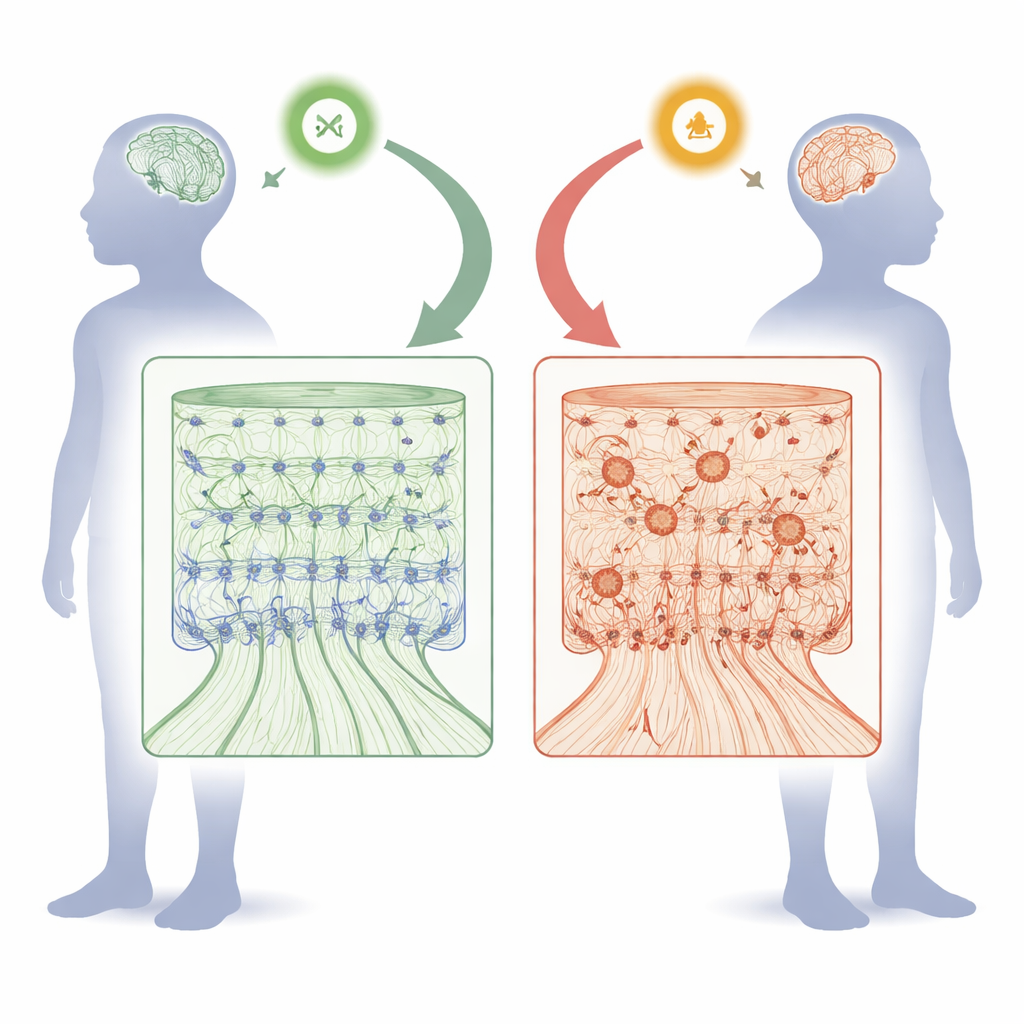
Wie FOXJ3 die Denkoberfläche des Gehirns mitgestaltet
Während der fetalen Entwicklung wird der Kortex wie ein mehrstöckiges Gebäude aufgebaut. Stammzellähnliche Zellen, die die innere Oberfläche des Gehirns auskleiden, teilen sich und schicken dann Neuronen entlang radialer "Gerüste" nach außen, um sechs geordnete Schichten zu bilden. Das Team fand heraus, dass FOXJ3 sowohl in diesen progenitorischen Stammzelltypen als auch in jungen Neuronen aktiv ist, wobei seine Aktivität in den Progenitoren nach einem bestimmten Zeitpunkt in der mittleren Gestationszeit natürlicherweise abnimmt. Mit Gen-Silencing-Werkzeugen in Maus-Embryonen reduzierten die Forschenden Foxj3-Spiegel in verschiedenen Stadien und beobachteten die Folgen. Ein früher Verlust von Foxj3 ließ neugeborene Neurone langsamer wandern und in falschen Schichten landen. Zellen, die eigentlich zu tiefen Schichten hätten werden sollen, nahmen stattdessen Identitäten an, die für obere Schichten typisch sind, und korpuskallosale Projektionsneurone, die die beiden Hirnhälften verbinden, wurden im Übermaß gebildet. Später in der Entwicklung hingegen hatte die Reduktion von Foxj3 deutlich mildere Effekte, was zeigt, dass seine Rolle hochgradig zeitabhängig ist.
Zellteilung und Wachstum im Gleichgewicht halten
Um zu verstehen, warum FOXJ3 so einflussreich ist, kombinierten die Forschenden mehrere groß angelegte Ansätze. Sie kartierten, wo FOXJ3 an der DNA bindet, und welche Gene in tausenden einzelnen kortikalen Zellen aktiv sind. Das wies deutlich auf Gene hin, die den Zellzyklus und das Gehirnwachstum steuern, insbesondere PTEN, eine wichtige Bremse eines Wachstumswegs namens mTOR. In Progenitorzellen förderte FOXJ3-Bindung die PTEN-Aktivität, was wiederum den Zellen half, der Teilungsphase zu entkommen, sich in Neurone zu verwandeln und geordnet nach außen zu migrieren. Wurde Foxj3 herunterreguliert, blieben mehr Progenitoren im teilenden Zustand, weniger verließen den Zyklus rechtzeitig, und die Migration stockte in Zwischenzonen. Entscheidend war, dass das Wiederherstellen von PTEN-Spiegeln in Foxj3-defizienten Gehirnen die Probleme mit Migration, Schichtung und Zellschicksal größtenteils umkehrte, während die Erhöhung eines anderen Wachstumsregulators, TSC1, dies nicht vermochte. Damit steht PTEN im Zentrum der FOXJ3-gesteuerten Kontrolle des kortikalen Aufbaus.
Von fehlregulierten Signalwegen zu vergrößerten Neuronen
Das Team fragte als Nächstes, wie patientenähnliche FOXJ3-Varianten sich verhalten. Eine krankheitsassoziierte Version von FOXJ3 konnte PTEN-Spiegel nicht anheben und erlaubte dem mTOR-Weg, überaktiv zu werden, sichtbar durch erhöhte Phosphorylierung eines wichtigen wachstumsbezogenen Proteins. In jugendlichen Mäusen, die so konstruiert waren, diese mutierte Form im sich entwickelnden Kortex zu exprimieren, erschienen die Neurone später deutlich geschwollen, mit größeren Zellkörpern und Umfängen, was den dysmorphischen Zellen bei menschlicher FCD ähnelt. Dennoch erreichte das mutierte Protein noch korrekt den Zellkern, was darauf hinweist, dass das Problem in fehlerhafter Genregulation liegt und nicht in Fehllokalisierung. Insgesamt verknüpfen diese Befunde FOXJ3-Mutationen mit einer Kaskade von Ereignissen — weniger PTEN, mehr mTOR-Signalisierung, verzögerter Austritt aus dem Zellzyklus, gestörte Migration und hypertrophe Neurone — die das Fundament für epileptische Netzwerke legen können.
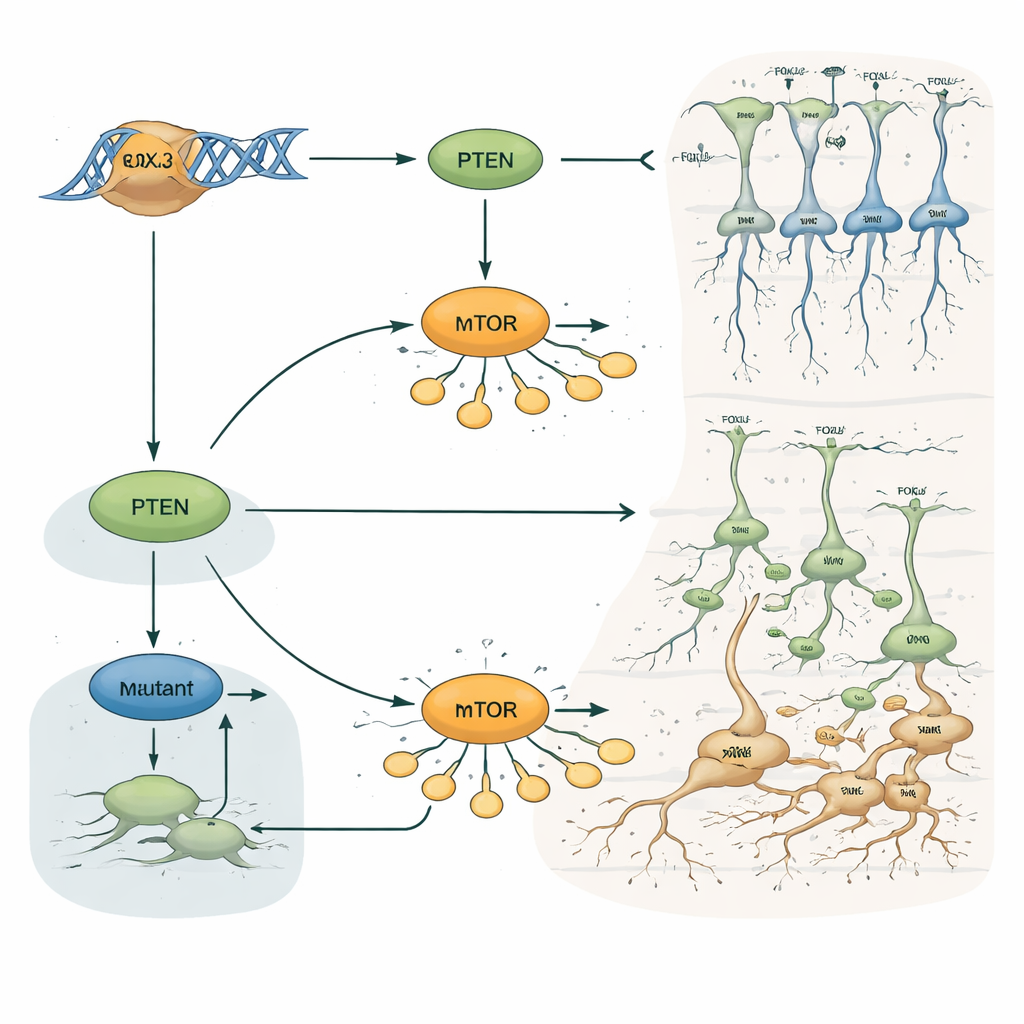
Warum das für Epilepsie und verborgene Hirnlesionen wichtig ist
Für Nicht-Spezialistinnen und -Spezialisten lautet die Kernbotschaft, dass ein einzelner Transkriptionsfaktor, FOXJ3, mitentscheidet, wann und wo kortikale Neurone entstehen, wie sie sich bewegen und in welche Schicht sie schließlich gelangen. Indem er über den PTEN–mTOR-Wachstumsweg wirkt, sorgt FOXJ3 dafür, dass der Aufbau des Gehirns nach Plan verläuft. Seltene Veränderungen in diesem Gen können dieses Gleichgewicht kippen und dazu führen, dass kleine Kortexbereiche falsch verschaltet und geschichtet sind, selbst wenn MRT-Scans normal erscheinen. Diese Arbeit schlägt nicht nur FOXJ3 als neue genetische Ursache für fokale kortikale Dysplasie und Epilepsie vor, sondern veranschaulicht auch, wie subtile Verschiebungen in der frühen Gehirnentwicklung Jahrzehnte später als schwer behandelbare Anfälle wiederhallen können.
Zitation: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Schlüsselwörter: fokale kortikale Dysplasie, FOHJ3-Gen, PTEN-mTOR-Signalweg, kortikale Entwicklung, fokale Epilepsie