Clear Sky Science · de
Verbesserte Natrium-Speicherung in Hartkohle durch Lösungsmittel-Ko-Interkalations-Elektrolyt ermöglicht Ah-Klasser-Akkus bei niedrigen Temperaturen
Warum frostfeste Batterien wichtig sind
Von Elektroautos in verschneiten Regionen bis zu Sensoren im tiefen Arktisbereich: Viele moderne Geräte benötigen Batterien, die auch bei Kälte zuverlässig funktionieren. Heutige Lithium- und Natrium-Batterien verlieren bei sehr niedrigen Temperaturen oft an Leistung oder versagen ganz, weil die zugrunde liegenden chemischen Prozesse langsamer ablaufen. Diese Studie untersucht einen neuen Ansatz für Natrium-Ionen-Batterien — mit einem speziell entwickelten Flüssigelektrolyt — sodass sie Energie zuverlässig speichern und abgeben können, selbst bei Temperaturen bis −50 °C.
Die Herausforderung gefrorener Batterien
Batterien speichern Energie, indem geladene Atome, sogenannte Ionen, zwischen zwei festen Elektroden durch ein flüssiges Elektrolyt transportiert werden. Bei Natrium-Ionen-Batterien müssen Natrium-Ionen eine dünne Oberflächenschicht überwinden und in eine kohlenstoffbasierte negative Elektrode, die sogenannte Hartkohle, eindringen. Bei niedrigen Temperaturen treten zwei Probleme auf: Ionen bewegen sich langsamer in der Flüssigkeit, und sie haben Schwierigkeiten, die sie umgebenden Lösungsmittelmoleküle vor dem Eintritt in die Hartkohle abzulegen. Gleichzeitig neigt die schützende Oberflächenschicht — die feste Elektrolyt-Grenzschicht (Solid Electrolyte Interphase, SEI) — dazu, in der Kälte dicker und widerstandsfähiger zu werden. All dies erschwert die Bewegung der Natrium-Ionen, sodass die Batterie deutlich weniger Energie liefern kann, wenn sie am meisten benötigt wird.
Ein neues Flüssigkeitsgemisch für leichteren Ionenfluss
Die Forschenden gingen das Problem an, indem sie den Elektrolyten so umgestalteten, dass Natrium-Ionen nicht mehr vollständig ihre Lösungsmittelhülle ablegen müssen, bevor sie in die Hartkohle eindringen. Sie mischten zwei ether-basierte Lösungsmittel: Diethylenglykol-Dimethylether (G2), das stark an Natrium-Ionen bindet und schnelle Ionenbewegung unterstützt, und 2-Methyloxolan (MO), eine weniger polare Flüssigkeit, die auch bei sehr niedrigen Temperaturen flüssig bleibt. In dem resultierenden „Ko-Interkalations-Elektrolyt“ koordinieren die Natrium-Ionen hauptsächlich mit G2, während MO weitgehend als freies, nicht bindendes Lösungsmittel wirkt und das Gemisch bis −50 °C flüssig hält. Computersimulationen und spektroskopische Messungen zeigten, dass dieses Gemisch eine stabile Struktur bildet, in der Natrium-Ionen und G2 gemeinsam als kleiner Cluster transportiert werden.
Ionen eintreten lassen, ohne sich zu entkleiden
Anstatt die Natrium-Ionen an der Elektrodenoberfläche dazu zu zwingen, ihre Lösungsmittelhülle abzulegen, erlaubt der neue Elektrolyt, dass die Natrium–G2-Cluster direkt durch die Oberflächenschicht gleiten und in die geschichteten Zwischenräume der Hartkohle gelangen. Dieser Vorgang, genannt Lösungsmittel-Ko-Interkalation, umgeht den langsamen „Entkleidungs“-Schritt, der die Leistung bei Kälte normalerweise begrenzt. Mikroskopische und spektroskopische Tests zeigten, dass die mit diesem Elektrolyt gebildete Oberflächenschicht dünner und anorganisch-reicher ist als in konventionellen Systemen. Diese Kombination schützt die Elektrode und lässt gleichzeitig einen schnellen Ionentransport zu. Messungen der Ionen-Diffusion und des elektrischen Widerstands bestätigten, dass Ionen sich schneller innerhalb der Kohlenstoffstruktur und über die Grenzfläche bewegen, insbesondere bei niedrigen Temperaturen.
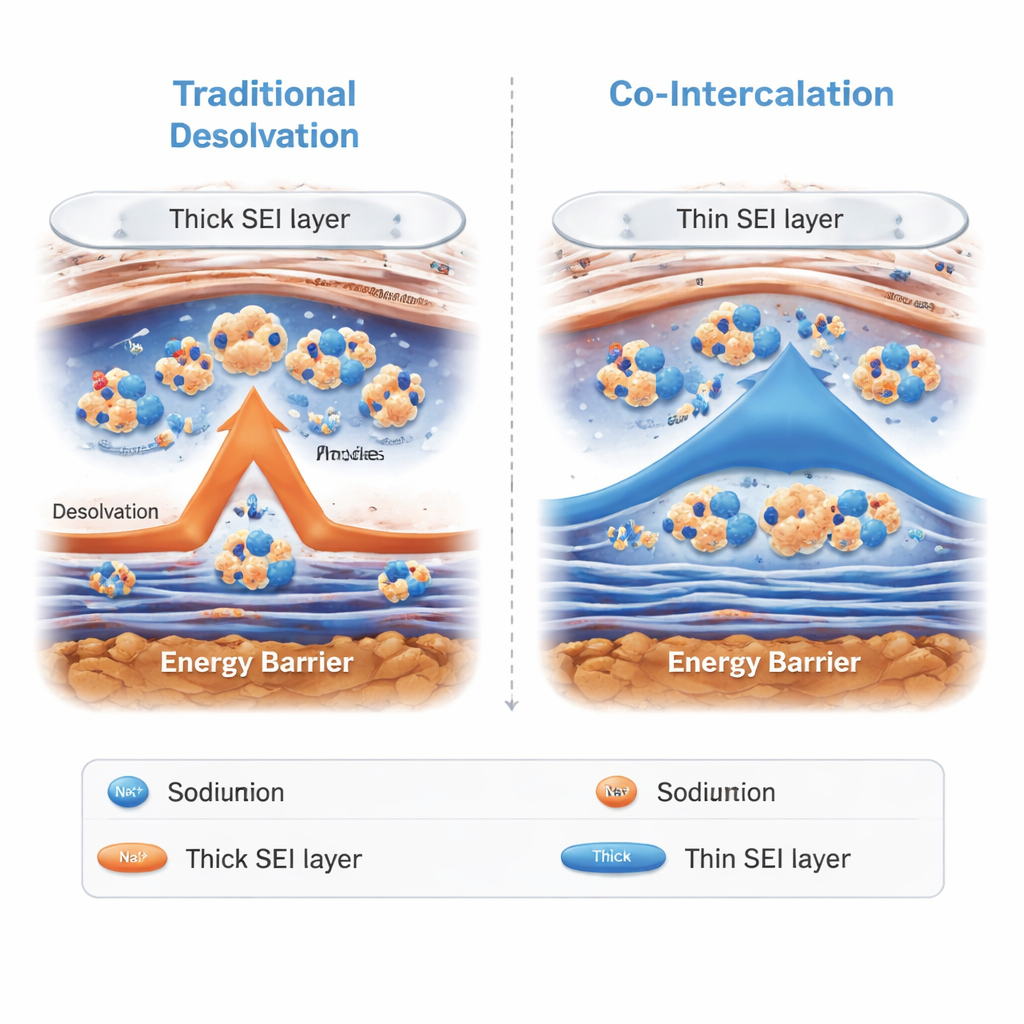
Starke Leistung selbst bei −50 °C
Als das Team münzgroße Zellen mit Hartkohle und dem neuen Elektrolyt testete, stellten sie fest, dass die Batterien von Raumtemperatur bis −50 °C eine hohe Kapazität und Effizienz beibehielten. Bei −50 °C erreichte die Hartkohle-Elektrode noch etwa 80 % ihrer anfänglichen Ladungs-Effizienz und behielt nach 200 Lade–Entlade-Zyklen über 90 % ihrer Kapazität. Über die kleinen Zellen hinaus bauten die Forschenden auch Pouch-Zellen — flache Batterien ähnlich denen in Unterhaltungselektronik — mit einer Kapazität von etwa 1,2 Amperestunden. Diese kompletten Natrium-Ionen-Batterien erreichten eine spezifische Energie von 163 Wattstunden pro Kilogramm bei Raumtemperatur und 107 Wattstunden pro Kilogramm bei −50 °C und betrieben weiterhin LED-Leuchten für mehr als 10 Stunden in einer −50 °C-Kammer.
Bedeutung für zukünftige Batterien in kalten Regionen
Für Nicht-Fachleute lautet die Kernbotschaft: Die Autorinnen und Autoren fanden einen Weg, Natrium-Ionen ihre nützliche Lösungsmittelhülle beim Eintritt in die Kohlenstoffelektrode behalten zu lassen. Indem sie einen Elektrolyt entwickelten, der in der Kälte flüssig bleibt und eine dünne, ionenfreundliche Oberflächenschicht bildet, beseitigten sie einen wesentlichen Engpass für die Leistung bei niedrigen Temperaturen. Dieser Ansatz könnte dazu beitragen, Natrium-Ionen-Batterien — eine preiswertere Alternative zu Lithium-Ionen — für den Einsatz in Winterklimata, hochgelegenen Regionen und anderen rauen Umgebungen praktikabler zu machen, in denen zuverlässige, erschwingliche Energiespeicherung dringend benötigt wird.
Zitation: Li, M., Liu, Z., Zhao, Y. et al. Enhanced sodium storage in hard carbon via solvent co-intercalation electrolyte enabling Ah-level pouch cells at low temperatures. Nat Commun 17, 1478 (2026). https://doi.org/10.1038/s41467-026-69237-y
Schlüsselwörter: Natrium-Ionen-Batterien, Niedrigtemperatur-Batterien, Elektrolyt-Design, Hartkohle-Anoden, Energiespeicherung