Clear Sky Science · de
Molekulare Grundlage der Galaktosylierung von Kollagen durch GLT25D1
Wie winzige Zuckermarken beim Aufbau starker Gewebe helfen
Kollagen ist das häufigste Protein im Körper und bildet das Gerüst für Haut, Knochen, Blutgefäße und viele andere Gewebe. Aber Kollagen wirkt nicht allein: Es muss an genau festgelegten Stellen mit kleinen Zuckermolekülen versehen werden, um die richtige Festigkeit und Flexibilität zu erhalten. Diese Studie zeigt auf atomarer Ebene, wie ein wichtiges Enzym, GLT25D1, einen bestimmten Zucker an Kollagen anfügt und wie Fehler in diesem Prozess zu brüchigen Gefäßen, Muskelproblemen und möglicherweise sogar Krebs führen können.
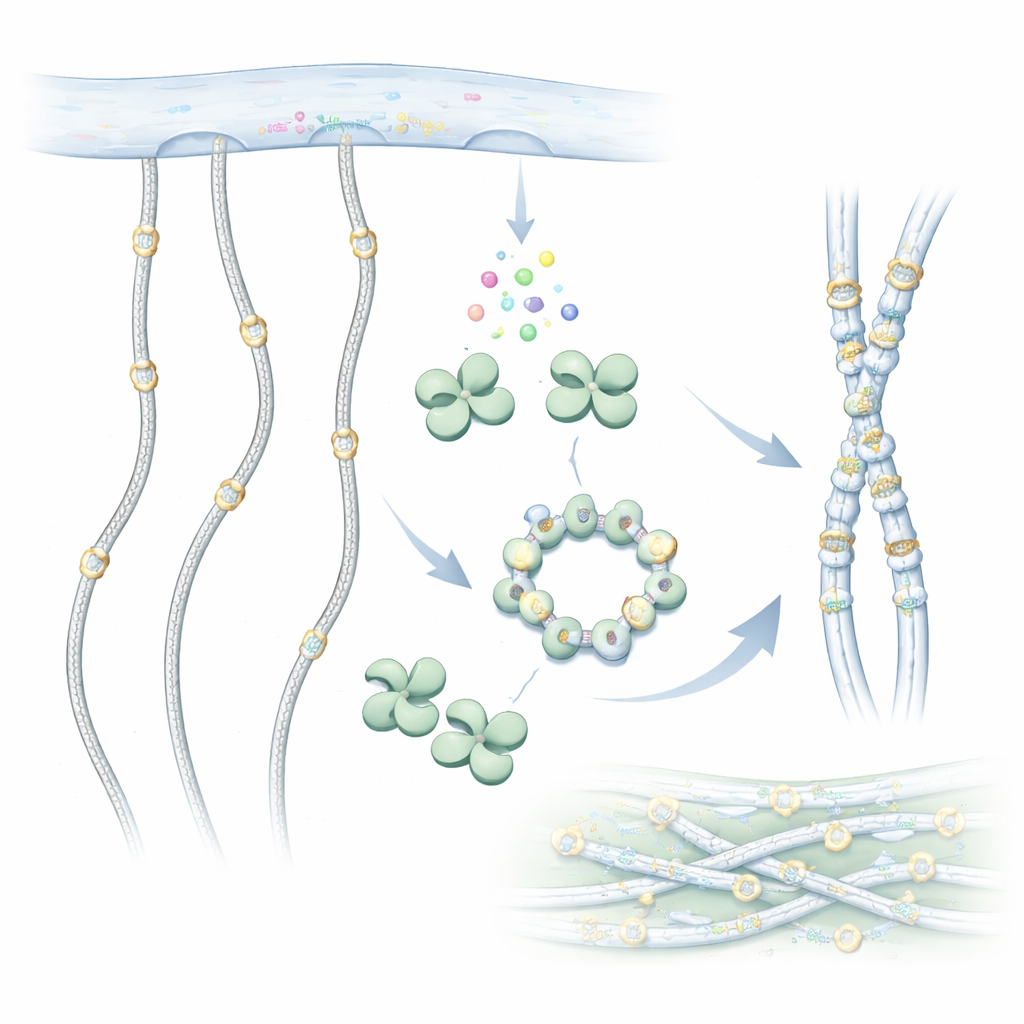
Ein genauer Blick auf Kollagens verborgene Umgestaltung
Kollagenmoleküle sind lange, seilartige Ketten, die sich außerhalb der Zellen zu stabilen Fasern zusammenlagern. Bevor sie jedoch die Zelle verlassen, werden sie chemisch nachbearbeitet. Eine wichtige Änderung ist das Anfügen von Zuckergruppen an spezielle Bausteine, die als Hydroxylysin entlang der Kollagenkette vorkommen. GLT25D1 führt den ersten Schritt dieser Zuckerkennzeichnung aus, indem es ein Galaktosemolekül von einem Donor auf das Hydroxylysin überträgt. Diese Zuckerdekoration ist von einfachen Tieren bis zum Menschen konserviert und hilft dem Kollagen, richtig zu falten, mit Zellen zu interagieren und Abrieb zu widerstehen.
Die Form eines Kollagen-Dekorateurs entschlüsseln
Um zu verstehen, wie GLT25D1 funktioniert, nutzten die Forscher Kryo-Elektronenmikroskopie, um das menschliche Enzym in nahezu atomarer Auflösung abzubilden. Sie entdeckten, dass jedes GLT25D1-Molekül zwei ähnliche Lappen besitzt, die beide zu einer häufigen Enzymfaltengruppe gehören, wie sie bei Zuckertransferasen zu finden ist. Diese Lappen paaren sich zu verlängerten Dimeren, und drei Dimerpaare können sich weiter zu einem ringförmigen Hexamer zusammensetzen. In diesen Assemblierungen liegen die eigentlichen Arbeitspferde — die katalytischen Zentren — weit voneinander entfernt, eine Anordnung, die es mehreren Zuckeranhangstellen erlauben könnte, gleichzeitig entlang einer gestreckten Kollagenkette zu arbeiten.
Die funktionalen Teile: wo der Zuckertausch wirklich geschieht
Das Team löste Strukturen von GLT25D1 in Komplex mit seinem Zucker-Donor und einem kurzen kollagenähnlichen Peptid, das Hydroxylysin enthält. Dieser ternäre Komplex zeigte, dass nur der zweite Lappen, das sogenannte C-terminale Domäne, tatsächlich die Chemie ausführt. Dort legt sich das Donormolekül in eine Tasche, die durch ein Metallion stabilisiert wird, während das Peptid in einer schmalen Furche liegt, die ein spezifisches lokales Muster erzwingt: ein Hydroxylysin, gefolgt unmittelbar von einem kleinen Glycin. Eine einzelne Aspartat-Residue wirkt als chemische Base, aktiviert die Hydroxylgruppe des Hydroxylysins, sodass sie den Zucker angreifen und die Übertragung abschließen kann. Veränderungen an einem dieser Schlüsselaminosäuren verringern oder beseitigen die Aktivität drastisch und bestätigen so ihre essenziellen Rollen.
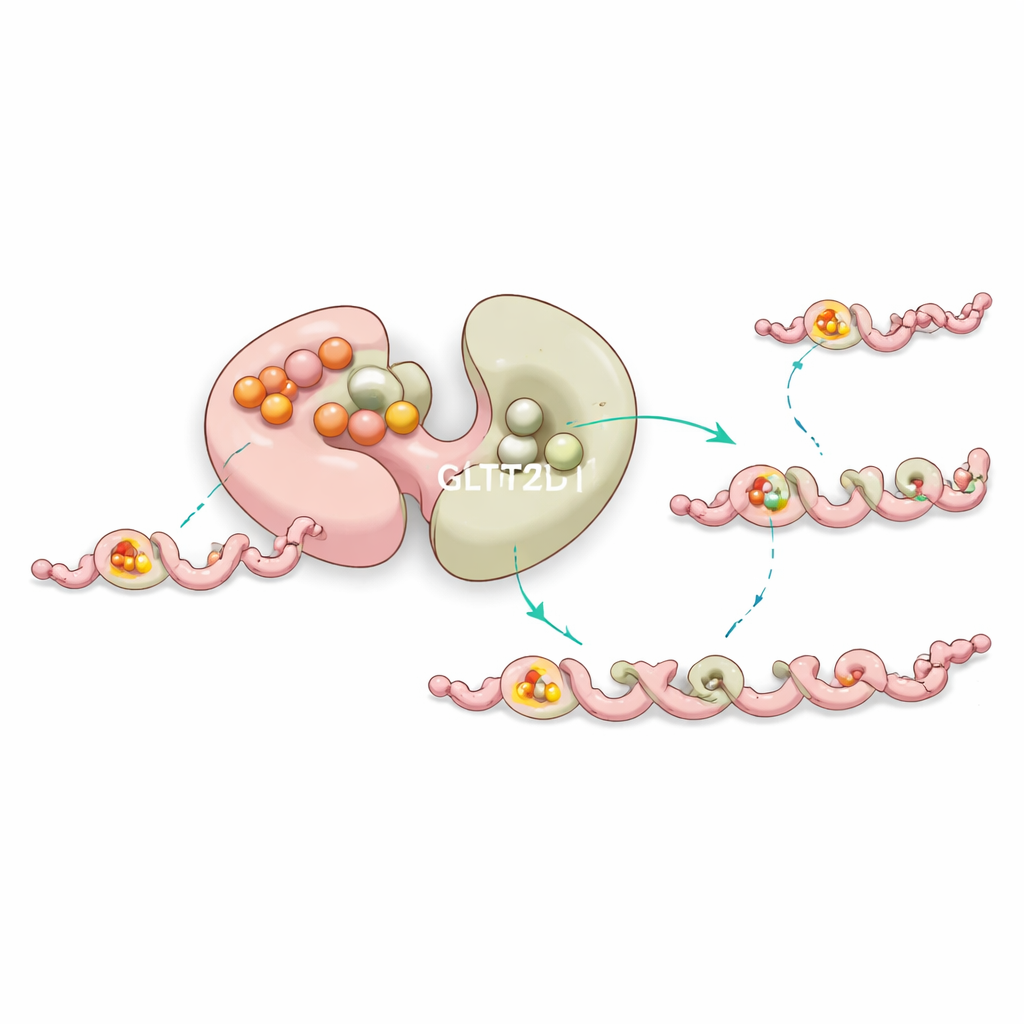
Ein eingebauter Stabilisator und Kontrolle über weite Distanzen
Eigenerweise bindet der erste Lappen von GLT25D1 einen Zucker-Donor sehr stark, führt die Übertragung jedoch nicht selbst durch. Stattdessen deuten Experimente und Computersimulationen darauf hin, dass diese „stille“ Stelle das Enzym stabilisiert und das Verhalten des aktiven Lappens durch langreichweitige Kommunikation innerhalb des Proteins subtil beeinflusst. Mutationen in der Nähe dieser nicht-katalytischen Tasche destabilisieren das Enzym häufig oder verändern seine Effizienz, was nahelegt, dass die Natur diese zusätzliche Bindungsstelle als eine Form interner Qualitätskontrolle nutzt, um die Kollagenmodifikation reibungslos laufen zu lassen.
Wenn der Dekorateur versagt: Verknüpfungen zu Krankheiten
Durch das Eintragen patientenabgeleiteter Mutationen in ihr Strukturmodell konnten die Autoren erklären, wie Fehler in GLT25D1 zu menschlichen Erkrankungen führen. Manche Mutationen entfernen den katalytischen Lappen vollständig, andere destabilisieren das Proteinkerngerüst, wieder andere treffen direkt die Zucker- oder Kollagenbindungsstellen. Diese Defekte reduzieren oder verhindern die Zuckeranlagerung an Kollagen und wurden mit Erkrankungen der kleinen Gefäße im Gehirn, kognitiven Problemen sowie Muskel- und Skelettdefekten in Verbindung gebracht. Mutationen, die mit Krebs assoziiert sind, gruppieren sich ebenfalls in kritischen Regionen, was darauf hindeutet, dass veränderte Kollagendekoration das Tumorwachstum und die Ausbreitung beeinflussen könnte.
Warum das für Gesundheit und künftige Therapien wichtig ist
Indem diese Arbeit eine detaillierte dreidimensionale Blaupause von GLT25D1 in Aktion liefert, erklärt sie, wie präzise Zuckermarken an Kollagen angefügt werden und warum dieser Schritt so wichtig für die Gewebestabilität ist. Für nicht Spezialisten lautet die Kernbotschaft: Kleine chemische Veränderungen am Kollagen können große Auswirkungen auf Blutgefäße, Knochen und möglicherweise das Krebsrisiko haben. Die strukturelle Karte von GLT25D1 bietet nun eine Grundlage, um schädliche Varianten zu diagnostizieren und Therapien zu entwerfen — sei es kleine Moleküle, die fehlerhafte Enzyme stabilisieren, oder gentherapeutische Ansätze — die eines Tages die Defekte bei der Kollagen-Zuckeranheftung an der Quelle korrigieren könnten.
Zitation: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Schlüsselwörter: Kollagen-Glykosylierung, GLT25D1, extrazelluläre Matrix, Gefäßerkrankung, cryo-EM-Struktur