Clear Sky Science · de
Sclerostinmangel macht weiße Adipozyten empfindlicher für thermogene Signale, die bei Mäusen Beiging auslösen
Warum das Aufheizen Ihres Fettgewebes Krankheiten abschwächen könnte
Die meisten von uns betrachten Knochen und Körperfett als zwei getrennte Bereiche: Das eine gibt Struktur, das andere speichert Energie. Diese Studie an Mäusen zeigt, dass Knochen und Fett in ständigem chemischen Austausch stehen und dass ein von Knochenzellen produziertes Protein entscheiden kann, ob unser „weißes“ Fett einfach nur Kalorien speichert oder sich in aktiveres, kalorienverbranntes „beiges“ Fett verwandelt. Das Verständnis dieses verborgenen Dialogs könnte neue Wege eröffnen, um Fettleibigkeit, Diabetes und Knochenschwund gleichzeitig anzugehen.
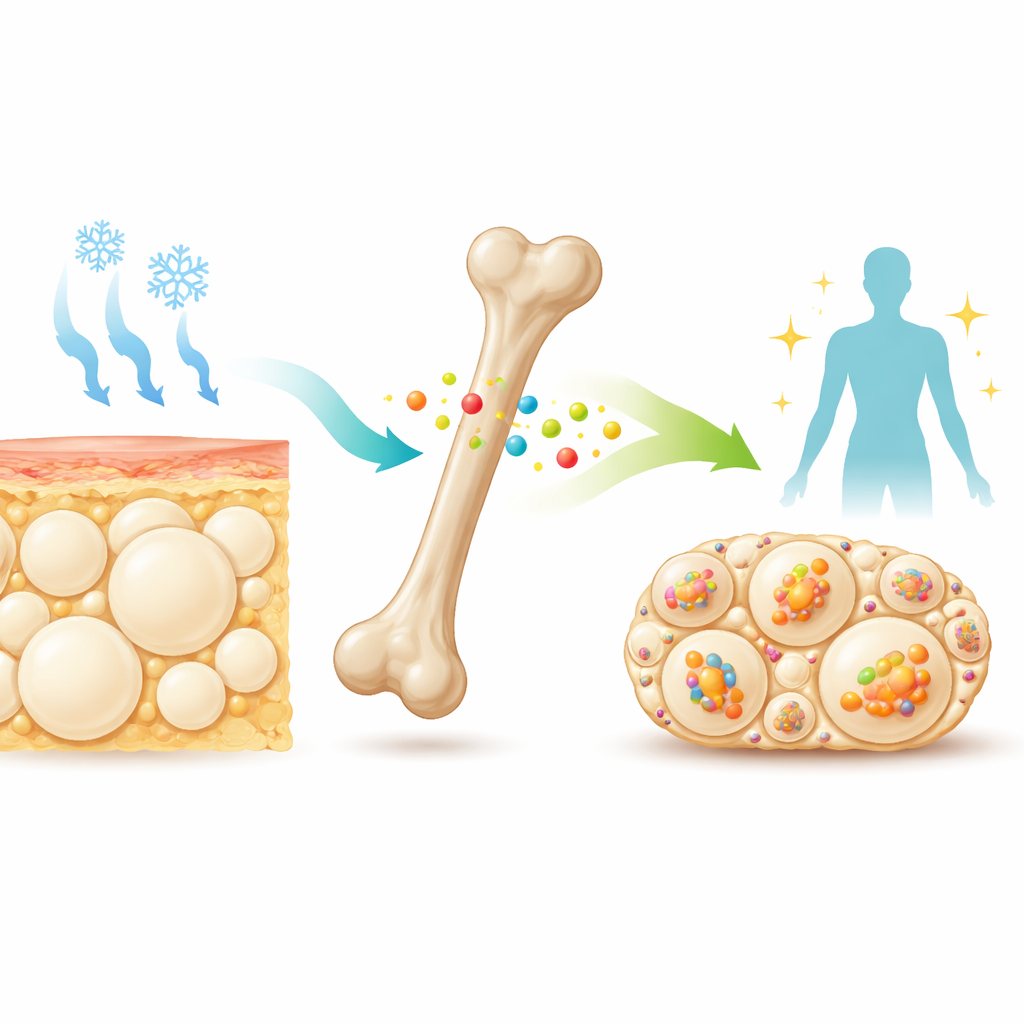
Ein stiller Bote aus dem Knochen
Tief im Inneren der Knochen geben spezialisierte Zellen ein kleines Protein namens Sclerostin in den Blutkreislauf ab. Ärztinnen und Ärzte zielen bereits mit Medikamenten auf Sclerostin ab, um bei bruchgefährdeten Patienten die Knochen zu stärken. Frühere Arbeiten zeigten, dass Mäuse ohne Sclerostin nicht nur sehr stabile Knochen haben, sondern auch schlanker sind und empfindlicher auf Insulin reagieren. Ihr subkutanes Fett, vor allem um die Hüfte (inguinales weißes Fett), enthält winzige, komplex aufgebaute Fettzellen, die wie „beiges“ Fett aussehen und Brennstoff in Wärme umwandeln können. Diese Hinweise veranlassten die Forschenden zu prüfen, ob Sclerostin normalerweise als Bremse für die Fähigkeit des Körpers wirkt, weißes Fett bei Kälteeinwirkung oder bei Wirkstoffen, die Nervensignale zum Fett nachahmen, in beige Fett umzuwandeln.
Kältesignale, Knochensignale und Aktivierung des Fetts
Das Team setzte normale Mäuse und Mäuse ohne das Sclerostin-Gen (Sost-/-) einem Wirkstoff aus, der einen bestimmten Fettzellrezeptor (β3-adrenerger Rezeptor) aktiviert, oder milder Kälte. Bei normalen Tieren erhöhten diese thermogenen Signale die Sclerostinproduktion im Knochen und hoben dessen Spiegel im Blut an. Dieser Anstieg war mit einem Verlust an schwammartiger Knochenmasse, aber nur mit geringen Veränderungen im subkutanen Fett verbunden. Im Gegensatz dazu zeigten Sclerostin-defiziente Mäuse eine deutlich stärkere Reaktion: Ihr inguinales Fett nahm mehr Glukose auf, setzte mehr Fettsäuren frei, schrumpfte und war von beige-ähnlichen Zellen durchzogen, die voller Mitochondrien, den Kraftwerken der Zelle, waren. Wichtige thermogene Gene wurden in diesen Mäusen besonders im subkutanen Fett stärker aktiviert, während klassisches braunes Fett weitgehend unverändert blieb.
Feinsteuerung des Fettabbaus über einen gemeinsamen Schalter
Um zu verstehen, wie Sclerostin diese Kontrolle ausübt, konzentrierten sich die Forschenden auf β-Catenin, ein Protein, das an der Wnt-Signalgebung beteiligt ist und das Sclerostin im Knochen normalerweise unterdrückt. Im Fett trieb die Aktivierung von β-Catenin nach der Geburt weiße Zellen in Richtung eines beige-ähnlichen Zustands und verstärkte ihre Reaktion auf β3-adrenerge Signale, doch dieser Effekt verschwand, wenn die Mäuse bei einer warmen, thermoneutralen Temperatur gehalten wurden, bei der der Körper keine zusätzliche Wärme benötigt. Umgekehrt beseitigte die gezielte Deletion von β-Catenin in Fettzellen sclerostin-defizienter Mäuse deren beiges Fett, stellte größere weiße Fettzellen wieder her und kehrte Verbesserungen bei Insulin- und Fettsäurespiegeln um. Diese Experimente legen nahe, dass bei niedrigem Sclerostin β-Catenin in Fettzellen zu einem wichtigen inneren Hebel wird, der weißes Fett empfindlicher für thermogene Signale macht.
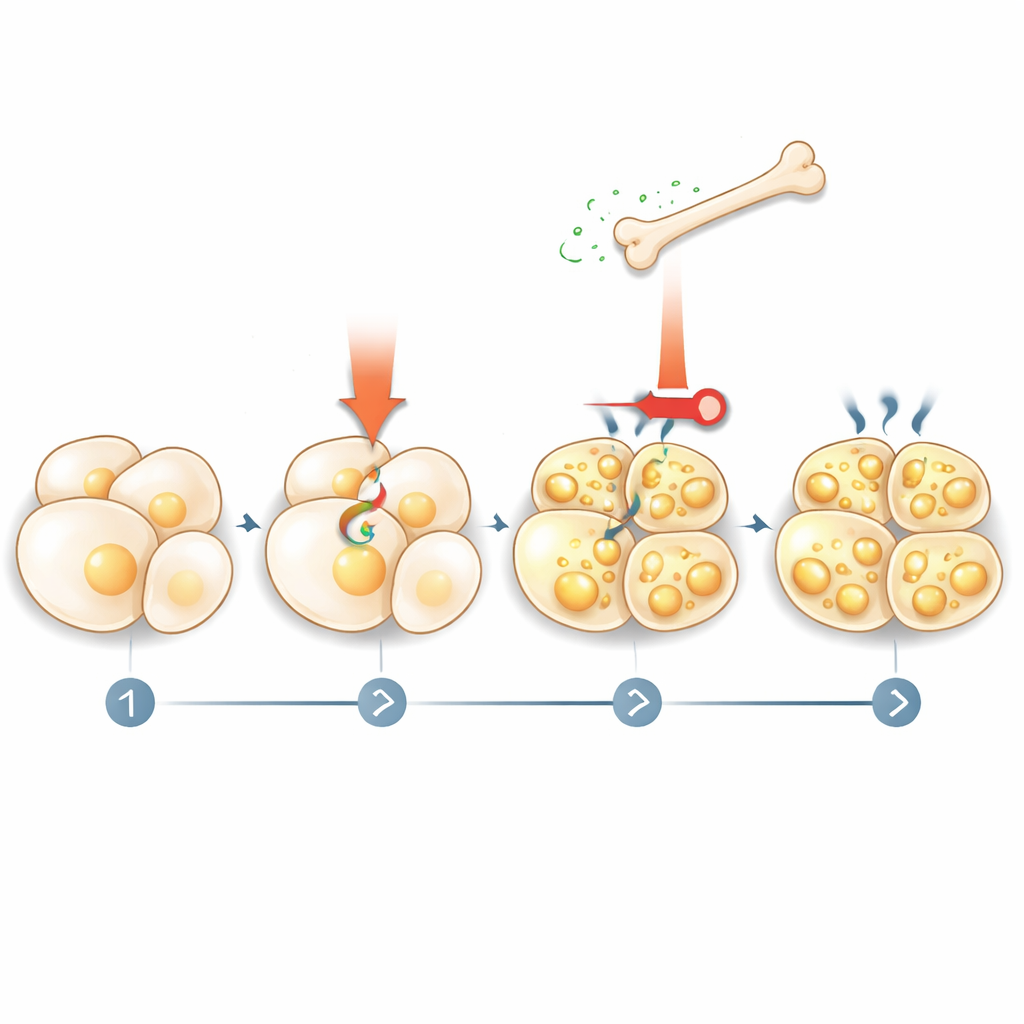
Wie Fett zum Knochen zurückspricht
Die Geschichte endet nicht damit, dass der Knochen dem Fett sagt, was zu tun ist. Das Team fand heraus, dass thermogene Stimulation den Fettabbau (Lipolyse) aktiviert und Fettsäuren ins Blut freisetzt. Diese Fettsäuren wirken wiederum über einen nukleären Rezeptor namens PPARγ auf Knochenzellen und steigern die Sclerostinproduktion. Wenn die Forschenden die Lipolyse in Fettzellen blockierten oder PPARγ in Knochenzellen entfernten, konnten kälteimitierende Wirkstoffe den Sclerostinspiegel nicht mehr erhöhen. Das zeigt einen Regelkreis: Thermogene Signale veranlassen Fett, Brennstoff freizusetzen; dieser Brennstoff veranlasst den Knochen, mehr Sclerostin zu sezernieren; und Sclerostin bremst wiederum die weitere Aktivierung und Beiging des Fetts.
Kombination von Knochen- und Fettmedikamenten für die metabolische Gesundheit
Schließlich prüften die Forschenden, ob eine Unterbrechung dieses Kreislaufs in einem krankheitsähnlichen Modell hilfreich sein könnte. Fettleibige Mäuse auf fettreicher Diät erhielten eine niedrige Dosis Mirabegron (ein β3-adrenerger Wirkstoff, der bereits bei Blasenproblemen eingesetzt wird), einen Antikörper, der Sclerostin neutralisiert (Romosozumab, zugelassen bei Osteoporose) oder beides. Während jedes Medikament allein nur moderate Effekte zeigte, reduzierte die Kombination die Fettmasse in wichtigen Depots, verschob das Fett hin zu kleineren, aktiveren Zellen, senkte Insulin, Triglyzeride und Cholesterin und erhielt die Knochendichte. Warmes Halten, das den Wärmebedarf des Körpers senkt, hob die metabolischen Vorteile des Sclerostinverlusts weitgehend auf und unterstreicht, dass dieser Pfad vor allem dann relevant ist, wenn thermogene Signale vorhanden sind.
Was das für künftige Behandlungen bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass der Knochen nicht nur ein passives Gerüst ist, sondern aktiv reguliert, wie viel Energie Fettzellen verbrennen. Sclerostin fungiert wie ein Lautstärkeregler, der die Aktivität thermogenen Fetts – und damit den Brennstoffverbrauch – in Schach hält. Dreht man diesen Regler herunter, durch Genetik oder Medikamente, werden bestimmte weiße Fettdepots aufmerksamer darin, in einen wärmeproduzierenden Modus zu wechseln, wenn der Körper durch Kälte oder bestimmte Medikamente angeregt wird. Da dieselbe Intervention bei Mäusen Knochen stärken und die metabolische Gesundheit verbessern kann, könnten sorgfältig konzipierte Kombinationen von knochen- und fettgezielten Therapien eines Tages helfen, Fettleibigkeit, Diabetes und Osteoporose zusammen zu behandeln, statt jede Krankheit einzeln anzugehen.
Zitation: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Schlüsselwörter: Sclerostin, beiges Fett, Knochen–Fett-Kommunikation, Thermogenese, metabolische Erkrankung