Clear Sky Science · de
Lokale PI(4,5)P2-Synthese durch septin-assoziierte PIPKIγ-Isoformen steuert die Assoziation von Centralspindlin mit dem Midbody während der Zytokinese
Wie Zellen das Auseinanderbrechen beenden
Die Zytokinese – der finale Einschnürungsschritt, der eine Zelle in zwei teilt – wird leicht als selbstverständlich hingenommen; wenn sie jedoch fehlschlägt, kann das zur Entstehung von Krebs und anderen Erkrankungen beitragen. Diese Studie enthüllt, wie ein bestimmter Satz von Molekülen wie Bauleiter an der schmalen Brücke zwischen zwei Neuzellen wirkt und dafür sorgt, dass die Trennung sauber abgeschlossen wird, anstatt zurückzuschnappen oder zu stocken.
Die letzte Brücke zwischen Tochterzellen
Nachdem eine Zelle ihr genetisches Material verdoppelt und die Chromosomen getrennt hat, muss sie sich physisch teilen. Ein kontraktiler Ring aus Proteinfilamenten zieht sich um die Zellmitte zusammen und bildet eine tiefe Furche, die als Teilungsfurche bezeichnet wird. Während diese Furche nach innen zieht, bleiben die beiden Tochterzellen durch eine dünne interzelluläre Brücke verbunden, die einen dichten Kern, den Midbody, enthält. Der Midbody ist eine winzige, aber komplexe Struktur aus gebündelten Mikrotubuli, Gerüstproteinen und signalgebenden Lipiden; er fungiert sowohl als Verbindung als auch als Schaltzentrum, das die letzten Schritte der Teilung und den finalen Schnitt zwischen den Zellen koordiniert. 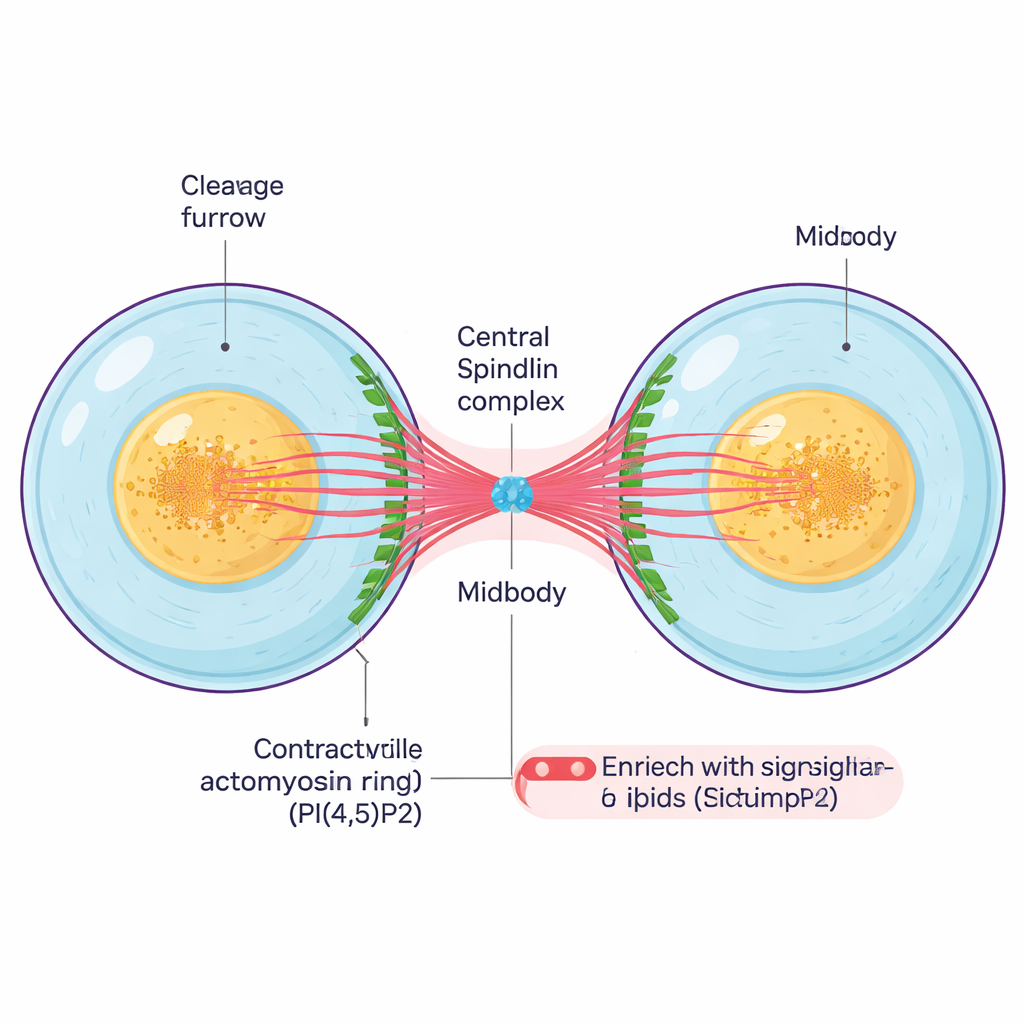
Ein Lipidsignal, das am richtigen Ort sein muss
Ein Schlüsselspieler in diesem Prozess ist ein signalgebendes Fettmolekül in der Zellmembran, genannt PI(4,5)P2. Dieses Lipid hilft, viele Proteine zu verankern, die den kontraktilen Ring aufbauen und verengen sowie die Brücke stabilisieren. Rätselhaft war, wie Zellen steuern, wo und wann PI(4,5)P2 auftritt, da es in der Membran diffundieren kann. Die Autor*innen konzentrierten sich auf Enzyme der Typ-I-PIP-Kinasen, die PI(4,5)P2 herstellen, insbesondere auf ein Gen, PIPKIγ, das in mehreren subtil verschiedenen Spleißformen vorliegt. Durch selektives Reduzieren jeder Kinase in menschlichen Zellen und Beobachtung der Effekte mit fortgeschrittener Mikroskopie fanden sie heraus, dass PIPKIγ eine besondere Rolle spät in der Zytokinese spielt, wenn die Brücke und der Midbody sich formen, obwohl es die Gesamtmenge an PI(4,5)P2 an der Zelloberfläche nicht stark verändert.
Septin-Gerüste rekrutieren ein spezialisiertes Enzym
Das Team entdeckte, dass zwei Spleißvarianten von PIPKIγ, genannt i3 und i5, wie präzise Werkzeuge wirken, die an den richtigen Ort von Strukturproteinen, den Septinen, gebracht werden. Septine bilden Filamente und Ringe, die helfen, die Brücke zu formen und andere Komponenten zu organisieren. Biochemische Pull-downs und Zellbildgebung zeigten, dass PIPKIγ-i3 und PIPKIγ-i5 physikalisch an Septinkomplexe binden und Septinfilamente besetzen, während andere PIPKIγ-Varianten dies nicht tun. Wenn die Forschenden zwei spezifische Aminosäuren in diesen Spleißeinfügungen mutierten, konnten die Enzyme Septine nicht mehr binden. In teilenden Zellen verlagern sich normale PIPKIγ-i3/i5 von einem diffusen Membranmuster zu einer Konzentration an der Teilungsfurche und umrahmen dann die interzelluläre Brücke und den Midbody im Einklang mit Septinen und einem weiteren Gerüstprotein, Anillin. Entfernt man nur die i3- und i5-Varianten, zerstreuen sich Anillin und Septine entlang der Brücke vom Midbody weg, und viele Zellen scheitern bei der Zytokinese und enden mit mehreren Zellkernen.
Lokale Lipidproduktion verankert die Teilungsmaschinerie
Um zu testen, ob diese Effekte von lokaler PI(4,5)P2-Produktion abhängen, maßen die Autor*innen PI(4,5)P2 in der Umgebung des Midbodies und manipulierten Enzyme, die dieses Lipid hinzufügen oder entfernen. Das Depletieren von PIPKIγ-i3/i5 verringerte PI(4,5)P2 am Midbody, während das Blockieren einer PI(4,5)P2-abbauenden Enzymaktivität den gegenteiligen Effekt hatte. Wichtig: Die Wiederherstellung einer normalen, septin-bindenden, katalytisch aktiven PIPKIγ-Spleißform rettete die richtige Clusterbildung von Anillin und Septinen an der Brücke, während kinase-tote oder septinbindungsdefiziente Mutanten dies nicht taten. Mithilfe von Live-Imaging und einer Expansionsmikroskopie-Technik, die die Probe physikalisch aufbläht, um feine Details sichtbar zu machen, zeigten die Forschenden, dass ohne PIPKIγ-i3/i5 Septine nicht mehr auf Brückenmikrotubuli übergehen, die Brücke kürzer und weniger gebündelt wird und ein entscheidender Komplex namens Centralspindlin es nicht schafft, eng mit dem Midbody assoziiert zu bleiben. 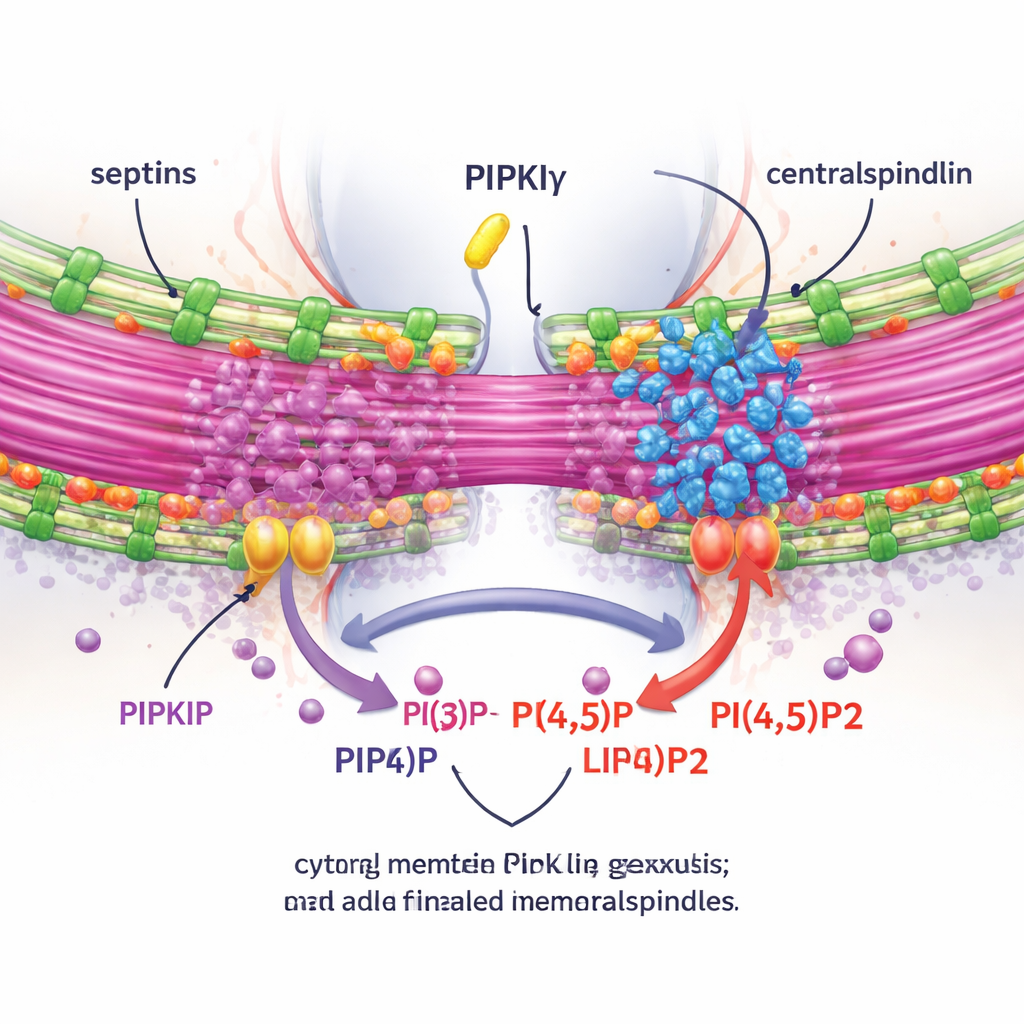
Aufbau einer Kontrollstation für einen sauberen Schnitt
Centralspindlin hilft, die Mikrotubuli des Midbodies mit der umgebenden Membran zu verbinden und reguliert kleine molekulare Schalter, die die Zellform steuern. Die Studie zeigt, dass Centralspindlin sowohl mit Septinen als auch mit PIPKIγ assoziiert und dass der Verlust eines dieser Partner seine Präsenz am Midbody ähnlich schwächt. Die Autor*innen schlagen vor, dass Septine PIPKIγ-i3/i5 zur eingesunkenen Furche rekrutieren, wo diese Enzyme einen konzentrierten Patch von PI(4,5)P2 erzeugen. Dieser lokale Lipid-Pool stabilisiert wiederum Anillin, Centralspindlin und Septine in der Nähe des Midbodies, fördert das Bündeln und die Stabilisierung der Brückenmikrotubuli und ermöglicht es der interzellulären Brücke, zu reifen, bis der finale Abscissionsschnitt erfolgt. Wird dieses System gestört, erscheint PI(4,5)P2 an falschen Stellen, Gerüstproteine dispersieren, Mikrotubuli sind schlecht gebündelt, und die Zytokinese schlägt häufig fehl.
Warum das über die Zellbiologie hinaus wichtig ist
Indem aufgezeigt wird, wie spezifische PIPKIγ-Spleißvarianten und Septine zusammenarbeiten, um am Midbody ein lokales Lipidsignal zu erzeugen, erklärt diese Arbeit, wie Zellen räumliche Präzision für ein hochgradig mobiles Signalmolekül schaffen. Diese Präzision ist entscheidend für den sicheren Abschluss der Zellteilung und hilft, Chromosomenfehlverteilungen und abnorme Zellzahlen zu verhindern, die Tumorentstehung begünstigen können. Dieselben Midbody-Strukturen beeinflussen auch das Schicksal und die Proliferation von Zellen nach der Teilung, sodass das Verständnis ihres Aufbaus neue Wege eröffnet, um zu erforschen, wie Fehler in diesen nanoskaligen Gerüsten zu Krebs beitragen könnten und möglicherweise wie man Stammzellen gezielt beeinflussen kann.
Zitation: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Schlüsselwörter: Zellteilung, Zytokinese, signalisierende Lipide, Septine, Krebsbiologie